Sono un’igienista dentale e lavoro nell’ambito della prevenzione orale fin dagli anni ‘80. Mi occupo anche di formazione e organizzo corsi rivolti ai colleghi. In questi trent’anni ho vissuto in prima persona i cambiamenti dell’odontoiatria e il modo in cui si è evoluto il concetto di prevenzione. In questo articolo, ripercorrerò le innovazioni più significative che hanno interessato la terapia parodontale. Cambiamenti avvenuti sia sul piano della comunicazione, ma anche ell’interpretazione della malattia e degli strumenti.
Anni ottanta: Nel 1965 il ricercatore H. Loe dimostrò la relazione di causa-effetto della placca batterica sullo sviluppo della gengivite. Fino ad allora, i batteri non erano ritenuti la causa primaria dei problemi gengivali, anche se molti anni prima Charles Bass (1875-1975), studioso di malattie tropicali, aveva dimostrato che pulendo bene con spazzolino e filo i problemi gengivali miglioravano. La divulgazione di alcuni concetti basilari della parodontologia impiegarono quasi due decenni per raggiungere il mondo odontoiatrico. Molti dentisti generici, fino alla fine degli anni Ottanta, consideravano la rimozione del tartaro più un fattore cosmetico che curativo. Il sanguinamento gengivale non veniva collegato alla presenza batterica e lo spazzolamento era spesso sconsigliato per non ferire la gengiva.
Si asportava il tartaro usando scaler grossolani, mentre le macchie si eliminavano con polvere di pomice mischiata con acqua. Il trattamento della parodontite consisteva per lo più nella rimozione del dente e la sua sostituzione con ponti fissi e protesi mobili. Giovani dentisti italiani formati negli Usa fondarono nel 1979 la SIDP (Società Italiana di Parodontologia). Negli anni ’90 ebbi la fortuna di collaborare con uno dei soci fondatori della SIDP, il dott. Carlo Mazzocco di Padova, con il quale approfondii le mie conoscenze di terapia parodontale non chirurgica.
Anni novanta: L’interesse per la parodontologia cresceva, pur restando un settore di nicchia. Si svilupparono conoscenze sulla specificità batterica (Miller 1973)1 e iniziò una nuova era di ricerche basate sull’impiego di antisettici e sull’impiego degli antibiotici. Si puntò verso la terapia rigenerativa guidata, fino all’estetica muco-gengivale. La terapia parodontale non chirurgica (TPNC) era considerata propedeutica agli eventuali trattamenti chirurgici.
Si procedeva con curette sito-specifiche di Gracey e la rimozione del cemento infetto era tra gli obiettivi della terapia. Levigare la radice tramite il “root planning” era al centro della terapia parodontale non chirurgica (TPNC), e anche il curettaggio dei tessuti molli era compreso nelle procedure. Si eliminavano molti batteri, l’infiammazione regrediva velocemente, ma sopraggiungevano forti problemi di ipersensibilità. La clorexidina era ampiamente utilizzata e i trattamenti desensibilizzanti erano prevalentemente a base di fluoruri. La comunicazione con il paziente parodontopatico era basata su un modello che poneva la terapia stessa e il suo successo come focus della comunicazione. Si impartivano tecniche di spazzolamento standardizzate e spesso difficili da attuare.
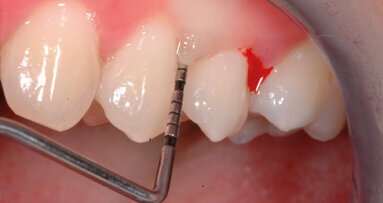
Anni duemila: la clinica fu innovata con la tecnica del Periodontal Debridement (PD). In particolare, la tecnica del Debridment nacque con il passaggio dalla teoria sulla specificità della placca, alla interazione tra placca, ospite e risposta immunitaria. Un soggetto con una “certa soglia” di tollerabilità del suo microbioma orale, si dimostrò, avrebbe potuto risolvere i problemi di infiammazione al di sotto di tale soglia2. Inoltre si scoprì che l’LPS, tossina batterica che innesca meccanismi distruttivi sul parodonto, non penetra il cemento; anzi, lo stesso cemento può aiutare la rigenerazione dei tessuti. Terapia chirurgica e non chirurgica non puntano più all’estensiva levigatura radicolare 3, 4. Con il debridement, ovvero la rimozione dei tessuti infetti fino ad arrivare a quelli sani, si affermava una terapia di decontaminazione della tasca con l’impiego di strumenti ultrasonici specifici per il parodonto. Il risultato della terapia, da quel momento in poi, si misurerà in base alla risposta dei tessuti (assenza di infiammazione) e a un indice di sanguinamento al sondaggio negativo (BoP, Bleeding on Probe). La rimozione del tartaro rimane indispensabile per una effettiva riduzione dell’infiammazione a lungo termine5, 6.
Da Placca dentale a Biofilm
Nello stesso periodo, si individuò nel biofilm il responsabile delle malattie di tipo cronico e delle infezioni nell’organismo. Fu dimostrato che la disgregazione meccanica, con spazzolino e strumentazione interdentale, abbatteva gli effetti negativi del biofilm dentale e gengivale. Lo spazzolino elettrico fu un’autentica rivoluzione, provando un’efficacia maggiore rispetto allo spazzolino manuale7, l’efficacia disgregante dei sistemi roto-oscillanti e sonici rimettono in discussione anche le vecchie tecniche manuali spesso fallimentari per la difficoltà di attuazione.
OSFMD One Stage Full Mouth Disinfection
Nel 2000 furono pubblicati gli studi dell’Università di Berna e del ricercatore Quirynen et al.8, 9. OSFMD si traduce in “disinfezione totale della cavità orale in un unico tempo” e consiste nella decontaminazione, strumentale e chimico-farmacologica, delle tasche parodontali. Lo scopo è evitare la ricontaminazione dei siti trattati da quelli infetti. Il paziente dev’essere trattato in un’unica seduta, o al massimo nell’arco di due appuntamenti nelle 24 ore che possono durare dalle 2 alle 6 ore. La superiorità del protocollo FMD, rispetto a un protocollo classico a quadranti e in appuntamenti distanziati10, non è stata ancora dimostrata. Ma la sua logica scientifica plausibile ha offerto alla TPNC un nuovo approccio terapeutico.
Gli anni 2010:L’evoluzione delle conoscenze e la scoperta delle correlazioni tra la salute orale e il benessere dell’organismo posizionano la TPNC in un contesto di salute globale del paziente. Ridurre il biofilm patogeno e mantenere la funzione masticatoria in una bocca salubre, oggi non è più un miraggio. Nell’era della medicina predittiva osserveremo sempre più l’utilizzo di marcatori biologici che indirizzino la prevenzione orale verso un trattamento personalizzato ed ecologico. La nuova classificazione del paziente parodontale esprime molto bene il cambiamento che sta avvenendo. Essa non si limita più ad una stadiazione della patologia, ma associa anche la valutazione biologica del paziente.
Oggi una nuova tecnologia meccanica imprime una svolta al trattamento parodontale: l’uso di polveri organiche molto sottili, veicolate con sistemi di air-polish APT (AIr-Polish Therapy)11. Il trattamento risulta molto confortevole per il paziente e permette di eliminare il biofilm sopra e sottogengivale, nella terapia di supporto, con una efficacia paragonabile all’uso degli ultrasuoni con inserti parodontali, riducendo inoltre i tempi del mantenimento.
L’educazione del paziente oggi è basata sulla partecipazione attiva e consapevole sia dei rischi sia dei risultati. L’uso dello spazzolino e degli strumenti domiciliari in generale è personalizzato e il risultato dell’efficacia si misura più con la risposta dell’organismo, e meno con la percentuale di placca residua, e così viene fatto con i tempi della terapia di supporto. Il controllo del biofilm orale ed il ruolo educativo dell’igienista dentale rimane il cardine indissolubile per il successo della terapia parodontale
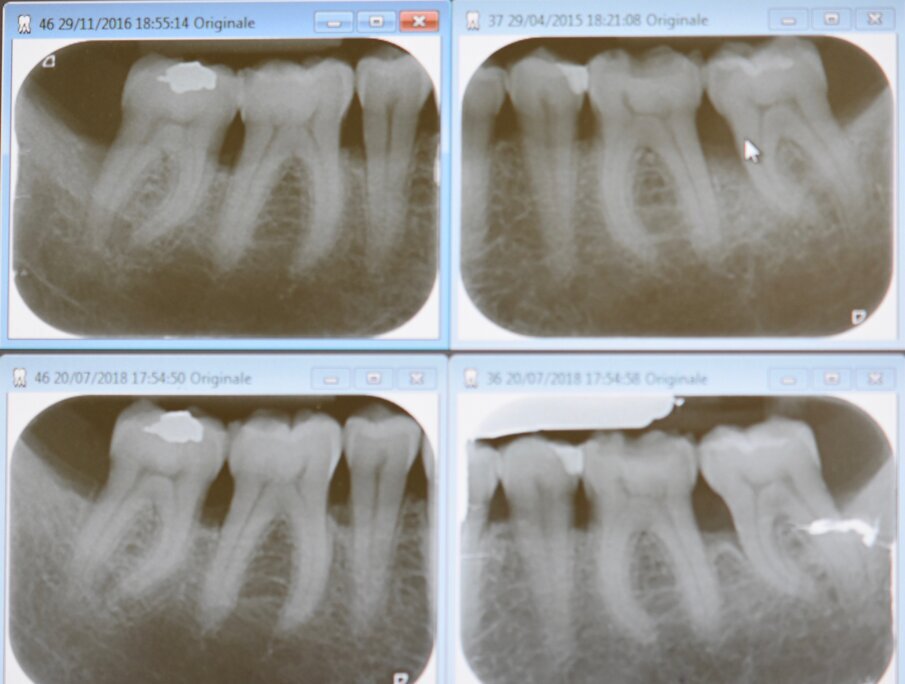
Fig. 1 - Miglioramento dei siti trattati con TPNC evidenziabile attraverso l’RBL (Radiographyc Bone Loss) in un paziente con parodontite di Stadio III e Grado A.
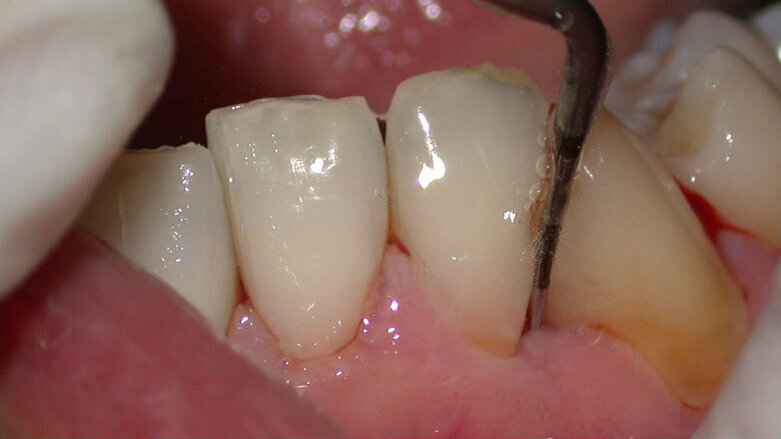
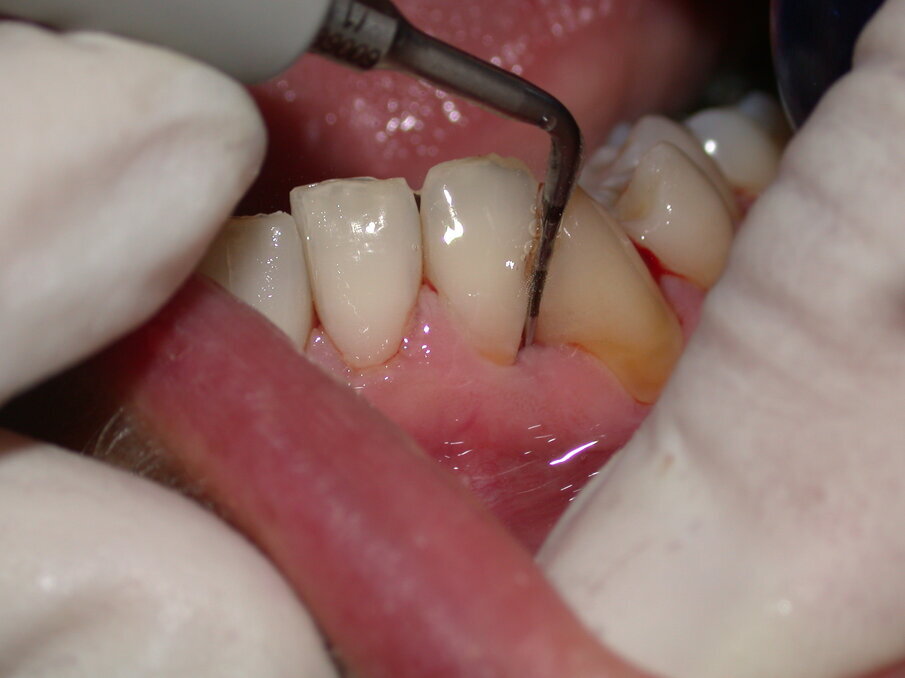
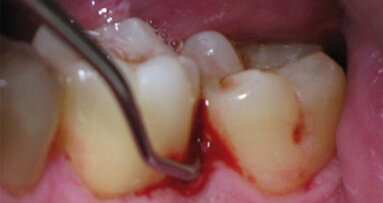
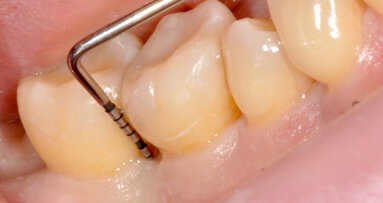
Fig. 2 - Debridement Parodontale con inserto specifico 10Z Acteon Satelec da utilizzare con basse e medie potenze.
Bibliografia
- Miller WD.. Micro-organisms of the humans mouth. Basel Switzerland, 1973, S Karger.
- Robertson PB.. The residual calculus paradox. J Periodontol 61:65, 1990.
- Mombelli A, Nyman S., Brägger U., Wennström J., Lang NP.. Clinical And Microbiological Changes Associated With An Altered Subgingival Environment Induced By Periodontal Pocket Reduction. J Clin Periodontol. 1995 Oct;22(10):780-7.
- Woodall IR., Stutsman Young N., O’Hehir TE.. Comprehensive Dental Hygiene Cap 25 Periodontal Debridement , Ed. Mosby 1993.
- Wilson TG., Harrel SK., Nunn ME., Francis B., Webb K..The relationship between the presence of tooth-borne subgingival deposits and inflammation found with a dental endoscope. J Periodontol.2008 Nov;79(11):2029-35.
- Checchi L., Montevecchi M., Checchi V., Zappulla F.. The Relationship Between Bleeding on Probing and Subgingival Deposits. An Endoscopical Evaluation Open Dent J. 2009; 3: 154–160.
- Van der Weijden FA., Campbell SL., Dorfer CE., Gonzalez-Cabezas C.. Slot DE Safety of oscillating-rotanting powered compared to manual toothbrushes: a stigmatic review. J Periodontol 2011 Jan; 82(1):5-24.
- Bollen CM., Vandekerckhove BN., Papaioannou W., Van Eldere J., Quirynen M.. Full vs. partial-mouth disinfection in the treatment of periodonti infections. A pilota study: long-team microbiologica observations. J Clin Periodontol 1996 Oct;23(109:960-70).
- Quirynen M., Mongardini C., de Soete M., Pauwels M., Coucke W., van Eldere J., van Steenberghe D.. The rôle of chlorhexidine in the one-stage full-mouth disinfection treatment of patients with advanced adult periodontitis. Long-term clinical and microbiological observations. J. Clin. Periodontol. 2000;27(8):578–589.
- Pockpa AD., Soueidan A., Louis P., Coulibaly NT., Badran Z., Struillou X..Twenty Years of Full-Mouth Disinfection: The Past, the Present and the Future.Open Dent J. 2018 May 31;12:435-442. doi: 10.2174/1874210601812010435. eCollection 2018.
- Cobb CM., Daubert DM., Davis K., Deming J., Flemmig TF., Pattison A., Roulet JF., Stambaugh RV.. Consensus Conference Findings on Supragingival and Subgingival Air Polishing. Compend Contin Educ Dent.2017 Feb;38(2):e1-e4.
La parodontite è la prima causa di perdita di denti nella popolazione adulta nei Paesi industrializzati e presenta molteplici ripercussioni sulle ...
La strumentazione parodontale non chirurgica è necessaria come trattamento iniziale, e come terapia di mantenimento, di qualsiasi patologia ...
Paziente di sesso femminile, 30 anni, non fumatrice, con anamnesi sistemica silente, assenza di allergie a farmaci e sostanze alimentari, familiarità ...
La malattia parodontale è una patologia cronica che colpisce i tessuti di supporto dei denti ed è caratterizzata da infiammazione, sanguinamento gengivale...
Le malattie parodontali possono causare gravi invalidità quali la perdita o la riduzione della funzionalità dell’apparato ...
Il Centro Corsi ProEd di Torino ospiterà anche nel 2015 il consolidato percorso formativo teorico-pratico “La terapia parodontale: Chirurgia ...
I più recenti dati epidemiologici confermano la parodontite come una delle principali patologie croniche del cavo orale, con una prevalenza stimata di ...
L’evoluzione nelle conoscenze sul microbiota e sulle problematiche orali ha cambiato radicalmente i piani di trattamento nelle varie tipologie di ...
Introduzione
La parodontite è una malattia infettiva caratterizzata dalla perdita di strutture di supporto del dente quali il tessuto connettivo e ...
La malattia parodontale è una patologia infiammatoria mediata dalla risposta dell’ospite causata dal biofilm batterico. La terapia causale si basa sul ...
Live webinar
mer. 3 giugno 2026
19:00 (CET) Rome
Live webinar
gio. 4 giugno 2026
20:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
18:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
19:00 (CET) Rome
Dr. Anthony Mak B.D.S, Prof. Marleen Peumans
Live webinar
lun. 8 giugno 2026
20:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
17:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
20:00 (CET) Rome
Nacho Fernández-Baca DDS, MSc



 Austria / Österreich
Austria / Österreich
 Bosnia ed Erzegovina / Босна и Херцеговина
Bosnia ed Erzegovina / Босна и Херцеговина
 Bulgaria / България
Bulgaria / България
 Croazia / Hrvatska
Croazia / Hrvatska
 Repubblica Ceca e Slovacchia / Česká republika & Slovensko
Repubblica Ceca e Slovacchia / Česká republika & Slovensko
 Francia / France
Francia / France
 Germania / Deutschland
Germania / Deutschland
 Grecia / ΕΛΛΑΔΑ
Grecia / ΕΛΛΑΔΑ
 Ungheria / Hungary
Ungheria / Hungary
 Italia / Italia
Italia / Italia
 Paesi Bassi / Nederland
Paesi Bassi / Nederland
 nordisch / Nordic
nordisch / Nordic
 Polonia / Polska
Polonia / Polska
 Portogallo / Portugal
Portogallo / Portugal
 Romania e Moldavia / România & Moldova
Romania e Moldavia / România & Moldova
 Slovenia / Slovenija
Slovenia / Slovenija
 Serbia e Montenegro / Србија и Црна Гора
Serbia e Montenegro / Србија и Црна Гора
 Spagna / España
Spagna / España
 Svizzera / Schweiz
Svizzera / Schweiz
 Turchia / Türkiye
Turchia / Türkiye
 Gran Bretagna e Irlanda / UK & Ireland
Gran Bretagna e Irlanda / UK & Ireland
 Internazionale / International
Internazionale / International
 Brasile / Brasil
Brasile / Brasil
 Canada / Canada
Canada / Canada
 America Latina / Latinoamérica
America Latina / Latinoamérica
 USA / USA
USA / USA
 Cina / 中国
Cina / 中国
 India / भारत गणराज्य
India / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
 Medio Oriente / Middle East
Medio Oriente / Middle East




















































To post a reply please login or register