Introduzione
La parodontite è una malattia infettiva caratterizzata dalla perdita di strutture di supporto del dente quali il tessuto connettivo e l’osso alveolare. La placca ed i batteri sono generalmente riconosciuti come la causa principale della malattia parodontale.1,2
Oggi,lo scaling e root planning (SRP) rappresenta la procedura più usata nel trattamento della malattia parodontale.3 Il suo scopo è la rimozione del biofilm subgengivale, che ha un ruolo importante nella inizializzazione e nella progressione della malattia.2
Questa procedura non è incruenta, e comporta lo sviluppo di una ferita a carico della parete interna della gengiva. Generalmente la sua guarigione induce la formazione di un epitelio giunzionale lungo piuttosto che un nuovo attacco connettivale.4
La guarigione delle ferite in siti non orali è stata studiata approfonditamente.5 In linea di principio, dopo un trauma si forma un coagulo di sangue. Questo ha due funzioni principali. È in grado di proteggere i tessuti e produce una matrice provvisoria che collega saldamente due superfici per permettere la migrazione di cellule indifferenziate (vedi la guarigione delle fratture delle ossa lunghe).5
Sebbene un gran numero di globuli bianchi raggiunga il coagulo entro poche ore, proteggendo la ferita dalla colonizzazione batterica, già dopo tre giorni la risposta infiammatoria diminuisce di intensità, e i macrofagi migrati nella ferita, secernendo polipeptidi, vengono coinvolti nelle fasi successive della guarigione.5 Vale la pena ricordare che queste cellule svolgono un ruolo chiave nella formazione del tessuto di granulazione, inducendo la guarigione attraverso la liberazione di fattori di crescita e citochine. In aggiunta, i fibroblasti differenziatisi producono una nuova matrice ricca di collagene, in modo che le cellule endoteliali possano migrare per formare vasi e collegamenti vascolari.6
Per quanto riguarda le cellule epiteliali, queste proliferano dallo strato basale e migrano attraverso il coagulo di fibrina per sigillare la breccia nell’epitelio. La maturazione del tessuto di granulazione porterà alla “rigenerazione” o “riparazione” della ferita. Due condizioni faranno sì che la rigenerazione piuttosto che la riparazione siano possibili: la disponibilità delle cellule richieste e la presenza/assenza di indizi e segnali necessari per stimolare queste cellule.7
Sebbene i suddetti principi di guarigione siano stati osservati in siti non orali, tali principi possono essere applicati ai processi di guarigione che avvengono dopo il trattamento parodontale, anche se alcune condizioni anatomiche possono rendere la guarigione più complessa.
Prima di tutto, i margini della ferita sono costituiti da un tessuto connettivo vascolare gengivale e epitelio, da un lato, e la superficie rigida non vascolare e mineralizzata del dente dall’altro. Quindi, il dente si trova in una posizione trans-gengivale, dove la radice è in un ambiente asettico mentre la corona è in un ambiente contaminato.8
Gli eventi che accadono durante la guarigione dell’interfaccia dento-gengivale sono stati studiati da Wikesjo et al. utilizzando blocchetti di dentina posti sotto un lembo gengivale nei cani.8 In pochi minuti un coagulo di fibrina si aggrega vicino alla superficie della radice. Successivamente si instaura il processo infiammatorio.
Dopo 7 giorni, un attacco di tessuto connettivale può essere visto sulla superficie della radice. Entro 14 giorni le fibre di collagene sembrano essere attaccate costantemente alla dentina.8,9,10
L’integrità funzionale di una ferita parodontale matura è stata esaminata da alcuni autori. Questi hanno sottolineato il fatto che, dopo un piccolo intervento parodontale, la resistenza alla trazione dell’interfaccia radice-gengivale aumenta da 200 g al 3° giorno, 340 g al 7° giorno successivo all’intervento fino al 1700 g dopo 14 giorni.11
Ciò suggerisce che la ferita parodontale potrebbe non raggiungere l’integrità funzionale fino a 2 settimane dopo l’intervento. Perciò, è ragionevole supporre che un graduale aumento delle forze applicate sulla ferita possano compromettere la formazione di un nuovo attacco connettivale che porta a una guarigione inappropriata con la formazione di un attacco epiteliale.
La letteratura non indica chiaramente se l’uso di alcuni dispositivi, come ad esempio l’impacco parodontale, possano dare vantaggi reali nella guarigione.
L’uso di una pasta derivata dall’eugenolo per proteggere le aree della ferita è stato introdotto per la prima volta nel 1923 da Ward.12 Nonostante il fatto che alcuni autori hanno sottolineato i vantaggi derivanti dall’utilizzo di un impacco dopo il trattamento, gli studi recenti spesso non ne consigliano l’impiego dopo la terapia parodontale.13
Al giorno d’oggi, le indicazioni del suo utilizzo sono limitate. Ad esempio, è suggerito nel riposizionamento di un lembo chirurgico per evitare che il lembo si possa spostare,14 mentre, a parte Sigush et al., nessun altro autore lo consiglia dopo la terapia parodontale non chirurgica.13
In passato, altri autori hanno discusso gli effetti positivi dell’utilizzo dell’impacco parodontale. Asboe-Jorgensen ha suggerito il suo utilizzo in particolare per migliorare il comfort del paziente.15 D’altra parte Ramfjord et al. affermano che il curettage a cielo chiuso potrebbe provocare un trauma parodontale che conduce a una deiscenza relativamente ampia delle papille interprossimali. Pertanto, il tessuto gengivale dovrebbe essere portato a stretto contatto con il dente dopo il trattamento mediante suture interprossimali o con il posizionamento dell’impacco parodontale.16,17
Inoltre, Pritchard et al. (1972) e Sachs et al. (1984) hanno osservato i vantaggi dell’utilizzo dell’impacco parodontale in termini di prevenzione di un persistente sanguinamento e di protezione dal trauma meccanico durante la guarigione.18,19
Infine, Plagmann ha osservato un effetto importante dell’uso dell’impacco. Per prevenire il distaccamento del coagulo, ha sostenuto l’idea che questo possa essere stabilizzato attraverso l’impiego dell’impacco parodontale in modo da facilitare la formazione di tessuto connettivo più stabile.17
L’ipotesi alla base di questo studio è che l’applicazione di un impacco parodontale dopo la procedura di SRP in pazienti affetti da parodontite da moderata a grave possa stabilizzare il coagulo, proteggendolo dalle forze esercitate durante il parlare e la masticazione, in modo che possa avvenire la formazione di un nuovo attacco connettivo, e i valori di profondità di tasca (PD) e livello di attacco parodontale (PAL) possano essere incrementati.
Materiali e metodi
Questa ricerca consiste in uno studio split mouth che coinvolge trenta (30) pazienti con diagnosi di parodontite da moderata ad avanzata con un età compresa tra i 35 ei 70 anni (52,3 ± 6,0 anni medi di età).
Tutti i pazienti sono stati selezionati tra i soggetti con parodontite del reparto di Odontoiatria, Ospedale della Versilia (Italia).
Il consenso informato è stato ottenuto da tutti i partecipanti. Tutti i soggetti soddisfano i criteri diagnostici per la parodontite secondo la nuova nomenclatura.21 I criteri di inclusione comprendevano pazienti non fumatori o fumatori al di sotto di 10 sigarette al giorno, presenza del 30% dei siti almeno con PD superiore a 5 mm e sanguinamento al sondaggio. Diversamente, tutti i pazienti che hanno ricevuto una terapia antibiotica durante i 6 mesi precedenti ed i pazienti con protesi implantari sono stati esclusi.
Sono stati raccolti di tutti i parametri parodontali, come PD, PAL, indice di sanguinamento al sondaggio (BdP), indice di placca (PI), e sono stati misurati da un odontoiatra utilizzando una sonda parodontale Michigan (Patterson Dental Minnesota, USA)
Tutte le valutazioni sono state effettuate su sei siti per dente, mesio-vestiobolare, vestibolare e disto-vestibolare, mesio-linguale/palatale, sito linguale/palatale, disto-linguale/palatale, mantenendo la sonda vicino alla superficie della radice e in linea con l’asse longitudinale del dente. L’operatore è stato istruito ad applicare una forza di 30 gr. Sono state scattate foto in modo non standardizzato.
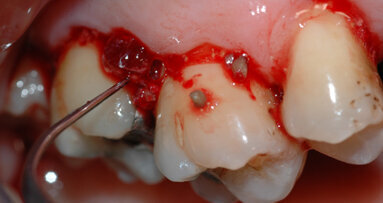
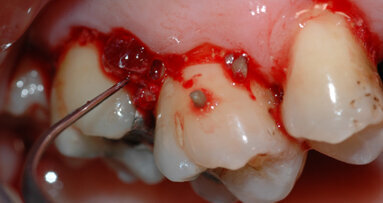
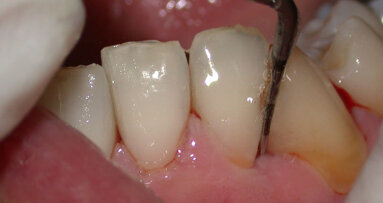
La prima fase della terapia consisteva in una seduta di igiene orale dopo il rilevamento dei parametri parodontali (Fig. 1). Inoltre, un igienista dentale ha istruito il paziente secondo la tecnica di Bass a svolgere le quotidiane manovre di igiene orale domiciliare.
Dopo una settimana è stata effettuata la seconda fase del trattamento. Il gruppo di pazienti è stato sottoposto a terapia parodontale costituita da SRP completo in 24 ore seguita da un curettage dell’epitelio gengivale interno per ciascuna tasca. Il curettage consente al coagulo di occupare lo spazio all’interno della tasca parodontale in modo che il processo di guarigione venga stimolato immediatamente dopo l’intervento.
Al termine del trattamento, per ciascun paziente sono stati selezionati un lato test e un lato controllo in modo casuale. Ė stato utilizzato un software specifico per ottenere una lista di randomizzazione (Random Allocation Software version 1.0, reperibile qui: http://mahmoodsaghaei.tripod.com/Softwares/randalloc.html).
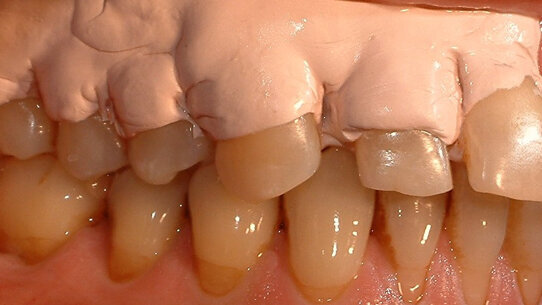
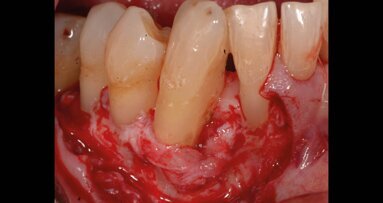
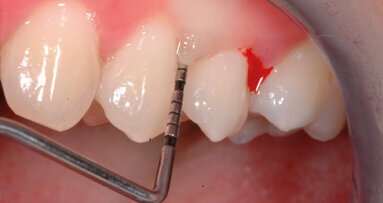
Successivamente, è stato applicato accuratamente l’impacco parodontale, come Coepak®, nell’arcata superiore ed inferiore del solo lato test (Figg. 2-3). Ogni volta è stata impiegata la massima cura nell’evitare che eccessi di saliva arrivassero alle zone trattate.
Vale la pena ricordare che Coepak® è un materiale privo di eugenolo per impacchi parodontali e aderisce in modo ottimo alle superfici dei denti.
L’assistente alla poltrona ha miscelato il materiale secondo le indicazioni del produttore. Il prodotto va applicato a partire dall’area della corona dentale. Al fine di adattare l’impacco alle papille l’igienista dentale ha applicato una leggera pressione nella zona dello spazio interdentale.
Ogni paziente è stato istruito a mantenere un buon livello di igiene orale, evitando però l’area dove l’impacco parodontale è stato posizionato.
Dopo una settimana l’impacco è stato rimosso dalla zona test dallo stesso igienista dentale, e i pazienti sono stati incoraggiati a mantenere un buon livello di igiene orale domiciliare. L’assegnazione del quadrante al gruppo test o controllo sono stati annotati in un apposito modulo da parte dell’igienista dentale, in modo che l’odontoiatra ignorasse dove era stato posto l’impacco parodontale.
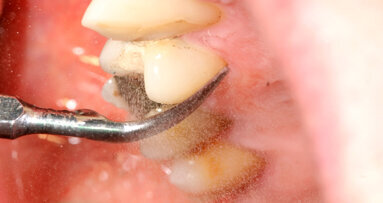
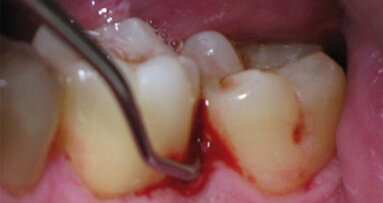
Tutti i parametri clinici sono stati rilevati dallo stesso odontoiatra dopo 2 mesi, valutando attentamente il grado di igiene orale (Fig. 4).
Per l’analisi statistica sono stati calcolati il valore medio, la deviazione standard e media della profondità di sondaggio, della recessione e del guadagno di attacco clinico. Per confrontare statisticamente i risultati del gruppo test e del gruppo controllo è stato usato il test di Fisher.
Risultati
La prima fase della terapia includeva la motivazione e la completa rimozione del tartaro e della placca sopragengivale. Questo era un prerequisito essenziale per avviare la seconda fase del trattamento, costituito dallo SRP. Il Full mouth plaque score (FMPS) è stato rilevato dopo 2 mesi in ciascun paziente. I risultati hanno mostrato una grande riduzione a confronto con i valori pre-trattamento.
Senza dubbio ciò è dovuto al regime efficace di igiene orale domiciliare e il breve periodo di tempo tra la prima fase e la rivalutazione finale (Tab. 1).
Allo stesso modo, Full mouth bleeding score (FMBS) è stato ridotto dopo il trattamento parodontale. In effetti i risultati osservati dopo 2 mesi, confermano il successo del trattamento (Tab. 2).
Rispetto ai dati di riferimento dopo 2 mesi sono stati registrate modifiche dei valori di PD e PAL. Notevoli miglioramenti sono stati osservati sia nel lato test che nel lato controllo indicando che la terapia è stata condotta con successo. Infatti sul lato controllo, la differenza tra i valori PD al baseline e dopo la terapia è 1,6 ± 0,6 millimetri dimostrando che le procedure di SRP hanno raggiunto l’obiettivo. D’altro canto, il lato test ha mostrato una riduzione PD di 2,4 ± 0,6 millimetri in media confermando che il PD si è ridotto maggiormente in questa zona. La Tabella 3 mostra la differenza tra i valori pre-trattamento e post.
Analoghe considerazioni possono essere condotte per i valori PAL. Infatti il guadagno di attacco dopo il trattamento parodontale migliora su entrambi i lati. Tuttavia, risultati migliori sono stati ottenuti nel lato test piuttosto che in quello di controllo. Osservando le differenze dei valori di PAL vediamo che le misure sono 1,4 ± 0,4 sul lato controllo e 2,5 ± 0,4 mm sul lato test (Tab. 4).
Differenze tra i lati test e controllo sono risultati statisticamente significativi secondo il test di Fisher (P < 0,05).
embedImagecenter("Imagecenter_2_658",658,"small");
Discussione
La rigenerazione parodontale è definita come «la riproduzione o la ricostituzione della parte perduta o danneggiata in modo che la forma e la funzione delle strutture perdute vengano ripristinate. Di conseguenza, la rigenerazione parodontale comprende la rigenerazione dell’osso alveolare, del cemento, del legamento parodontale e gengivale».22
Sebbene i famosi esperimenti di Nyman e Karring abbiano chiarito i concetti che regolano la rigenerazione parodontale, suggerendo che solo le cellule del legamento parodontale hanno la capacità di rigenerare l’attacco, altri autori hanno indicato che vari fattori possono contribuire alla ri-formazione dell’attacco.23,24
Prima di tutto la condizione delle superfici radicolari è di fondamentale importanza. Difetti parodontali risultano da una graduale e variabile distruzione del parodonto, causati dalla colonizzazione batterica del cemento radicolare.24 Il debridement tradizionale della radice, tuttavia, elimina la maggior parte dei batteri e tossine, anche se molti studi hanno rivelato che placca e tartaro possono rimanere nei setti interradicolari, nelle lacune e nelle superficie concave.25
È probabile che questo fatto possa compromettere il normale processo di guarigione, contribuendo alla formazione di un epitelio giunzionale.
Inoltre, alcuni tipi di superfici radicolari sembrano essere sfavorevoli per l’assorbimento del plasma e la stabilizzazione del coagulo come descritto in Polimeni et al.26 Anche Polso e Proye hanno dimostrato che i denti reimpiantati dopo il solo root planning hanno comportamenti diversi messi a confronto con denti ri-posizionati, dopo il root planning e la demineralizzazione delle superfici. Infatti la superficie delle radici demineralizzata favorisce la maturazione della fibrina in un attacco connettivale. Questa è conseguenza di un ancoraggio più stabile del coagulo su questo tipo di superficie.27
Inoltre, sembra che la presenza di materiale antigenico residuo sulla superficie radicolare potrebbe aumentare il numero di cellule neutrofile in fase iniziale di guarigione e, come conseguenza, un rilascio maggiore di enzimi proteolitici, che a loro volta, potrebbero ritardare la maturazione del coagulo.26
In ogni caso, l’esatta influenza della superficie radicolare non è ancora chiara. È stato dimostrato che le superfici radicolari coagulate con eparina mostrano una maggior formazione di attacco epiteliale rispetto ai siti di controllo condizionati con soluzione salina e l’epitelio si arresta in corrispondenza o immediatamente apicalmente alla giunzione amelo-cementizia.24 D’altra parte, è stata osservata la formazione di un nuovo attacco quando la superficie è stata demineralizzata utilizzando acido citrico o tetracicline.31
In secondo luogo, l’adattamento del lembo rappresenta un fattore di fondamentale importanza. Il fragile coagulo di fibrina è cruciale per la riparazione connettivale, come mostrato in modelli sperimentali in cui l’assenza di un ancoraggio stabile della fibrina porta ad una rapida epitelizzazione del difetto.27 Come menzionato sopra, gli esperimenti su animali indicano che la forza necessaria a staccare il lembo deve essere intorno a 200 gr dopo 3 giorni, aumentando a 340 gr dopo 7 giorni.29 Di conseguenza, queste forze potrebbero facilmente compromettere la stabilità del coagulo.
Il terzo fattore in questione è la morfologia del difetto. In linea di principio, la natura dei difetti è intimamente legata alla quantità e posizione della gengiva residua, alla morfologia dell’osso alveolare residuo e del legamento parodontale, nonché alla particolare anatomia del dente o denti coinvolti. Elementi dentali che presentano una larghezza ridotta di tessuto gengivale cheratinizzato sono state considerate più sensibili alla progressione della malattia parodontale.30 D’altra parte, la riduzione della gengiva aderente non è comunemente considerata critica per l’esito della terapia.31,32 Inoltre, la posizione dei singoli denti nel processo alveolare può predisporre a difetti sopraossei, intraossei o recessioni.33 Caratteristiche radicolari variabili, come forcazioni doppie o triple sembrano particolarmente suscettibili alla progressione della malattia.34
La morfologia del difetto svolge un ruolo chiave anche nella previsione della guarigione. Ciò è dovuto in primo luogo alla quantità di risorse rigenerative: per esempio, la disponibilità delle risorse rigenerativi è drasticamente diminuita nei difetti intraossei a una o due pareti.
In secondo luogo, le pareti del difetto sono in grado di proteggere il coagulo dalle forze meccaniche, e, di conseguenza, la stabilità del coagulo aumenta.
Inoltre, va notato che per eventuali difetti parodontali, la quantità e le caratteristiche della gengiva residua sono fondamentali per il raggiungimento di un adattamento passivo del lembo passivo e per la chiusura di una ferita primaria.35
Nel complesso, questi studi sottolineano l’importanza cruciale dell’adesione e della maturazione di un coagulo stabile di fibrina per la formazione di un attacco del tessuto connettivo rispetto all’epitelio giunzionale e successivamente dell’assorbimento del coagulo stesso.
I nostri risultati indicano chiaramente che il mantenimento di un impacco parodontale per sette giorni, contribuisce a migliorare i parametri parodontali dopo la procedura di SRP.
Sulla base dello studio di Sigush et al., dove venivano osservati risultati meno soddisfacenti nel gruppo di pazienti in cui l’impacco veniva rimosso dopo soli 3 giorni, abbiamo deciso di mantenere CoePak® per 7 giorni in tutto pazienti.36
Per quanto riguarda il guadagno di attacco, i nostri dati rivelano una differenza importante tra il lato test e controllo. Sul lato test abbiamo ottenuto un guadagno di 2,5 mm in media contro 1,4 mm sul lato controllo. La letteratura indica che dopo terapia con SRP, una valutazione dopo pochi mesi dimostra un guadagno di attacco fino a 0,55 millimetri per 4-6 tasche mm e 1,19 mm in caso di tasche > di 7 mm.37 Considerando che i nostri pazienti avevano più del 30% delle tasche > di 5 mm, i risultati sul lato controllo possono essere considerati più che soddisfacenti. D’altro canto, il lato test ha dimostrato un guadagno maggiore, supportando l’idea che la collocazione di un impacco parodontale con una leggera pressione in modo da adattarlo alla spazio interdentale, permetta l’adesione del tessuto molle sulla superficie radicolare e ai tessuti duri consentendone la stabilità.
Linghorne e O’Connell hanno osservato, già diversi anni fa, che la mancanza di stabilità della ferita potrebbe condurre alla formazione di un epitelio giunzionale lungo.38 Wikesjo et al. hanno anche confermato che la formazione di un attacco connettivale sulla superficie della radice dopo la chirurgia ricostruttiva parodontale è criticamente dipendente dalla stabilità della coagulazione.39
Hiatt et al. hanno evidenziato un ruolo fondamentale dell’adesione e della stabilità del coagulo di fibrina alla superficie radicolare in modo da impedire la migrazione apicale dell’epitelio gengivale.11
Su questa base, la formazione di epitelio giunzionale, comunemente osservata dopo il trattamento parodontale, sembra essere un fallimento della guarigione.20,40
Oltre alla stabilità, l’impacco parodontale potrebbe offrire anche altri vantaggi, quali una mancanza della penetrazione dei fluidi e dei batteri nella zona trattata. In realtà, è opportuno ricordare che, dopo la procedura di SRP o un intervento chirurgico la tasca parodontale viene esposta direttamente all’ambiente orale. Di conseguenza, i batteri potrebbero ricolonizzare in blocco le stesse tasche parodontali, e le superfici radicolari mettendo a rischio la guarigione.41
I nostri risultati mostrano anche una notevole riduzione dei valori della profondità di sondaggio (PD) dopo il trattamento sia sul lato test che di controllo. La riduzione dei valori di PD dopo la strumentazione meccanica sono il risultato della combinazione di guadagno di attacco e la formazione di recessione gengivale.42
La riduzione del PD sul lato test è di 2,4 mm contro 1,6 mm del lato di controllo. La letteratura indica che per le tasche che inizialmente misuravano 4-6 mm, la riduzione media di PD è di 1,29 mm mentre per le tasche superiori a 7 mm, la riduzione è di 2,16 mm.37 I valori sul lato controllo sembrano essere in accordo con la letteratura mentre il lato test mostra una maggiore riduzione.
Secondo Sigush et al. l’applicazione dell’impacco potrebbe aver ridotto l’entità della risposta infiammatoria nella area parodontale.36 Questo conferma che la riduzione dei valori PD sul lato test è dovuta sia a un guadagno reale di attacco (come discusso sopra) che a una riduzione dell’edema gengivale.
Con i limiti del nostro studio, riteniamo che i nostri risultati forniscano nuove indicazioni sull’uso dell’impacco parodontale. Infatti, come abbiamo dimostrato, l’impacco parodontale può migliorare l’esito del trattamento parodontale non chirurgico probabilmente attraverso la stabilizzazione del coagulo in modo che la guarigione ideale possa essere raggiunta.
Tuttavia sono necessari ulteriori studi per confermare i nostri risultati, e per chiarire quali sono esattamente i meccanismi coinvolti nella guarigione delle ferite dopo SRP e se l’impacco parodontale può davvero migliorare la guarigione da un punto di vista istologico.
Bibliografia
1. Loe H., Theilade E., Jensen Sb. Experimental Gingivitis In Man.J Periodontol. 1965 May-Jun;36:177-87.
2. Socransky SS., Haffajee AD. The bacterial etiology of destructive periodontal disease: current concepts. J Periodontol. 1992 Apr;63(4 Suppl):322-31
3. Socransky SS., Haffajee AD., Smith C., Duff GW. Microbiological parameters associated with IL-1 gene polymorphisms in periodontitis patients.J Clin Periodontol. 2000 Nov;27(11):810-8.
4. Yukna RA. A clinical and histologic study of healing following the excisional new attachment procedure in rhesus monkeys. J Periodontol. 1976 Dec;47(12):701-9.
5. Clark RAF. Wound repair. Overview and general considerations. In: Clark RAF, editor The molecular and cellular Biology of wound reapir, 2nd edn. New York, NY Plenum Press, 1996:3-50
6. Martin P. Wound healing – aiming for perfect skin regeneration. Science 1997: 276:75-81
7. Grzesik WJ., Narayanan AS. Cementum and periodontal wound healing and regeneration.Crit Rev Oral Biol Med. 2002;13(6):474-84. Review.
8. Wikesjö UM., Selvig KA., Zimmerman G., Nilvéus R. Periodontal repair in dogs: healing in experimentally created chronic periodontal defects.J Periodontol. 1991 Apr;62(4):258-63.
9. Ririe CM., Crigger M., Selvig KA. Healing of periodontal connective tissues following surgical wounding and application of citric acid in dogs. J Periodontal Res. 1980 May;15(3):314-27.
10. Selvig KA., Biagiotti GR., Leknes KN., Wikesjo UME. Periodontal reapir in dogs: space provision by reinforced ePTFE membranes enhances bone and cementum regeneration in large supra alveolar defects. J Periodontol 1994:65:350-356.
11. Hiatt WH., Stallard RE., Butler ED., Badgett B. Repair following mucoperiosteal flap surgery with full gingival retention. J Periodontol. 1968 Jan;39(1):11-6.
12. Ward, AW. (1923) Inharmonious cusp relation as a factor in periodontoclasia. The Journal of the American Dental Association 10, 471.
13. Sigusch BW., Pfitzner A., Nietzsch T., Glockmann E. Periodontal dressing (Vocopac) influences outcomes in a two-step treatment procedure. J Clin Periodontol. 2005 Apr;32(4):401-5.
14. Araiudo AA Tyrell HA Repositioning and increasing the zone of attached gingival. J periodontology 1957;28 (2):106-10.
15. Asboe Jorgensen V., Attstrom R., Lang N.P. & Loe H. (1974) Effect of a chlorhexidine dressing on the healing after periodontal surgery. The Journal of Periodontology 45, 13.
16. Ramfjord, SP. (1980) Root planing and curettage. International Dental Journal 30,93–100.
17. Plagmann, HC. (1998) Lehrbuch der Parodontologie, pp. 452–453. Mu¨nchen: Hanser.
18. Pritchard, JF. (1972) Advanced Periodontal Disease, 2nd edition, pp. 348. Philadelphia: W.B. Saunders Co.
19. Sachs, HA., Farnoush, A., Checchi, L. & Joseph, CE. (1984) Current status of periodontal dressings. The Journal of Periodontology 55, 689–696.
20. Wikesjo¨, UM., Nilve´us, RE. & Selvig, KA. (1992) Significance of early healing events on periodontal repair: a review. The Journal of Periodontology 63, 158-165.
21. Armitage GC Development of a classification system for periodontal diseases and conditions.Ann Periodontol. 1999 Dec;4(1):1-6. Review
22. American academy of periodontology, Glossary of periodontal terms. 3rd edn Chicago, IL: American academy of periodontology 1992.
23. Nyman S., Gottlow L., Karring T., Lindhe J. The regenerative potential of the periodontal ligament. 1 Clin Periodontol 1982: 9: 257-265.
24. Wikesjo UME., Claffey N., Egelberg J. Periodontal repair in dogs: Effect of heparin treatment of the root surface. J Clin Periodontol 1991: 18: 60-64.
25. Crespi R., Barone A., Covani U. Histologic evaluation of three methods of periodontal root surface treatment in humans. J Periodontol. 2005 Mar;76(3):476-81.
26. Polimeni G., Albandar JM., Wikesjo UME. Porgnostic factors for alveolar re generation: effect of space provision. J clin Periodontol 2005:32:951-954
27. Polson AM., Proye MF. Fibrin linkage: a precursor for new attachment. J Periodontol 1983: 54: 141-147.
28. Wikesjo UME., Claffey N., Christersson LA., Franzetti LC., Genco RJ., Terranova FL., Egelberg J. Repair of periodontal furcation defects in beagle dogs following reconstructive surgery including root surface demineralization with te- tracycline hydrochloride and topical fibronectin appli- cation. J Clin Periodontol 1988: 15: 73-80.
29. Hiatt WH. Free gingival graft or frenectomy? J Colo Dent Assoc. 1968 Mar;46(2):7-9.
30. Lang NP., Loe H. The relationship between the width of keratinized gingiva and gingival health. J Periodontol 1972:43:623-627
31. Kennedy JE., Bird WC., Palcanis KG., Dorfman HS. A longitudinal evaluation of varying widths of attached gingiva. J Clin Periodontol 1985: 12: 667475.
32. Tackas VJ. Root coverage techniques: a review. J West SOC Periodont Periodont Abstr 1995: 43: 5-14
33. Nielsen IM., Glavind L., Karring T. Interproximal periodontal intrabony defects. Prevalence, localization and etiological factors. J Clin Periodontol 1980: 7: 187-198
34. Leknes KN., Lie T., Selvig KA. Root grooves: a risk factor in periodontal attachment loss. J Periodontol 1994: 65: 859- 863.
35. Wikesjö UM, Selvig KA Periodontal wound healing and regeneration. Periodontol 2000. 1999 Feb;19:21-39.
36. Sigusch BW., Pfitzner A., Nietzsch T., Glockmann E. Periodontal dressing (Vocopac) influences outcomes in a two-step treatment procedure. J Clin Periodontol 2005; 32: 401–405.
37. Cobb CM. Clinical significance of non-surgical periodontal therapy: an evidence-based perspective of scaling and root planing. J Clin Periodontol. 2002 May;29 Suppl 2:6-16.
38. Linghorne WJ., O’Connell DC. Studies in the regeneration and reattachment of supporting structures of teeth. I. Soft tissue reattachment. J Dent Res 1950: 29: 419-428.
39. Wikesjo UME., Nilveus R. Periodontal repair in dogs: Effect of wound stabilization on healing. J Periodontol 1990: 61:719-724
40. Wikesjo UME., Hanisch 0, Sigurdsson TJ, Caplanis N. Application of rhBMP-2 to alveolar (peri-implant) and periodontal defects. In: Lynch SE, Genco RG, ed. Tissue engineering: applications in periodontics and oral surgery. Chicago, I L Quintessence
41. Farman M., Joshi RI. Full-mouth treatment versus quadrant root surface debridement in the treatment of chronic periodontitis: a systematic review. Br Dent J. 2008 Nov 8;205(9):E18; discussion 496-7. Epub 2008 Oct 3.
42. Proye M., Caton J., Polson A. Initial healing of periodontal pockets after a single episode of root planing monitored by controlled probing forces. J Periodontol. 1982 May;53(5):296-301.
L'articolo è stato pubblicato sul numero 1 di Perio Tribune Italy 2013
Dopo la prima visita si propone al paziente un protocollo di trattamento. Come lo schema illustra (Fig. 1), previa diagnosi, se si decide di passare subito ...
Dopo la prima visita si propone al paziente un protocollo di trattamento. Come lo schema illustra (Fig. 1), previa diagnosi, se si decide di passare subito ...
La strumentazione parodontale non chirurgica è necessaria come trattamento iniziale, e come terapia di mantenimento, di qualsiasi patologia ...
Barcellona. Ricercatori spagnoli hanno trovato un’ulteriore prova della connessione fra parodontite e diabete di Tipo 2. In un recente studio hanno ...
Sono un’igienista dentale e lavoro nell’ambito della prevenzione orale fin dagli anni ‘80. Mi occupo anche di formazione e organizzo corsi rivolti ai ...
Come migliorare i fattori predittivi per gestire in maniera corretta i tessuti parodontali coinvolti nelle chirurgie odontostomatologiche.
Le malattie parodontali possono causare gravi invalidità quali la perdita o la riduzione della funzionalità dell’apparato ...
La parodontite è la prima causa di perdita di denti nella popolazione adulta nei Paesi industrializzati e presenta molteplici ripercussioni sulle ...
AARHUS, Danimarca – Il fumo può influenzare notevolmente il trattamento della parodontite: questi sono i risultati di un recente studio che ha esaminato ...
I più recenti dati epidemiologici confermano la parodontite come una delle principali patologie croniche del cavo orale, con una prevalenza stimata di ...
Live webinar
mer. 3 giugno 2026
19:00 (CET) Rome
Live webinar
gio. 4 giugno 2026
20:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
18:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
19:00 (CET) Rome
Dr. Anthony Mak B.D.S, Prof. Marleen Peumans
Live webinar
lun. 8 giugno 2026
20:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
17:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
20:00 (CET) Rome
Nacho Fernández-Baca DDS, MSc



 Austria / Österreich
Austria / Österreich
 Bosnia ed Erzegovina / Босна и Херцеговина
Bosnia ed Erzegovina / Босна и Херцеговина
 Bulgaria / България
Bulgaria / България
 Croazia / Hrvatska
Croazia / Hrvatska
 Repubblica Ceca e Slovacchia / Česká republika & Slovensko
Repubblica Ceca e Slovacchia / Česká republika & Slovensko
 Francia / France
Francia / France
 Germania / Deutschland
Germania / Deutschland
 Grecia / ΕΛΛΑΔΑ
Grecia / ΕΛΛΑΔΑ
 Ungheria / Hungary
Ungheria / Hungary
 Italia / Italia
Italia / Italia
 Paesi Bassi / Nederland
Paesi Bassi / Nederland
 nordisch / Nordic
nordisch / Nordic
 Polonia / Polska
Polonia / Polska
 Portogallo / Portugal
Portogallo / Portugal
 Romania e Moldavia / România & Moldova
Romania e Moldavia / România & Moldova
 Slovenia / Slovenija
Slovenia / Slovenija
 Serbia e Montenegro / Србија и Црна Гора
Serbia e Montenegro / Србија и Црна Гора
 Spagna / España
Spagna / España
 Svizzera / Schweiz
Svizzera / Schweiz
 Turchia / Türkiye
Turchia / Türkiye
 Gran Bretagna e Irlanda / UK & Ireland
Gran Bretagna e Irlanda / UK & Ireland
 Internazionale / International
Internazionale / International
 Brasile / Brasil
Brasile / Brasil
 Canada / Canada
Canada / Canada
 America Latina / Latinoamérica
America Latina / Latinoamérica
 USA / USA
USA / USA
 Cina / 中国
Cina / 中国
 India / भारत गणराज्य
India / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
 Medio Oriente / Middle East
Medio Oriente / Middle East

















































To post a reply please login or register