Le malattie parodontali possono causare gravi invalidità quali la perdita o la riduzione della funzionalità dell’apparato stomatognatico, la compromissione della fonazione e dell’estetica del sorriso, gravando sul benessere psicofisico di chi ne è colpito. La parodontite è la prima causa di perdita degli elementi dentari nella popolazione adulta dei Paesi industrializzati (SIdP, Progetto Perio-Medicine).
Il fattore eziologico della parodontite è rappresentato da alcuni gruppi di batteri specifici, causa di un’intensa risposta infiammatoria locale1.
Si ritiene che l’acquisizione di questi microrganismi avvenga tramite trasmissione orizzontale tra genitori (principalmente la madre) e figli e all’interno della coppia2. Come in molte forme di infezioni, il fattore eziologico batterico non è sufficiente per lo sviluppo della malattia, altresì in assenza di batteri la parodontite non si manifesta3. La presenza di fattori di rischio concorrenti genetici predispone il soggetto a manifestare forme di parodontiti con perdita severa di tessuto di supporto.
Vari studi hanno suggerito che i polimorfismi nei geni del cluster IL1 e TNFa potrebbero predisporre i soggetti a elevati livelli di IL1 e TNFa; tali mediatori immunologici hanno come proprietà la stimolazione del riassorbimento osseo.
La presenza di gravi forme di malattia parodontale non trattata può provocare infezioni sistemiche in seguito alla diffusione nel circolo ematico di microrganismi parodontali4, con la comparsa di infezioni cardiache; inoltre, i soggetti affetti da infezioni parodontali possono presentare, rispetto ai soggetti sani, elevati livelli di granulociti neutrofili e di proteina C reattiva.
La malattia parodontale è una patologia complessa in cui sono coinvolti sistemi di difesa innati e adattattivi.
Il principio secondo il quale le cellule epiteliali e endoteliali siano cellule strutturali non coinvolte in reazioni immunitarie è stato smentito; infatti, i recettori TOLL LIKE RECEPTOR (TLR), strutture che individuano sollecitazioni batteriche, sono presenti su tutte le cellule umane, incluse quelle epiteliali ed endoteliali. I TLR riconoscono gli LPS batterici e le strutture accessorie come il flagello batterico attraverso il mamp (microbe-associated molecular pattern), considerato come un “codice a barre” che, attraverso i TLR, attiva determinate cellule della difesa, attuando così una difesa più personalizzata. Grazie a questo sistema i batteri commensali vengono tollerati anche se in possesso di flagelli.
Gli obiettivi della terapia parodontale sono l’eliminazione dell’infezione, la correzione delle sequele anatomiche e il mantenimento della salute parodontale nel lungo periodo.
Il controllo dell’infezione avviene mediante la terapia non chirurgica. Le modalità di approccio terapeutico possono essere:
1. strumentazione convenzionale a quadranti;
2. strumentazione eseguita in 24 ore di entrambe le arcate con l’utilizzo di antisettici locali, ovvero con la One-Stage Full-Mouth Disinfection (OSFMD) oppure senza l’ausilio di antisettici locali, ovvero con la Full-Mouth Scaling and Root Planing (FMSRP).
Entrambi gli approcci possono essere associati al trattamento laser assistito. L’ausilio del laser permette di avvalersi di un’azione battericida eliminando anche i batteri, che con la loro capacità invasiva colonizzano l’epitelio interno della tasca. In fase finale di strumentazione si può eseguire la biostimolazione laser assistita dei tessuti dell’area trattata5.
Il protocollo della OSFMD proposto da Quirynen nel 1995 trova il suo razionale nel drastico abbattimento della carica microbica in tutto l’ambiente orale da eseguirsi in 24 ore; questo permette di ridurre il rischio di cross-contamination o di intra-oral traslocation, intendendo per entrambi il meccanismo di ricolonizzazione dei siti trattati da parte di batteri provenienti dai siti non ancora trattati. Mediante l’approccio OSFMD si verifica un miglioramento statisticamente significativo della riduzione/eliminazione dei microrganismi parodontopatogeni, sia sottogengiva sia nelle nicchie ecologiche6.
Le nicchie ecologiche – come le membrane mucose, le cripte tonsillari, la saliva, il tartaro – risultano essere reservoirs di microrganismi.
La riduzione dei microrganismi patogeni può variare, dopo 1 mese dal trattamento, da una completa eradicazione (100%) di Eikenella corrodens, al 92,8% del Porphyromonas gingivalis, e all’80% del Fusobacterium nucleatum7. Dati di letteratura dimostrano come mediante l’applicazione del protocollo OSFMD si ottengano miglioramenti dei parametri clinici e microbiologici nell’arco dei successivi 8 mesi, sia nei casi di parodontite cronica sia nei casi di parodontite a insorgenza precoce8.
La parodontite aggressiva (AgP) è caratterizzata dalla presenza di flora batterica virulenta unitamente a una suscettibilità individuale alla malattia parodontale di alto livello.
Gli aspetti principali che contraddistinguono le AgP sono: anamnesi medica del paziente priva di rilevanza, ovvero assenza di patologie sistemiche che possono influire sul corretto funzionamento delle difese dell’ospite, rapida perdita di attacco e distruzione ossea, presenza di aggregazione di casi in famiglia.
Gli aspetti secondari delle AgP, presenti non in tutti i casi, sono: depositi di biofilm batterico definiti irrilevanti rispetto alla gravità della distruzione parodontale; elevate percentuali di Aggregatibacter actinomycetemcomitans (A.a.)9; fenotipo dei macrofagi iperattivo con elevata sintesi di PGE2 e IL-1b in risposta alle endotossine microbiche; possibile arresto spontaneo della distruzione ossea e della perdita di attacco. Caratteristiche cliniche e di laboratorio determinano una sottoclassificazione della AgP in forme generalizzate (GAP) e localizzate (LAP).
L’A.a. è considerato il microrganismo di maggiore interesse nell’eziologia delle AgP, in quanto è stato isolato in più del 90% dei soggetti affetti da LAP; esso produce fattori di virulenza come la leucotossina che ha capacità citotossiche. Inoltre, A.a. è in grado di migrare attraverso le membrane epiteliali. Nei pazienti affetti da LAP sono stati riscontrati livelli di anticorpi sierici anti-A.a. significativamente elevati10. Il successo della terapia delle AgP è legato, quando possibile, a una diagnosi precoce, alla soppressione dei parodontopatogeni mediante terapia meccanica e farmacologica, al costante monitoraggio finalizzato alla prevenzione e intercettazione del break down e al mantenimento dell’alleanza terapeutica tra paziente e operatore.
Il paziente candidato a ricevere la OSFMD può essere il paziente affetto da parodontite di grado severo, con ampi depositi di placca e tartaro, oppure il paziente affetto da parodontite aggressiva generalizzata o localizzata11. Il timing della OSFMD trova la sua realizzazione nel rispetto dei seguenti step:
– periodontal debridement di entrambe le arcate in due sedute nelle 24 ore;
– irrigazione sottogengivale con chx gel 1% ripetuto 3 volte in 10’;
– detersione del dorso linguale con chx gel 1% per la durata di 1’;
– sciacqui alla poltrona e gargarismi o spray rivolto verso le tonsille con chx 0,2% della durata di 2’;
– istruzione di manovre corrette di igiene orale domiciliare + sciacqui domiciliari con chx 0,2% per la durata di 2 mesi11.
Nei casi di parodontite aggressiva, unitamente alla OSFMD si può associare la terapia farmacologica sistemica con la somministrazione di antibiotici secondo il “Winkelhoff-Cocktail”12:
– amoxicillina cps 1 gr: 1/2 cps ogni 8 ore per 7 gg
più
– metronidazolo cps 250 mg: 1 cps ogni 8 ore per 7 gg.
Per i soggetti allergici alla penicillina si somministra:
– ciprofloxacina cps 250 mg: 1 cps ogni 8 ore per 7 gg, mentre la somministrazione di metronidazolo rimane invariata.
Tale terapia farmacologica inizia il giorno stesso della prima seduta della OSFMD.
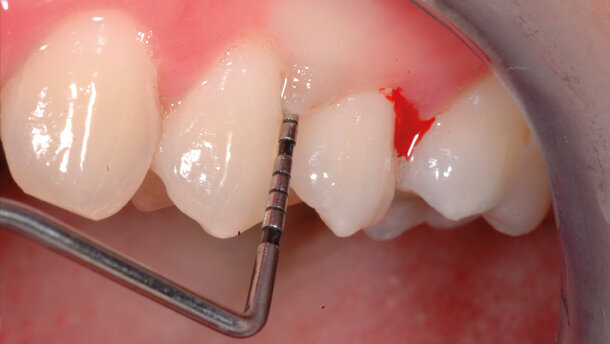
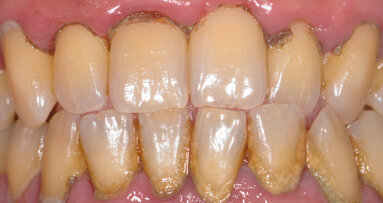
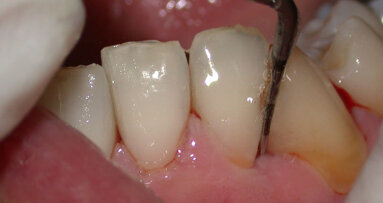
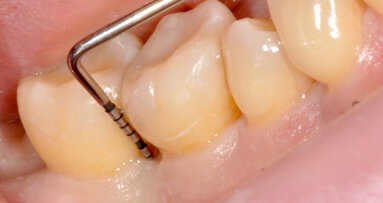
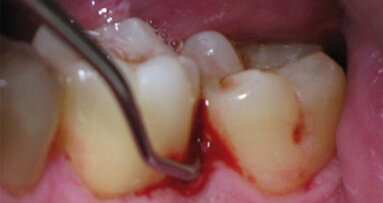
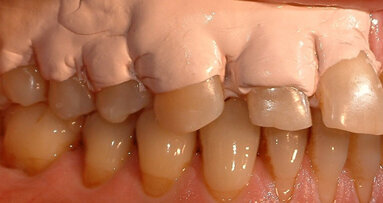
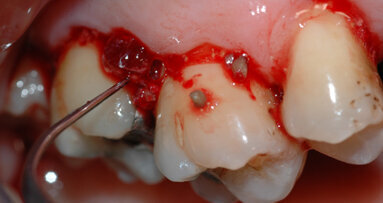
Caso clinico: descrizione e foto
Paziente di sesso femminile di anni 26. Anamnesi generale priva di patologie sistemiche, non fumatrice.
Il piano di trattamento scelto è stata la “terapia causale” secondo protocollo OSFMD con terapia farmacologica secondo protocollo van Winkelohff. È stato eseguito test microbiologico in occasione del primo appuntamento, prima di iniziare il trattamento meccanico. L’esito del test microbiologico ha mostrato positività all’Aggregatibacter actinomicetemcomitans.
In letteratura vi sono dati contrastanti a riguardo del reale vantaggio offerto dalla OSFMD. La clorexidina, non utilizzata nella FMSRP, risulta essere un importante ausilio nel controllo chimico del biofilm batterico8.
Inoltre, il drastico abbattimento in breve tempo della carica microbica risulta essere efficace nella riduzione dei livelli di proteina C reattiva e dei livelli di leucociti13.
La OSFMD può rappresentare per il clinico un valido approccio terapeutico anche qualora vi sia l’esigenza di svolgere la terapia parodontale non chirurgica previa profilassi antibiotica, consentendo una riduzione del numero di volte di assunzione del farmaco. Con la OSFMD l’operatore ha a disposizione un’idonea alternativa all’approccio convenzionale nel controllo dell’infezione parodontale.
embedImagecenter("Imagecenter_2_1424",1424,"small");
L'articolo è stato pubblicato sul numero 2 di Perio Tribune Italy 2014.
Gli obiettivi principali di ogni trattamento professionale sono l’arresto della malattia in corso e il mantenimento della salute orale e della sua ...
L’evoluzione nelle conoscenze sul microbiota e sulle problematiche orali ha cambiato radicalmente i piani di trattamento nelle varie tipologie di ...
La strumentazione parodontale non chirurgica è necessaria come trattamento iniziale, e come terapia di mantenimento, di qualsiasi patologia ...
Sono un’igienista dentale e lavoro nell’ambito della prevenzione orale fin dagli anni ‘80. Mi occupo anche di formazione e organizzo corsi rivolti ai ...
Paziente di sesso femminile, 30 anni, non fumatrice, con anamnesi sistemica silente, assenza di allergie a farmaci e sostanze alimentari, familiarità ...
La malattia parodontale è una patologia cronica che colpisce i tessuti di supporto dei denti ed è caratterizzata da infiammazione, sanguinamento gengivale...
La parodontite è la prima causa di perdita di denti nella popolazione adulta nei Paesi industrializzati e presenta molteplici ripercussioni sulle ...
I più recenti dati epidemiologici confermano la parodontite come una delle principali patologie croniche del cavo orale, con una prevalenza stimata di ...
Introduzione
La parodontite è una malattia infettiva caratterizzata dalla perdita di strutture di supporto del dente quali il tessuto connettivo e ...
Dopo la prima visita si propone al paziente un protocollo di trattamento. Come lo schema illustra (Fig. 1), previa diagnosi, se si decide di passare subito ...
Live webinar
mer. 3 giugno 2026
19:00 (CET) Rome
Live webinar
gio. 4 giugno 2026
20:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
18:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
19:00 (CET) Rome
Dr. Anthony Mak B.D.S, Prof. Marleen Peumans
Live webinar
lun. 8 giugno 2026
20:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
17:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
20:00 (CET) Rome
Nacho Fernández-Baca DDS, MSc



 Austria / Österreich
Austria / Österreich
 Bosnia ed Erzegovina / Босна и Херцеговина
Bosnia ed Erzegovina / Босна и Херцеговина
 Bulgaria / България
Bulgaria / България
 Croazia / Hrvatska
Croazia / Hrvatska
 Repubblica Ceca e Slovacchia / Česká republika & Slovensko
Repubblica Ceca e Slovacchia / Česká republika & Slovensko
 Francia / France
Francia / France
 Germania / Deutschland
Germania / Deutschland
 Grecia / ΕΛΛΑΔΑ
Grecia / ΕΛΛΑΔΑ
 Ungheria / Hungary
Ungheria / Hungary
 Italia / Italia
Italia / Italia
 Paesi Bassi / Nederland
Paesi Bassi / Nederland
 nordisch / Nordic
nordisch / Nordic
 Polonia / Polska
Polonia / Polska
 Portogallo / Portugal
Portogallo / Portugal
 Romania e Moldavia / România & Moldova
Romania e Moldavia / România & Moldova
 Slovenia / Slovenija
Slovenia / Slovenija
 Serbia e Montenegro / Србија и Црна Гора
Serbia e Montenegro / Србија и Црна Гора
 Spagna / España
Spagna / España
 Svizzera / Schweiz
Svizzera / Schweiz
 Turchia / Türkiye
Turchia / Türkiye
 Gran Bretagna e Irlanda / UK & Ireland
Gran Bretagna e Irlanda / UK & Ireland
 Internazionale / International
Internazionale / International
 Brasile / Brasil
Brasile / Brasil
 Canada / Canada
Canada / Canada
 America Latina / Latinoamérica
America Latina / Latinoamérica
 USA / USA
USA / USA
 Cina / 中国
Cina / 中国
 India / भारत गणराज्य
India / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
 Medio Oriente / Middle East
Medio Oriente / Middle East



















































To post a reply please login or register