L’aumento del tessuto osseo e gengivale intorno agli impianti dentali, come dimostrato nella bibliografia, svolge un ruolo importante nell’ottimizzazione dei siti di impianto atrofici: la generazione di un contorno cervicale armonioso insieme alla conservazione del tessuto cheratinizzato sembrano essere obbligatori per la stabilità a lungo termine e la protezione contro lo sviluppo di peri-implantite. Inoltre, quanto sopra può essere raggiunto quando viene fornito un adeguato supporto sottostante per il tessuto molle che imiti la natura, sia utilizzando innesti ossei e/o di tessuti molli per aumentare il sito e migliorare la gengiva cheratinizzata quando necessario.
Questo processo di aumento segue uno schema analitico di atti chirurgici successivi in cui ogni fase ha un ruolo specifico durante il trattamento implantare. Etichettate come innesto osseo, posizionamento dell’impianto o aumento del tessuto molle, tali procedure seguono il dogma del “un miracolo alla volta” che enfatizza la sicurezza come fattore ottimale per il successo. Tuttavia, è evidente che questa affermazione implica che sia il numero di atti chirurgici che l’intera durata del trattamento debbano essere aumentati. Aumenta anche il numero di rischi peri e post-operatori per il paziente, soprattutto quando combinati con il prelievo di tessuto osseo e molle autologo. La morbilità del sito donatore, il dolore e il sanguinamento post-operatorio e la necrosi dell’innesto sono solo alcune delle complicanze riportate con diverse incidenze. Tuttavia, il prelievo di blocchi ossei, l’uso di materiali non riassorbibili come le griglie di titanio, le barriere in PTFE o le viti di ancoraggio e gli innesti di tessuto gengivale connettivo o libero sono ancora considerati “gold standard” nelle procedure rigenerative combinate con il posizionamento degli impianti. La vera domanda oggi è se siano davvero obbligatori all’interno di un moderno flusso di lavoro chirurgico potenziato dalla protesi. E sarebbe possibile evitare un processo lungo, frammentato e invasivo e riunire tutti gli atti chirurgici in una procedura in un solo stadio?
Vari protocolli innovativi potrebbero fornire risposte alle domande precedenti, in quanto propongono un approccio più “sinergico” al trattamento degli impianti, riducendo il numero di fasi chirurgiche e quindi la durata complessiva della terapia. Un protocollo bifasico recentemente pubblicato riesce a ottenere l’ottimizzazione del tessuto duro e molle per siti atrofici che ricevono impianti adiacenti, in soli 4 mesi invece dei soliti 6-9. Un altro protocollo introduce una procedura di ottimizzazione in un solo passo con l’uso di innesti sintetici, ma si riferisce a siti non atrofici che necessitano di condizionamento del tessuto molle. Inoltre, diverse aziende di implantologia dentale e biomateriali hanno introdotto nuovi prodotti non riassorbibili o riassorbibili, che promettono di ridurre la durata del trattamento chirurgico (rigenerazione ossea - osteointegrazione dell’impianto - aumento del tessuto molle) a nuovi standard inferiori e al di sotto della soglia dei 6 mesi. Tuttavia, nonostante questi sforzi, tali prodotti sembrano fallire nel ridurre il numero di interventi chirurgici invasivi e il tasso di complicanze. Nel complesso, e a parte i loro benefici, gli approcci rigenerativi menzionati non riescono a eliminare la loro natura analitica del processo. Ciò potrebbe essere spiegato dal fatto che condividono una caratteristica comune: l’uso dell’impronta per la generazione del contorno cervicale (di solito un moncone personalizzato o provvisorio) alla fine del trattamento anziché all’inizio. Implementando il processo sopra descritto, vengono aggiunte ulteriori fasi per la manipolazione/aumento del tessuto molle a seguito della rigenerazione ossea e del posizionamento dell’impianto, rendendo l’intero trattamento più complesso.
Questo articolo presenta un nuovo protocollo per l’aumento del tessuto duro e molle con il posizionamento simultaneo di impianti in siti edentuli con atrofia alveolare, utilizzando una lamina corticale riassorbibile montata su un moncone personalizzato in una procedura singola.
Materiali e metodi
In questa pubblicazione presenteremo due casi, entrambi riferiti a siti edentuli di 46 con atrofia ossea. I criteri di inclusione per l’arruolamento dei 2 pazienti erano i seguenti:
- Pazienti che hanno firmato un consenso informato e accettato di seguire le istruzioni post-operatorie e il piano di follow-up;
- pazienti con una buona igiene orale e privi di malattie parodontali (indice di placca <25%, assenza di tasche durante il sondaggio, livelli di BoP <25%);
- pazienti con gengiva cheratinizzata di almeno 4 mm sui siti edentuli da trattare.
I criteri di esclusione erano:
- Pazienti affetti da patologie che influenzano il metabolismo osseo e la guarigione delle ferite;
- gravidanza e/o allattamento durante il trattamento e il periodo di guarigione;
- fumatori.
Caso 1
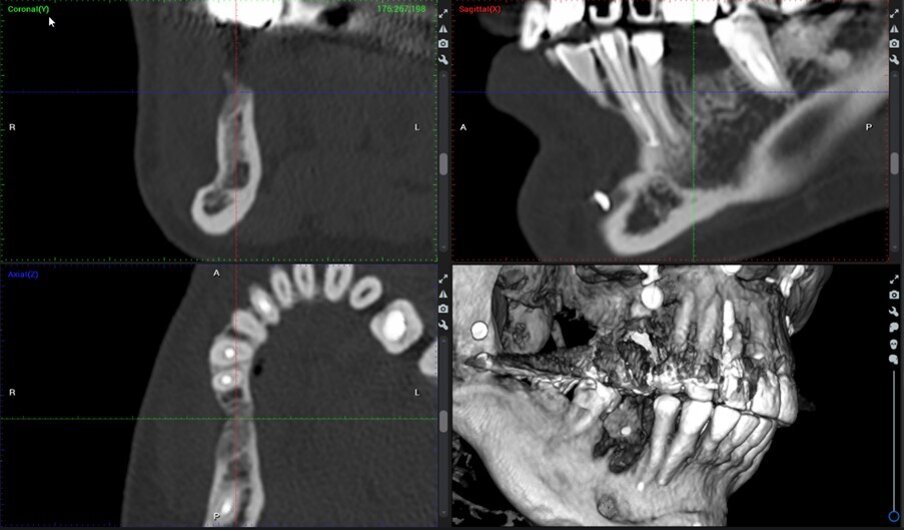
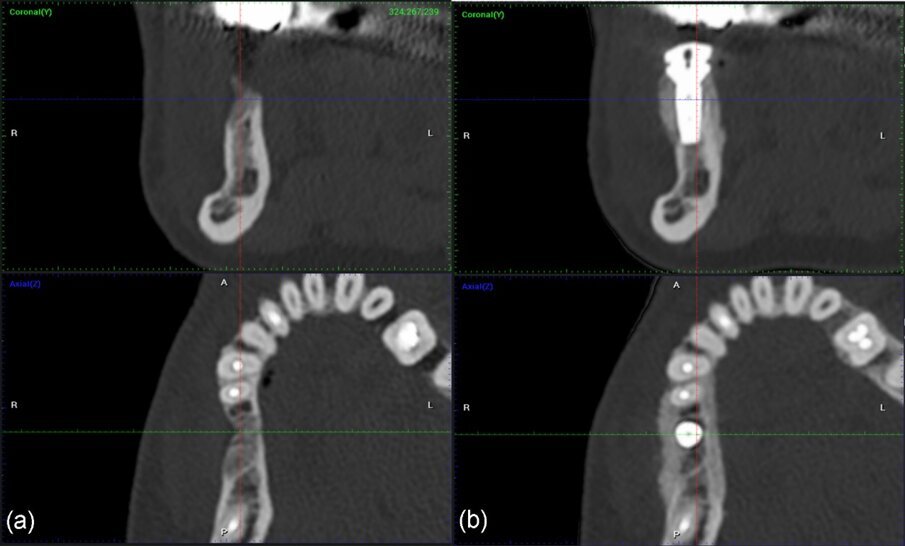
Una paziente di 51 anni di sesso femminile ha frequentato la nostra clinica cercando una riabilitazione in un sito edentulo inferiore 46. L’elemento dentale 46 è stato estratto più di 4 mesi prima della consulenza e non è stato utilizzato alcun materiale per la conservazione dell’alveolo. La paziente era una non fumatrice in buona salute, senza malattie parodontali (nessuna perdita di attacco, tasche al sondaggio e BoP). È stato eseguito un esame pre-operatorio con tomografia computerizzata a fascio conico (CBCT) nel quarto quadrante inferiore, che ha rivelato una significativa perdita ossea orizzontale nella zona edentula (Fig. 1). La densità ossea è stata classificata come tipo 2 e la distanza dal margine alveolare più coronale al canale alveolare inferiore era sufficiente per posizionare un impianto dentale (più di 10 mm) (Fig. 1). L’esame clinico ha rivelato una larghezza del tessuto cheratinizzato di più di 4 mm sulla cresta comunque sottile (Fig. 2). Il paziente è stato trattato con la tecnica del Poncho Lamina per un processo di ottimizzazione in un solo passo (Processo O.S.O.) nel sito 46. In questo caso, abbiamo selezionato e utilizzato un impianto MIS V3 (MIS Implants Technologies) e una ben documentata barriera corticale Soft Lamina 25x25 (Osteobiol by Tecnoss). L’ottimizzazione del tessuto molle è stata ottenuta con un moncone personalizzato generato tramite il sistema VPI Cervico (VP Innovato Holdings).
Dopo l’anestesia locale (Articaina con adrenalina1.200.00) l’accesso alla cresta edentula è stato fornito con una lama 15C utilizzando incisioni intrasulculari buccali e linguali dalla zona distale del dente 43 fino all’aspetto mesiale del dente 48, e un’incisione mid-crestale sul sito edentulo 46 (Fig. 3). Le aree delle papille interdentali sono state attentamente dissezionate a spessore parziale e sono stati sollevati con cura 2 lembi (buccale e linguale) (Fig. 4). Il lembo buccale è stato ulteriormente rilasciato con una incisione periostea utilizzando una lama 15 e uno scollaperiostio. Per il rilascio del lembo linguale si è ottenuto con un leggero stiramento delle fibre del muscolo miloioideo mentre si tirava il lembo verso l’alto (Fig. 5). È stato eseguito un’operazione di preparazione con un protocollo di espansione del margine alveolare utilizzando frese Densah (Versah) sul sito 46, ed è stato inserito un impianto MIS V3 con diametro di 4,3 mm e lunghezza di 10 mm (MIS Implants Technologies) 2 mm al di sotto del margine crestale con una coppia di serraggio di 35 N.cm, lasciando una significativa deiscenza vestibolare (Fig. 6). Un moncone singolo (moncone di connessione con diametro di 5,7 mm e altezza di 2 mm, MIS Implants Technologies) è stato collegato all’impianto con una coppia di serraggio finale di 30 N.cm (Fig. 7).
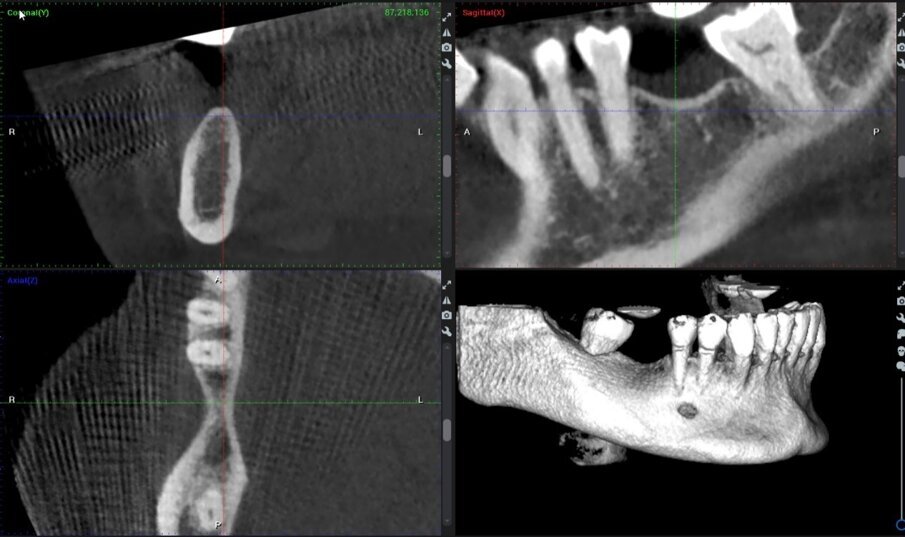
Fig. 1_Immagini CBCT pre-operatorie del sito 46.
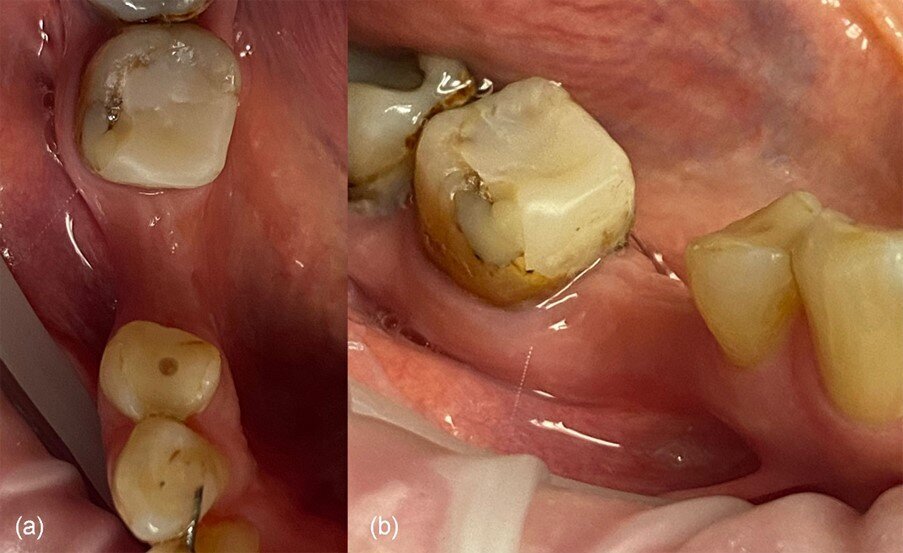
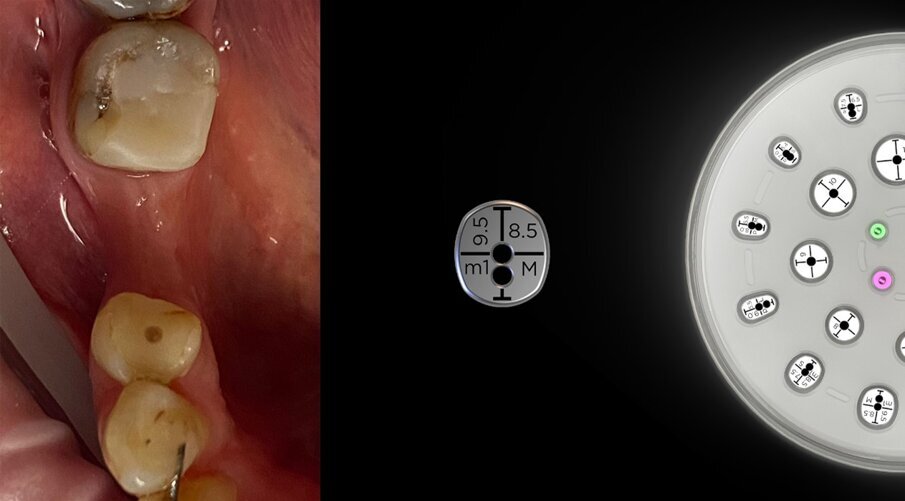
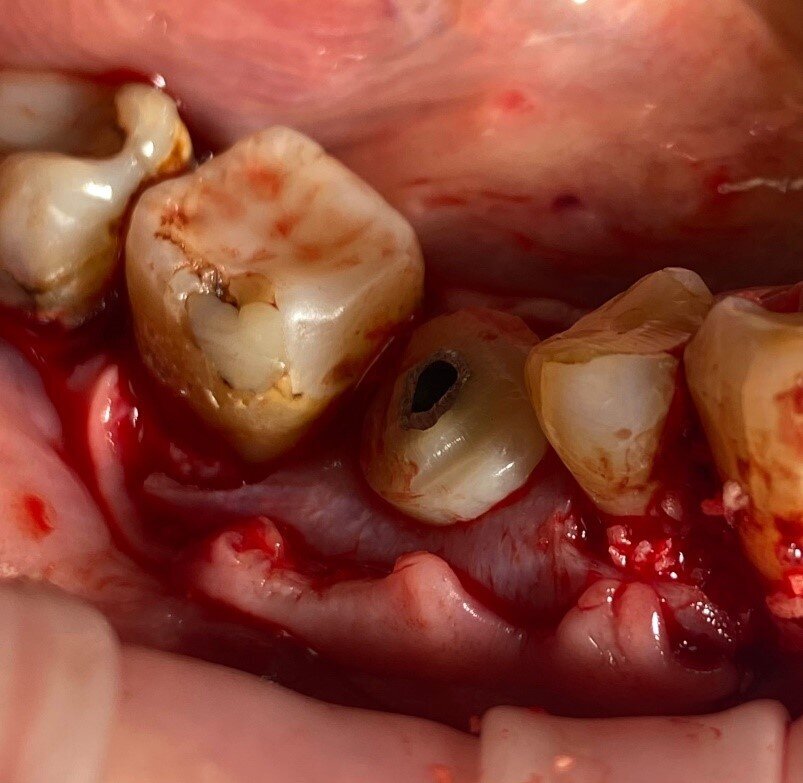
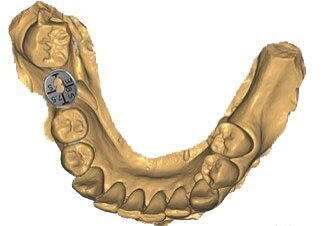
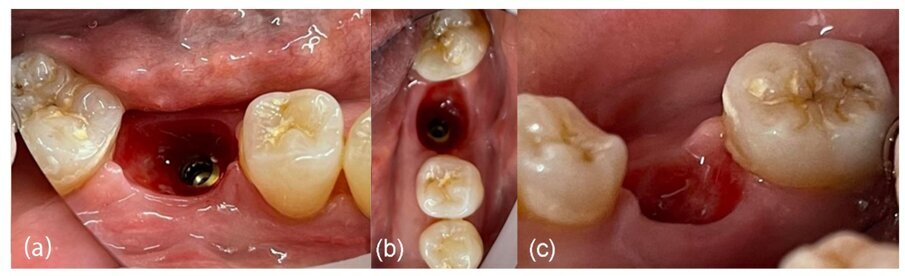
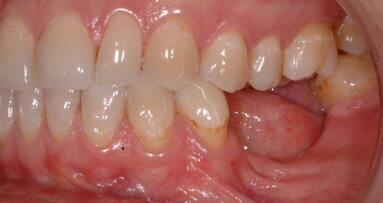
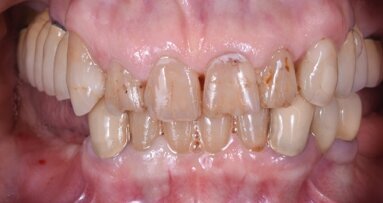
Fig. 2_Situazione iniziale del sito 46: a) vista occlusale, b) vista vestibolare.
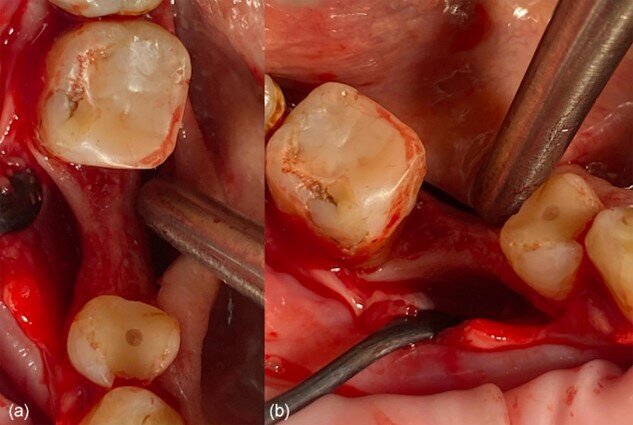
Fig. 3_Progetto dell’incisione nel sito 46: a) vista occlusale, b) vista vestibolare.
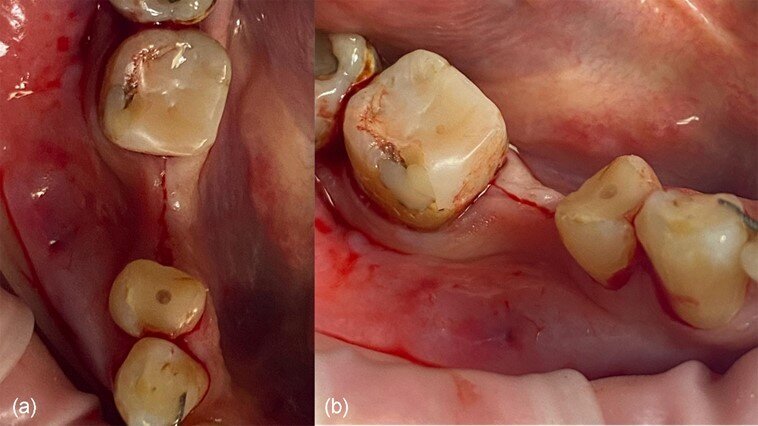
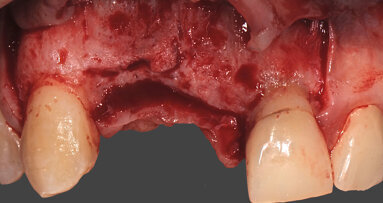
Fig. 4_Situazione clinica dopo l’elevazione del lembo: a) vista occlusale, b) vista vestibolare.
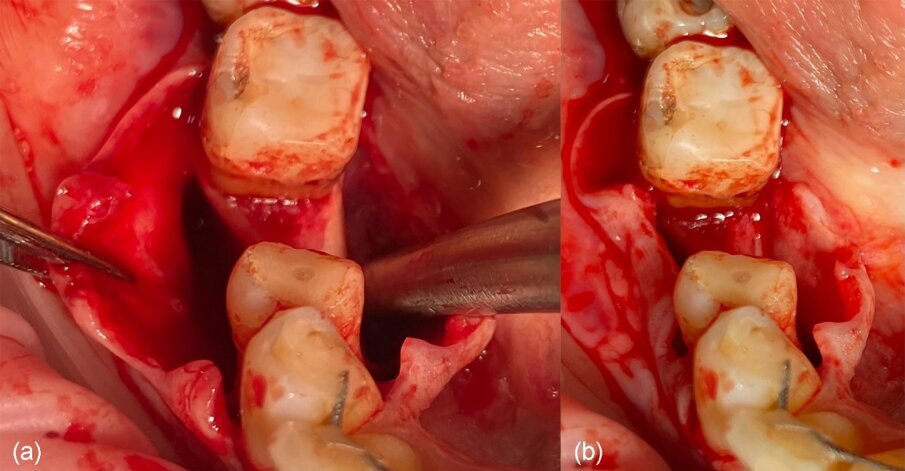
Fig. 5_a) Rilascio del lembo buccale dopo incisione periostea, b) passivazione del lembo linguale dopo il rilascio del muscolo miloioideo.
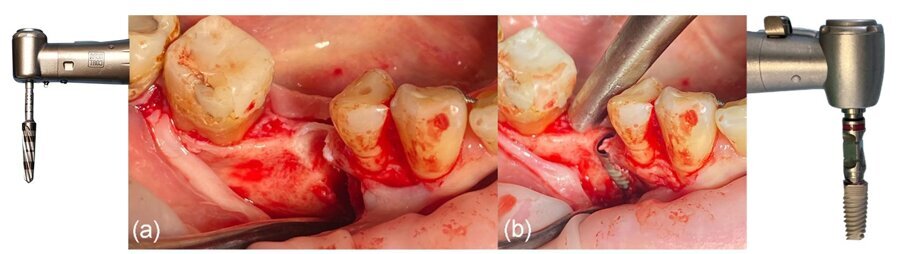
Fig. 6_a) Deiscenza vestibolare dopo la perforazione, b) situazione clinica dopo il posizionamento dell’impianto.
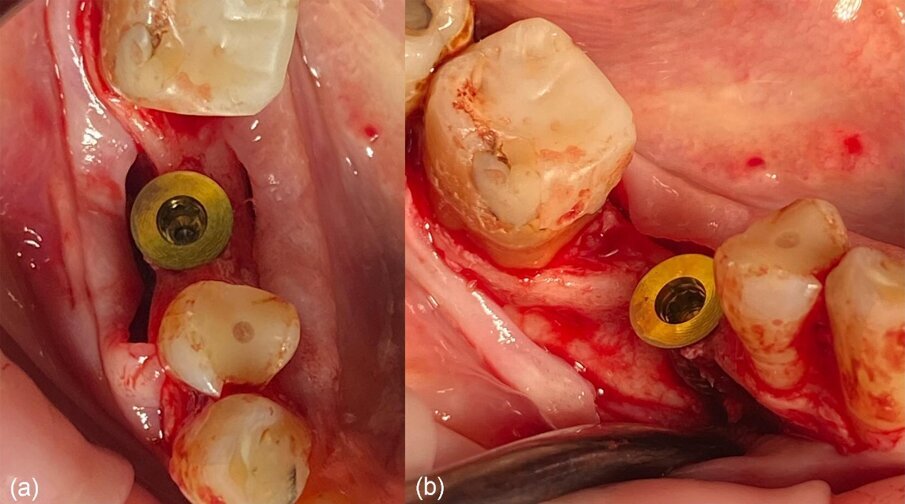
Fig. 7_Moncone di connessione in situ: a) vista occlusale, b) vista vestibolare.
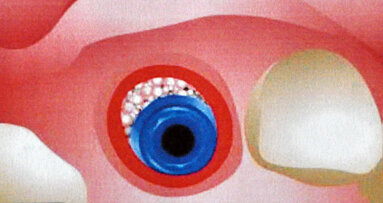
Utilizzando il sistema di guida VPI Cervico, è stato selezionato un tab m1M adeguato per il sito e un moncone provvisorio con diametro di 5,7 mm è stato trasferito al VPI Cervico nel relativo stampo dove è stato generato un moncone personalizzato m1M con composito ibrido nano-flusso (Figg. 8, 9). È stata realizzata una scanalatura periferica di 1 mm di larghezza e 1 mm di profondità utilizzando una fresa tonda piccola a 3 mm al di sopra della base del moncone. La metà buccale del moncone è stata attentamente rifinita dal centro ai suoi bordi periferici con una fresa diamantata per la lucidatura al fine di conferire un aspetto smussato (Fig. 10). Infine, il moncone è stato lucidato e quindi pulito con un vaporizzatore. Dopo la preparazione del sito, il posizionamento dell’impianto e la generazione del moncone, una barriera corticale lamellare (Soft Lamina 25x25 - Osteobiol) è stata idratata in soluzione salina sterile per 5 minuti. Poiché una sezione di meno 1 mm (profondità della scanalatura periferica sul moncone generato) su un moncone molare inferiore di dimensioni medie (m1M, dimensioni: 9,5x8,5 mm) sul sistema di guida VPI Cervico corrisponde a un piccolo moncone molare inferiore (m1S, dimensioni 8,5x7,5 mm), è stato utilizzato un guida m1S come riferimento per ritagliare un’apertura nella barriera per un corretto adattamento del moncone personalizzato nell’area della scanalatura (Fig. 11). La barriera lamellare è stata poi modellata con una lama 15C e delle micro-forbici in base alla topografia del sito, e si è prestata attenzione per assicurare che la membrana fosse saldamente attaccata intorno al moncone nell’area della scanalatura (Fig. 12).
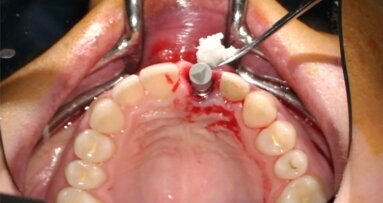
Prima del posizionamento del composto moncone-barriera, il sito è stato sovra-innestato con 1,5 g di xenoinnesto GenOs 0,5 g (dimensione delle particelle: 0,5-1 mm - Osteobiol) precedentemente idratato con soluzione salina sterile (Fig. 13). Dopo che il materiale d’inserzione ossea è stato posizionato su entrambi i lati vestibolare e linguale del sito, i due lembi sono stati delicatamente separati per consentire un preciso posizionamento del composto sopra il moncone di connessione. Il moncone personalizzato è stato fissato con una coppia di serraggio di 20 N.cm. e rifinito sul lato occlusale-linguale per evitare qualsiasi contatto con i denti antagonisti superiori. L’apertura del cilindro provvisorio è stata sigillata con nastro in teflon e composito fluente polimerizzato con luce (Fig. 14).
Fig. 8_Selezione di un profilo m1M VPI Cervico per la generazione di un moncone personalizzato.
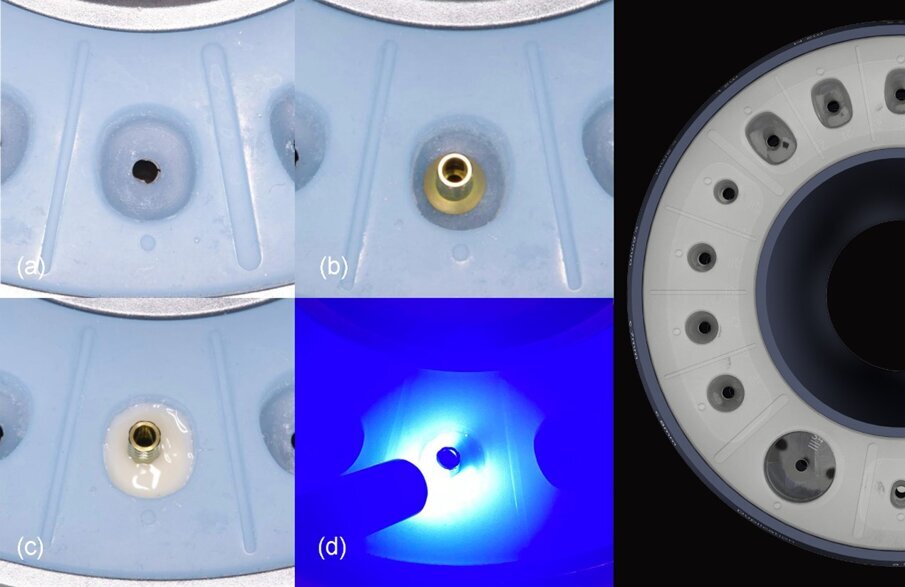
Fig. 9_Da a) a d): Generazione di un moncone personalizzato m1M con lo stampo VPI Cervico.
Fig. 10_Modifica del moncone personalizzato regolare m1M in un moncone per rigenerazione ossea guidata (GBR) con scanalatura periferica.
Fig. 11_Utilizzo della guida m1S per la preparazione della Lamina soft.
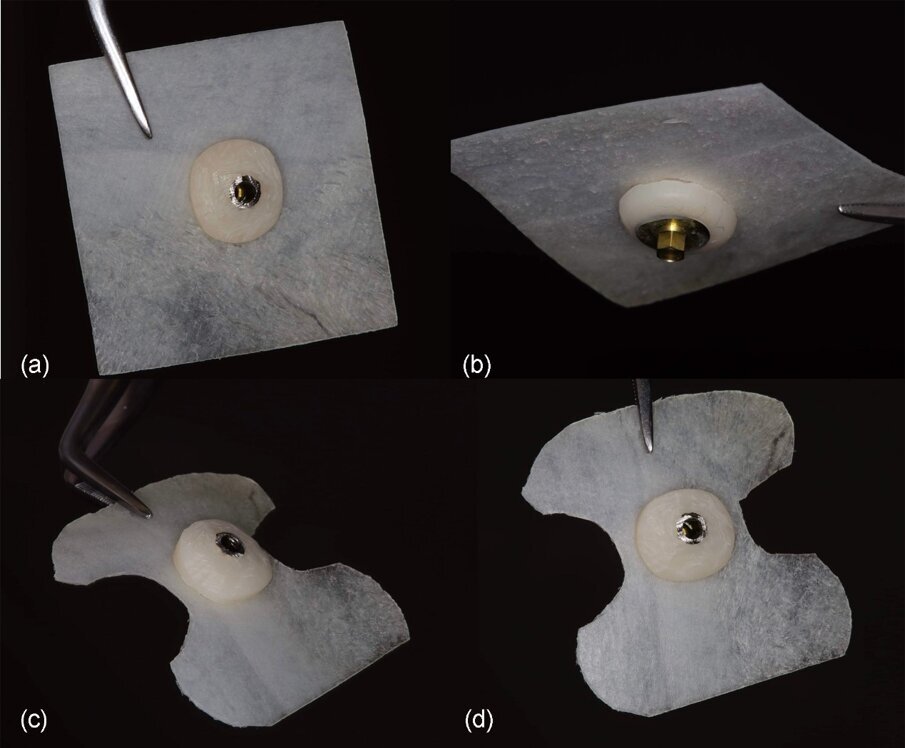
Fig. 12_a) e b) Composito lamina-moncone prima della modellatura finale, c) e d) Composito dopo la modellatura della barriera in base alla topografia del sito.
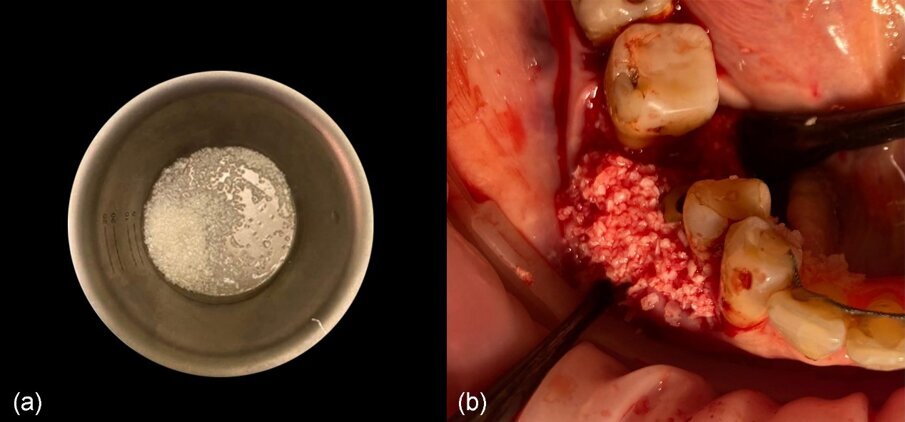
Fig. 13_a) Materiale da innesto dopo l’idratazione con soluzione salina, b) situazione clinica dopo l’innesto.
Fig. 14_Composito lamina-moncone in situ.
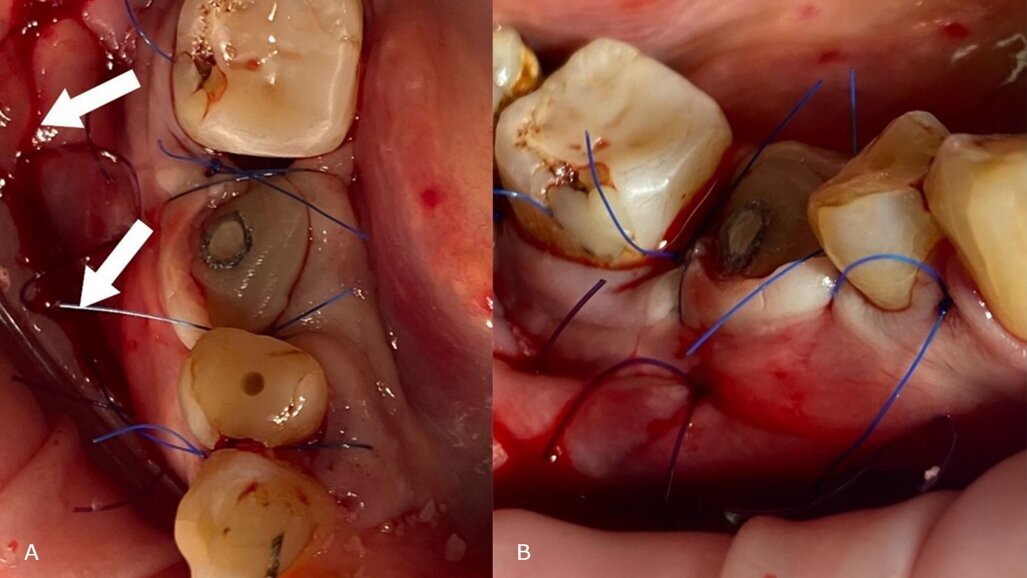
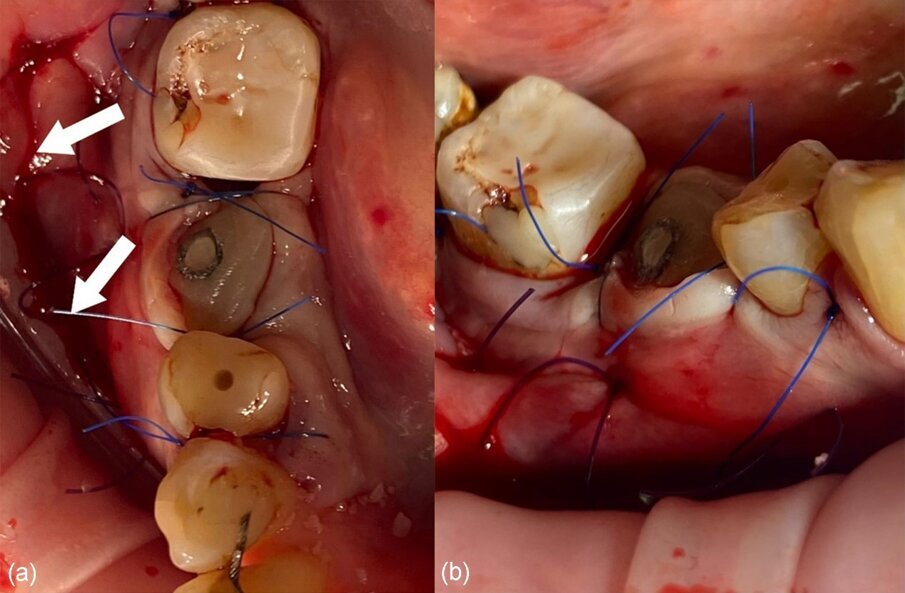
Fig. 15_a) e b) Strato intermedio (colore viola scuro) e strato superficiale (colore blu) di sutura monofilamento. Le frecce bianche indicano la posizione dell’incisione superficiale.
L’adattamento del lembo e la chiusura sopra la barriera e intorno al moncone sono stati eseguiti con 2 strati di sutura:
- uno strato intermedio di sutura di adattamento monofilamento non assorbibile 4.0 (Glycolon, Resorba) fino a 2 mm sotto la linea mucogengivale per una stabilizzazione aggiuntiva della membrana e un avanzamento coronale del lembo;
- uno strato superficiale di sutura di chiusura a materassaio verticale non assorbibile 5.0 (Resolon, Resorba) per la stabilizzazione della papilla tra gli elementi dentali e sutura interrotta semplice nelle aree prossimali al moncone.
Infine, è stata eseguita un’incisione superficiale profonda nel vestibolo con una lama 15 per ridurre la trazione muscolare durante il periodo di guarigione precoce (primo mese) (Fig. 15).
Al paziente sono state fornite istruzioni post-operatorie dopo l’intervento chirurgico. Le è stato consigliato di sciacquare con una soluzione disinfettante (BlueM Mouthwash, BlueM Oral Care) due volte al giorno per un periodo di 1 mese. Le è stato inoltre detto di evitare di spazzolare l’area chirurgica durante lo stesso periodo e di evitare di masticare cibi di consistenza dura nella parte sinistra della bocca. Sono stati prescritti anche Augmentin 875/125 mg (2 volte al giorno per una settimana), azitromicina 500 mg (1 dose singola dopo l’intervento chirurgico) e ibuprofene 600 mg (2 volte al giorno per 5 giorni), e sono stati programmati controlli a 2 settimane e a 1, 2, 3 e 4 mesi post-operatori.
Caso 2
Una paziente di 68 anni di sesso femminile ha frequentato la nostra clinica e ha richiesto un trattamento di riabilitazione per il sito edentulo 46. La paziente era una non fumatrice in buona salute, senza malattie parodontali attive (nessuna perdita di attacco, tasche al sondaggio e BOP). È stata eseguita una tomografia computerizzata a fascio conico (CBCT) preoperatoria nel quarto quadrante inferiore (Fig. 16). I risultati hanno rivelato un’atrofia orizzontale della cresta nella zona del sito 46. La densità ossea è stata definita come di tipo 2 e la distanza dal margine alveolare più coronale al canale alveolare inferiore era sufficiente per posizionare un impianto dentale di 10 mm di lunghezza. Durante l’esame clinico è stata misurata una ampiezza del tessuto cheratinizzato di 4 mm sulla sottile cresta.
Dopo l’anestesia locale (Articaina con adrenalina 1.200.000), abbiamo utilizzato lo stesso flusso di lavoro chirurgico del caso 1: dopo l’elevazione e il rilascio del lembo su entrambi i lati della cresta, è stato posizionato un impianto MIS V3 con diametro di 4,3 mm e lunghezza di 10 mm (MIS Implants Technologies) subcrestale con il protocollo di espansione Versah con una stabilità primaria di 35 N.cm. Un moncone di connessione con diametro di 5,7 mm e altezza di 2 mm è stato fissato sopra la piattaforma dell’impianto con 30 N.cm. Il sito è stato innestato con osso preparato con l’addizione di SPRF (Process for PRF) e 2 g di osso equino collagenato 0,5 g (Biogen dimensione delle particelle: 0,5-1 mm, Bioteck). Il materiale d’innesto è stato poi coperto da una lamina corticale (Lamina Soft, Osteobiol) montata su un moncone personalizzato realizzato in laboratorio adattato a un cilindro temporaneo da 5,7 (MIS Implants Technologies). La chiusura del lembo è stata ottenuta con i 2 strati di sutura e lo stesso materiale di sutura descritto nella fase 1, e la riduzione della trazione muscolare è stata eseguita con un’incisione superficiale alla profondità del vestibolo, come già spiegato. Le istruzioni post-operatorie e la medicazione erano identiche a quelle del caso 1.
In questo caso particolare abbiamo eseguito una impronta digitale prima del trattamento chirurgico con un dispositivo di scansione intraorale e un file STL è stato inviato al tecnico di laboratorio. Lo scopo del flusso di lavoro digitale adottato qui era di progettare digitalmente e preparare l’unità di profilo personalizzato e un template come guida per il taglio della barriera lamellare con i seguenti processi:
Creazione del profile
Il file STL è stato prima importato nel software exocad (Fig. 16). Successivamente, è stata selezionata e importata nel software una tabella digitale VPI Cervico adatta al sito e allo spazio interprossimale (Fig. 17). Un’unità di profilo corrispondente all’abbinamento digitale della tabella è stata progettata dopo la scansione del modulo VPI Cervico con un dispositivo di scansione Ceramill Map 400 (Amann Girrbach) e posizionata 3 mm al di sotto della gengiva sul modello exocad. Il design è stato inviato all’operatore e, dopo la sua approvazione, è stata creata una scanalatura di 1 mm di larghezza e 0,5 mm di profondità a livello della mucosa marginale utilizzando gli strumenti di exocad (Figg. 18, 19). Il profilo è stato quindi stampato con una stampante 3D Asiga 3D max utilizzando una resina free print temp A2, pulito con alcool isopropilico al 99%, post-indurito utilizzando Otoflash G171 con azoto e infine rimosso dalla sua struttura di supporto e pulito con un vaporizzatore (Fig. 20). Questa unità di profilo è stata collegata in bocca durante l’intervento chirurgico con il cilindro temporaneo per generare un moncone personalizzato. Sono state aggiunte estensioni mesiali e distali occlusali ai denti vicini 45 e 47 all’unità al fine di facilitarne il posizionamento e l’adattamento all’interno del cilindro provvisorio.
Fig. 16_Immagini CBCT preoperatorie del sito 46.
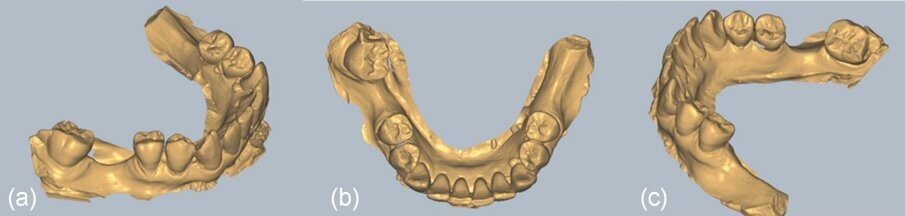
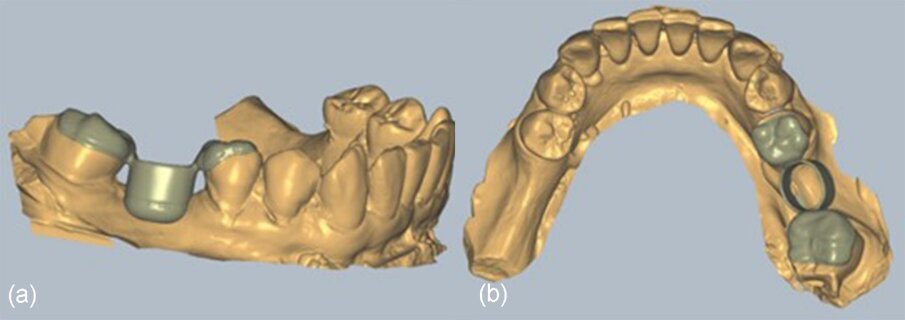
Fig. 17_a) fino a c): Viste del file STL nel software Exocad.
Fig. 18_Scelta della tabella digitale VPI appropriata sul modello Exocad.
Fig. 19_L’unità di profilo con la scanalatura di trattenimento a livello della mucosa marginale generata con gli strumenti di Exocad.
Fig. 20_L’unità di profilo personalizzato prima del suo collegamento con il cilindro provvisorio.
Fig. 21_Lamina Soft in soluzione salina e il template in acrilico.
Creazione del Template
L’unità di profilo STL è stata importata nel software Blender 3D (www.blender.org) e una forma di 45x45x3 mm è stata creata per servire come template per la futura modellatura della membrana. L’unità di profilo e il template sono stati allineati e successivamente è stata effettuata un’intersezione, utilizzando l’unità, sul template che è stato successivamente ritagliato. Lo spessore del template digitale è stato ulteriormente aumentato e il file STL è stato stampato con una stampante 3D Formlabs Form 2 utilizzando la resina Dental LT. Il template stampato è stato successivamente pulito con alcool isopropilico al 99% per rimuovere la resina in eccesso, post-indurito in un dispositivo BB Cure rimosso dalla sua struttura di supporto con una fresa diamantata e pulito con un vaporizzatore. Alla fine della procedura, lo spessore è stato ridotto da 3 a 1 mm con una lima umida dentale. Questo template è stato successivamente utilizzato durante l’intervento chirurgico sopra la barriera Lamina Soft come guida per eseguire un’apertura con una micro-lama per il suo ulteriore adattamento corretto nell’area di scanalatura dell’unità di profilo fabbricata in laboratorio (Fig. 21).
Risultati
Entrambi i pazienti hanno seguito le istruzioni post-operatorie e hanno avuto un processo di guarigione senza complicazioni. I risultati sono stati valutati per i 2 casi a 4 mesi (T2). Una valutazione aggiuntiva è stata effettuata per il secondo caso con il periodo di follow-up più lungo a 2 anni e 7 mesi (T3). La rivalutazione dal periodo preoperatorio T1 a 4 mesi e 2 anni e 7 mesi è stata clinica e radiologica.
Caso 1
Rivalutazione clinica
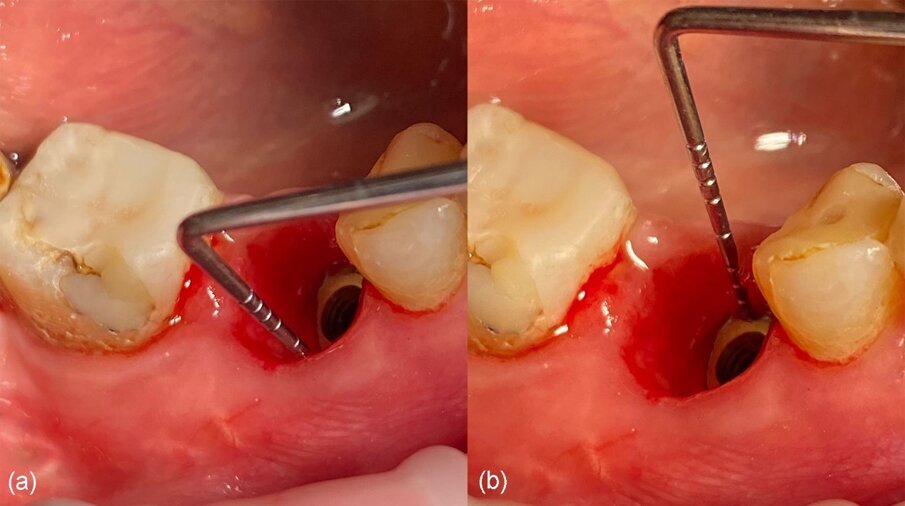
L’esame clinico al termine del periodo di guarigione di 4 mesi ha rivelato, dopo la rimozione del moncone anatomico e l’uso di una sonda parodontale (sonda Williams PW - Hu-Friedy Group), la generazione di un profilo cervicale adeguato (Fig. 22) con un’altezza del tessuto molle di 4 mm dalla piattaforma del moncone di connessione fino al margine del tessuto marginale sia sul lato vestibolare che sul lato linguale (Fig. 23). Tenendo conto che l’altezza del moncone di connessione era di 2 mm, la larghezza complessiva del complesso sopracrestale è stata valutata a 6 mm dalla piattaforma dell’impianto (Fig. 24). Il tessuto cheratinizzato è stato preservato sia sul lato vestibolare che sul lato linguale.
Ri-valutazione radiologica
Le immagini CBCT sono state ottenute utilizzando un sistema di radiografia computerizzata CS8100 3D Carestream (Carestream Health) con una dimensione di voxel di 0,150 mm e un campo visivo di 8x9 cm prima (T1) e 16 settimane (T2) dopo l’inserimento dell’impianto. I file originali in formato DICOM sono stati importati nel software Romexis (Planmeca) per l’analisi. Per entrambi i set di dati T1 e T2, abbiamo selezionato per la valutazione delle sezioni trasversali nel mezzo del sito sulla sezione assiale e perpendicolare alla cresta alveolare (Fig. 25).
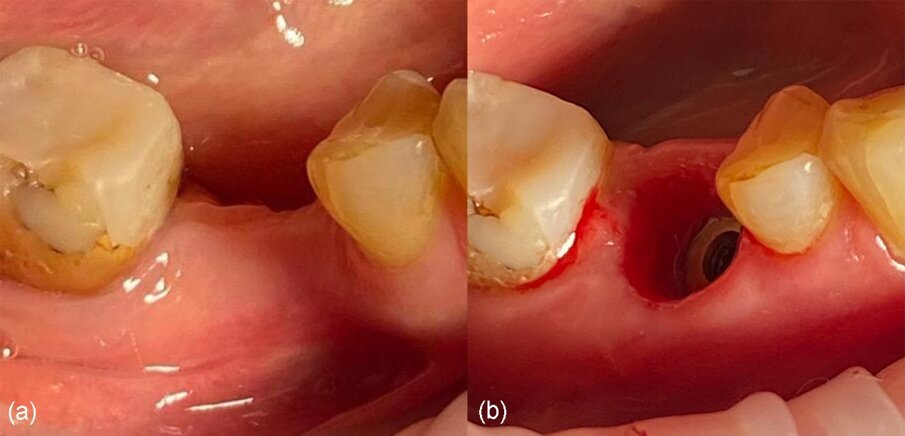
Fig. 22_a) Vista clinica vestibolare pre-operatoria, b) vista clinica vestibolare post-operatoria a 4 mesi.
Fig. 23_Registrazione dell’altezza del tessuto molle sopra la piattaforma del moncone di connessione con una sonda parodontale.
Fig. 24_La configurazione del complesso sopracrestale a 4 mesi per il caso 1.
Fig. 25_a), b): Immagini coronali e assiali CBCT prima dell’intervento chirurgico e a 4 mesi dopo l’intervento.
Caso 2
Rivalutazione clinica
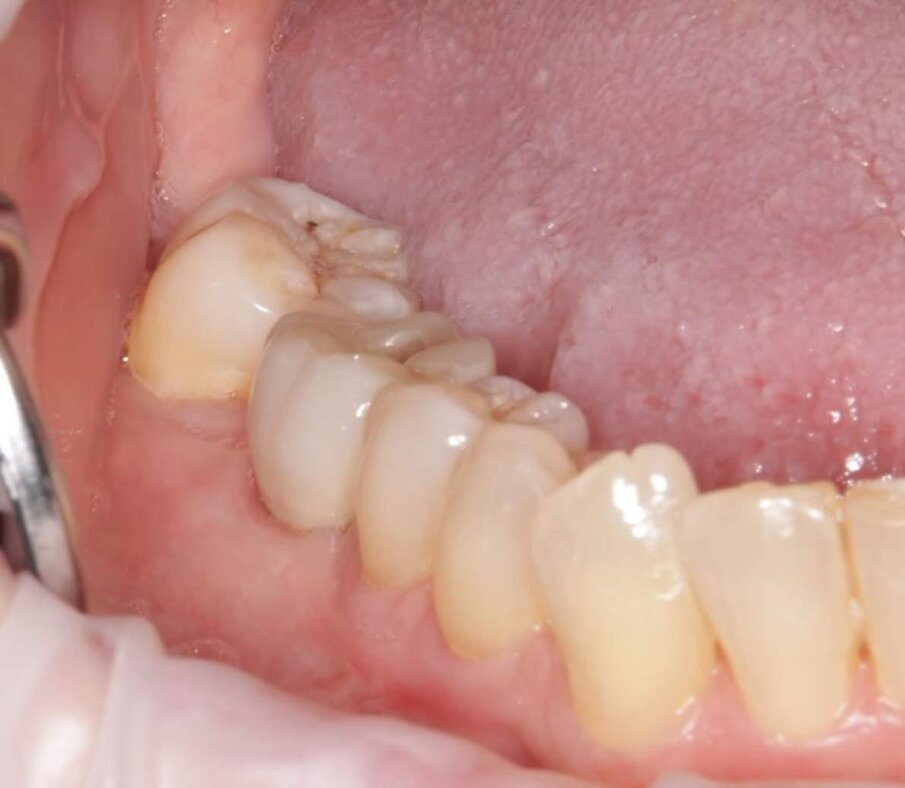
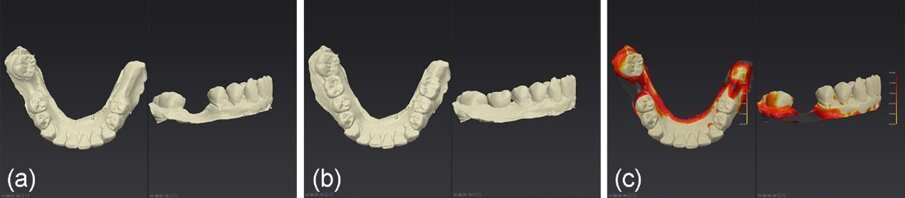
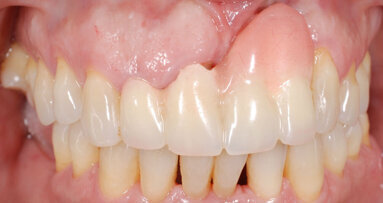
Nel caso 2, il tessuto cheratinizzato è stato preservato anche sui lati vestibolare e linguale a T2 e i valori dell’altezza del complesso sovracrestale erano identici a quelli registrati nel caso 1 (Fig. 26). Per quanto riguarda la valutazione a T3 e dopo l’inserimento di una corona monolitica in zirconia completa a 4 mesi, è evidente che è stata preservata una mimica del profilo cervicale del tessuto molle con conservazione del tessuto cheratinizzato (Fig. 27). Infine, sono state effettuate impronte digitali intraorali utilizzando lo scanner intraorale iTero (Align Technology), a T1 e a T3. I file STL (standard tessellation language) sono stati esportati nel software DTX Studio Clinic (Envista) per la comparazione nel tempo. Sulla base di un algoritmo di informazioni reciproche, le scansioni sono state sovrapposte automaticamente e un codice a colori ha mostrato le aree di differenza (Fig. 27).
Rivalutazione radiologica
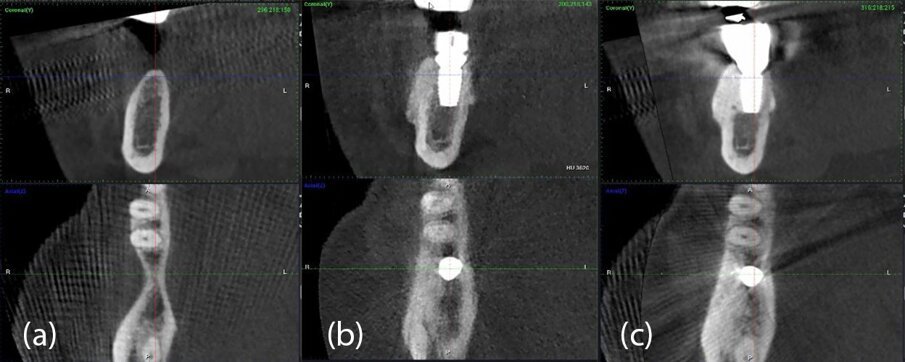
La stessa metodologia del caso 1 è stata applicata per il confronto T1-T2-T3. La valutazione è stata effettuata attraverso sezioni trasversali prese nel mezzo del sito sulla sezione assiale e perpendicolari alla cresta alveolare (Figg. 28, 29).
Fig. 26_Generazione del profilo cervicale a 4 mesi dopo la rimozione del moncone personalizzato: a) vista vestibolare, b) vista occlusale, c) vista linguale.
Fig. 27_Risultato clinico del sito 46 con corona in zirconia in situ dopo 2 anni e 7 mesi.
Fig. 28_a), b): File STL pre-operatori e a 2 anni e 7 mesi post-operatori esportati nel software DTX Studio; c) i due file STL sovrapposti per ulteriori confronti.
Fig. 29_Valutazione CBCT del caso 2 da sinistra a destra: a) immagini coronali e assiali preoperatorie; b) immagini coronali e assiali CBCT post-operatorie a 4 mesi; c) immagini coronali e assiali CBCT a 2 anni e 7 mesi.
Disclosure
Gli autori dichiarano di non avere conflitti di interesse.
Bibliografia
- Beretta, M.; Poli, P.P.; Pieriboni, S.; Tansella, S.; Manfredini, M.; Cicciù, M.; Maiorana, C. Peri-implant soft tissue conditioning by means of customized healing abutment: A randomized controlled clinical trial. Materials 2019, 12, 3041.
- Berglundh, T.; Lindhe, J. Dimension of the peri implant mucosa. Biological width revisited. J. Clin Periodontol. 1996, 10, 971–973.
- Carlsen, A.; Gorst-Rasmussen, A.; Jensen, T. Donor site morbidity associated with autogenous bone harvesting from the ascending mandibular ramus. Implant. Dent. 2013, 22, 503–506.
- Esposito, M.; Grusovin, M.G.; Felice, P.; Karatzopoulos, G.; Worthington, H.V.; Coulthard, P. The efficacy of horizontal and vertical bone augmentation procedures for dental implants-Cochrane systematic review. Our. J. Oral Implant. 2009, 2, 167–184.
- Fabbri, G.; Staas, T.; Linkevicius, T.; Valantiejiene, V.; González-Martin, O.; Rompen, E. Clinical performance of a novel two-piece abutment concept: Results from a prospective study with a 1 year-follow up. J. Clin. Med. 2021, 10, 1594.
- Giannobile, W.V.; Jung, R.E.; Schwarz, F. Evidence-based Knowledge on the aesthetics and Maintenance of peri-implant soft tissues: Osteology Foundation Consencus Report Part 1-Effects of soft tissue augmentation procedures on the maintenance of peri-implant soft tissue health. Clin. Oral Implant. Res. 2018, 29 (Suppl. S15), 7–10.
- Her, S.; Kang, T.; Fine, M.J. Titanium Mesh as an alternative to a membrane for ridge augmentation. J. Oral Maxillofac. Surg. 2012, 70, 803–810.
- Huwais, S.; Meyer, E.G. A novel osseous densification approach in implant osteotomy preparation to increase biomechanical primary stability, bone mineral density, and bone-to -implant contact. Int. J. Oral Max. Implant. 2016, 32, 27–36.
- Glauser, R.; Schupbach, P.; Gottlow, J.; Hammerle, C.H.F. Peri implant soft tissue barrier at experimental one-piece mini-implants with different surface topography in humans: A light- microscopic overview and histometric analysis. Clin. Implant. Dent. Relay Res. 2005, 7 (Suppl. S1), S44–S51.
- Koutouzis, T.; Huwais, S.; Hasan, F.; Trahan, W.; Waldrop, T.; Neiva, R. Alveolar ridge expansion by osseodensification-mediated plastic deformation and compaction autographing: A multi-center retrospective study. Implant. Dent. 2019, 28, 349–355.
- Lekhom, U.; Zarb, G.A. Patient selection and preparation. In Tissue Integrated Prostheses: Osseointegration in Clinical Dentistry; Branemark, P.I., Zarb, G.A., Albrektsson, T., Eds.; Quintessence Publishing Company: Chicago, IL, USA, 1985; pp. 199–209.
- Leventis, M.; Vergoullis, I,; Valavanis, K. Soft tissue emergence profile reconstruction. EDI Journal. 2021,4, 42.
- Mattei, B.M.; Imanishi, S.A.W.; de Oliveira Ramos, G.; de Campos, P.S.; Weiss, S.G.; Deliberator, T.M. Mouthwash with active oxygen (BlueM) induces keratinocytes proliferation. Open J. Stomatol. 2020, 10, 107–114.
- Mattheos, N.; Vergoullis, I.; Janda, M.; Miselli, A. The implant supracrestal complex and its significance for long-term successful clinical outcomes. Int. J. Prosthodont. 2021, 34, 88–100.
- Retzepi, M.; Donos, N. Guided Bone Regeneration: Biological principal and therapeutic applications. Clin. Oral. Implant. Res. 2010, 21, 567–576. Retzepi, M.; Donos, N. Guided Bone Regeneration: Biological principal and therapeutic applications. Clin. Oral. Implant. Res. 2010, 21, 567–576.
- Rossi, R.; Rancitelli, D.; Poli, P.P.; Rasia Dal Polo, M.; Nannmark, U.; Maiorana, C. The use of a Collagenated porcine cortical lamina in the reconstruction of alveolar ridge defects. A Clinical and histological study. Minerva Stomatol. 2016, 65, 257–268.
- Rossi, R.; Ghezzi, C.; Tomecek, M. Cortical Lamina: A new device for the treatment of Moderate and severe tridimensional bone and soft tissue defects. Int. J. Esthet. Dent. 2020, 15, 454–473.
- Sanchez, I.S.; Ortiz Vigon, A.; Sanz Martin, I.; Figuero, E.; Sanz, M. Effectiveness of lateral bone augmentation on the alveolar crest dimension: A systematic review and meta-analysis. J. Dent. Res. 2015, 94 (Suppl. S9), 128S–142S.
- Serino, G.; Strom, C. Peri-implantitis in partially edentulous patients: Association with inadequate plaque control. Coin Oral Implant. Res. 2009, 20, 169–174.
- Stefanini, M.; Marzadori, M.; Sangiorgi, M.; Rendon, A.; Testori, T.; Zucchelli, G. Complications and treatment errors in peri-implant soft tissue management. Periodontology 2000 2023, 92, 263–277. Wenstromm, J.L.; Bengazi, F.; Lekholm, U. The influence of masticatory mucosa on the peri-implant soft tissue condition. Clin. Oral Implant. Res. 1994, 5, 1–8.
- Tzovairis, A.;Van Someren Brand, R.;,Rossi,R. One step optimisation (o.s.o) process for hard and soft tissue augmentation in single implant sites with the Poncho Lamina Technique: Clinical protocol description and case report. Mod Res Dent. 2022, 7, 705-716.
- Tzovairis, A.; Leretter, M.; Vandenberghe, B.; Rossi, R. The Poncho Lamina Technique: A Protocol for Hard and Soft Tissue Augmentation in Atrophic Ridges Receiving Adjacent Implants. Medicina 2023, 59, 1994.
- Vergoullis, I.; Badell, C.L.; Papadopoulos, G. An innovative approach for the selection, generation and recording of a custom emergence profile around implants. J. Implant. Adv. Clin. Dent. 2017, 9, 6–19.
L'articolo è stato pubblicato su implants international magazine of oral implantology Italian edition n. 1/24.
Tag:
Con questo articolo desidero mostrare un caso clinico di gestione dei tessuti molli periimplantari mediante l’associazione di matrice in collagene ...
Da un punto di vista estetico, un impianto malposizionato specialmente nella regione anteriore, porta inevitabilmente alla realizzazione di un lavoro ...
WEST LAFAYETTE, Indiana, USA: La xerostomia è una condizione frequentemente riscontrata nei pazienti sottoposti a emodialisi, chemioterapia o radioterapia ...
La chirurgia rigenerativa ossea si occupa da più di vent’anni della soluzione delle atrofie ossee conseguenti alla perdita degli elementi dentali. Molte ...
Una paziente di 65 anni si presentò alla nostra attenzione, riferita dal dentista curante, per risolvere il suo edentulismo posteriore bilaterale. ...
Neoss sta lanciando un nuovo tipo di membrana in PTFE, in esclusiva con Neoss, che porta l’innovazione delle membrane in PTFE ad un altro livello: la ...
Le tecniche di rigenerazione ossea guidata, siano esse di tipo orizzontale, verticale, piuttosto che combinata, sono ormai procedure ben codificate e ...
Dental Tribune intervista il dott. Alessandro Carmignani che ha ricevuto il premio PEERS nella sezione Protesi cementata, con un caso clinico dal titolo ...
Introduzione
La guarigione del sito alveolare post estrattivo è un processo biologico che induce un parziale riassorbimento dell’osso ...
La piezosurgery (PES) è una tecnica chirurgica utilizzata in varie branche specialistiche della medicina, al fine di realizzare osteotomie ...
Live webinar
mer. 15 aprile 2026
20:00 (CET) Rome
Live webinar
gio. 16 aprile 2026
2:00 (CET) Rome
Linda Hecker MS, BSDH, RDH
Live webinar
gio. 16 aprile 2026
18:00 (CET) Rome
Dr. Pär-Olov Östman, Dr. Robert Gottlander DDS
Live webinar
ven. 17 aprile 2026
18:00 (CET) Rome
Live webinar
ven. 17 aprile 2026
19:00 (CET) Rome
Dr. Stuart Yeaton BDentSc, MOrth
Live webinar
lun. 20 aprile 2026
19:00 (CET) Rome
Dr. Alberto Monje DDS, MS, PhD
Live webinar
mer. 22 aprile 2026
17:00 (CET) Rome
MDT Andreas Chatzimpatzakis



 Austria / Österreich
Austria / Österreich
 Bosnia ed Erzegovina / Босна и Херцеговина
Bosnia ed Erzegovina / Босна и Херцеговина
 Bulgaria / България
Bulgaria / България
 Croazia / Hrvatska
Croazia / Hrvatska
 Repubblica Ceca e Slovacchia / Česká republika & Slovensko
Repubblica Ceca e Slovacchia / Česká republika & Slovensko
 Francia / France
Francia / France
 Germania / Deutschland
Germania / Deutschland
 Grecia / ΕΛΛΑΔΑ
Grecia / ΕΛΛΑΔΑ
 Ungheria / Hungary
Ungheria / Hungary
 Italia / Italia
Italia / Italia
 Paesi Bassi / Nederland
Paesi Bassi / Nederland
 nordisch / Nordic
nordisch / Nordic
 Polonia / Polska
Polonia / Polska
 Portogallo / Portugal
Portogallo / Portugal
 Romania e Moldavia / România & Moldova
Romania e Moldavia / România & Moldova
 Slovenia / Slovenija
Slovenia / Slovenija
 Serbia e Montenegro / Србија и Црна Гора
Serbia e Montenegro / Србија и Црна Гора
 Spagna / España
Spagna / España
 Svizzera / Schweiz
Svizzera / Schweiz
 Turchia / Türkiye
Turchia / Türkiye
 Gran Bretagna e Irlanda / UK & Ireland
Gran Bretagna e Irlanda / UK & Ireland
 Internazionale / International
Internazionale / International
 Brasile / Brasil
Brasile / Brasil
 Canada / Canada
Canada / Canada
 America Latina / Latinoamérica
America Latina / Latinoamérica
 USA / USA
USA / USA
 Cina / 中国
Cina / 中国
 India / भारत गणराज्य
India / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
 Medio Oriente / Middle East
Medio Oriente / Middle East





















































To post a reply please login or register