La perimplantite è un processo infiammatorio, che colpisce i tessuti intorno all’impianto osteointegrato portando ad una perdita ossea periimplantare. Inoltre, si ha infiammazione dei tessuti molli. L’eziologia è di natura infettiva.
Le specie batteriche coinvolte, spesso anaerobie, sono le stesse tipicamente riscontrate nei casi di parodontite1, 2. Ulteriori fattori che possono contribuire all’instaurarsi e all’aggravarsi della patologia includono la predisposizione dell’individuo, la scarsa igiene orale, il fumo, il posizionamento non corretto dell’impianto, la scelta di un impianto non adeguato per morfologia e dimensioni, la scorretta finalizzazione protesica, la presenza di materiale estraneo, come il cemento, ed un’errata passivazione implanto-protesica (oltre al trauma occlusale).
La diffusione delle citochine pro-infiammatorie rilasciate dal sistema immunitario nella zona perimplantare infetta porta a una cascata di segnali che determina l’attivazione degli osteoclasti prossimali nell’osso alveolare3, portando al riassorbimento della matrice minerale perimplantare4, 5. Non intervenendo tempestivamente sull’infezione e sul processo infiammatorio, l’erosione si estende progressivamente portando all’esposizione del corpo implantare; nei casi più gravi, si ha la perdita dell’impianto per mancanza di sostegno da parte della struttura ossea circostante. Una volta generatosi un deficit osseo periimplantare, anche se questo è opportunamente deterso con adeguati protocolli di igiene dentale professionale, è spesso difficile stabilizzare la situazione.
Il difetto osseo perimplantare può essere comunque causa di diversi inconvenienti successivi: il paziente non potrà detergerlo correttamente con le manovre domiciliari, la cavità ossea potrà favorire la recidiva della perimplantite a causa dell’ecosistema microbico in essa presente. Inoltre, l’assenza di un adeguato supporto osseo al tessuto molle contiguo può impedire la corretta formazione del sigillo perimplantare, favorendo altresì la recidiva della patologia. Una volta risolto lo stato infiammatorio ed eliminata la causa, un efficace trattamento del difetto osseo perimplantare è quindi di primaria importanza.
Purtroppo, il difetto osseo perimplantare decontaminato non è in grado di rigenerare in modo autonomo, ed è necessario intervenire a livello chirurgico. A questo fine, sono state proposte e adottate varie tecniche di chirurgia rigenerativa6. Ad oggi non esiste consenso unanime e condiviso su quale sia il miglior protocollo da adottare. L’apertura di un lembo al fine di rendere ottimale la decontaminazione sia dei tessuti biologici che della superficie implantare è sicuramente condiviso come concetto generale. A seguire una rigenerazione ossea che preveda l’innesto di biomateriali nel difetto osseo alveolare, che possa facilitare la rigenerazione dell’osso del paziente. Inoltre, è fondamentale l’utilizzo di membrane, riassorbibili o meno, che separino il difetto osseo innestato dal tessuto mucogengivale.
Una rigenerazione corretta prevede sempre che si ottenga una guarigione ottimale dei tessuti molli, se ciò avviene, seguono, nella zona innestata, I) una fase di angiogenesi e infiltrazione di progenitori mesenchimali, (II) il rimodellamento dell’innesto e la formazione di nuovo tessuto osseo, (III) la stabilizzazione dei tessuti. Tra i sostituti ossei che possono essere impiegati, quelli derivati da tessuto osseo di mammifero sono una valida opzione7, data la somiglianza morfologica e di composizione della componente minerale del tessuto osseo tra le diverse specie. I sostituti ossei di origine animale devono essere opportunamente trattati per eliminare gli antigeni specie-specifici che potrebbero causare delle reazioni immunitarie indesiderate da parte del paziente.
Le modalità di rimozione degli antigeni dal tessuto osseo di origine sono molteplici. I trattamenti enzimatici mirano a non alterare la componente minerale ossea e, possibilmente, a conservare all’interno dell’innesto il collagene di tipo I, una proteina strutturale che favorisce la migrazione delle cellule del paziente nell’innesto osseo. Nel caso di trattamenti di natura termica, l’impiego di temperature di qualche centinaio di gradi mira all’eliminazione dell’intera componente organica presente, compreso il collagene. Nel caso dei sostituti ossei equini ottenuti per via enzimatica, è stato dimostrato che la loro colonizzazione efficace da parte degli osteoblasti ed osteoclasti del paziente, probabilmente mediata dal collagene, ne permette il rimodellamento in tempi fisiologici8.
Nel caso in cui le condizioni cliniche portino a preferire innesti con cinetiche di riassorbimento più lente è possibile utilizzare i sostituti ossei ottenuti attraverso il processo di eliminazione degli antigeni di tipo termico, che rallenta il riassorbimento del biomateriale pur garantendone una buona capacità di osteoconduzione. I sostituti ossei equini ottenuti attraverso un processo di eliminazione degli antigeni di tipo enzimatico9, come anche i sostituti ossei bovini trattati per via termica10, sono già stati utilizzati con successo per la rigenerazione di difetti ossei perimplantari conseguenti a perimplantite, ma in letteratura non sono presenti studi clinici di confronto tra le due tipologie di sostituto osseo condotti su di un numero significativo di casi e con una solida analisi statistica.
Le diverse meta-analisi che hanno analizzato gli studi oggi disponibili sul trattamento chirurgico rigenerativo della perimplantite concludono che, al momento, vi è una mancanza di evidenze scientifiche per determinare quale sia la tipologia preferibile di biomateriale da utilizzare11-13. Questo articolo presenta un caso di perimplantite a carico di due impianti, trattato con l’uso di un sostituto osseo equino a lento riassorbimento.
Caso studio
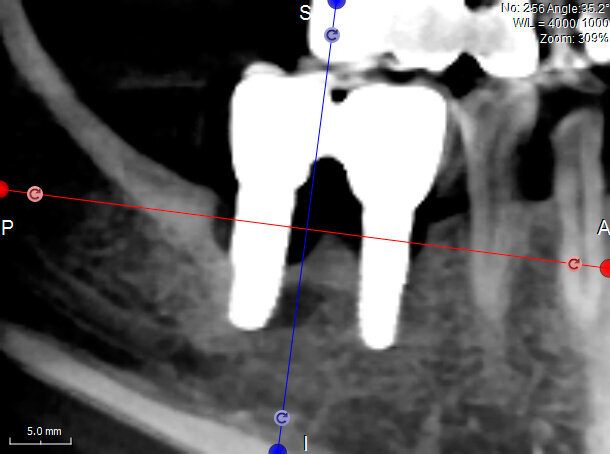
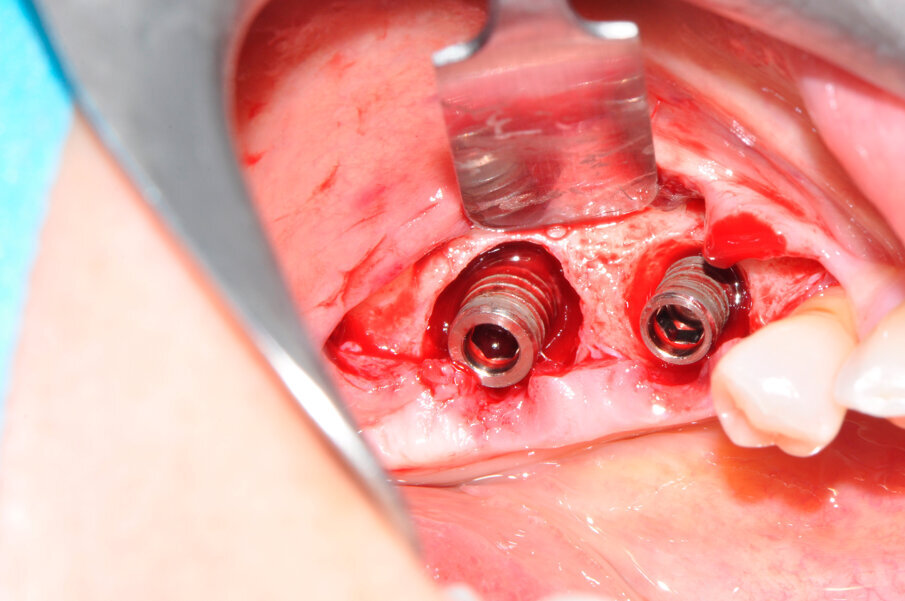
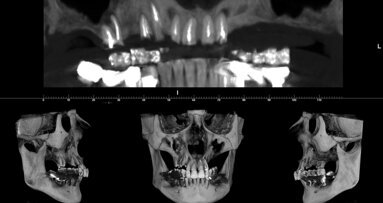
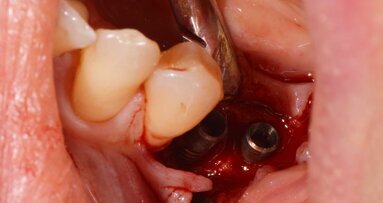
Il caso in esame riguarda una paziente di 53 anni, fumatrice, che si presentava all’osservazione per il consueto controllo periodico lamentando sanguinamento e dolore gengivale durante le manovre di igiene orale a livello di due impianti situati in posizione 4.6 e 4.7. A seguito dell’esecuzione di una CBCT per altri motivi si è potuto evidenziare un marcato riassorbimento osseo perimplantare (Fig. 1). Come si può osservare durante la chirurgia (Fig. 3) l’esposizione della superficie implantare è superiore al 50%. In entrambe le fixture con un maggior coinvolgimento in posizione 4.6. È stata inoltre riscontrata una sofferenza della mucosa attorno ai monconi delle due fixture.
In seguito alla diagnosi di perimplantite a carico di entrambi gli impianti, alla paziente è stato proposto un piano di trattamento che prevedeva la pulizia e decontaminazione della zona perimplantare seguite da un intervento di GBR che comprendeva l’innesto di un sostituto osseo di origine equina a lento riassorbimento, ottenuto per eliminazione termica degli antigeni (Calcitos, Bioteck S.p.A., Arcugnano), che potesse garantire una prolungata stabilità temporale dei profili ossei in fase di rigenerazione, e una membrana in collagene, anch’essa di origine equina (Biocollagen, Bioteck) a protezione dell’innesto.
Il sostituto osseo in granuli (0,5-1 mm) di origine equina è reso non antigenico per via termica; la sua porosità gli permette di agire come substrato adeguato all’infiltrazione dei vasi sanguigni e degli elementi cellulari provenienti dall’osso del paziente e la conseguente colonizzazione da parte del tessuto osseo endogeno. La membrana (25 x 25 x 0.2 mm) è composta di collagene naturale di tipo I estratto da tendine d’Achille equino e, secondo i principi della GBR, viene posizionata per evitare l’infiltrazione dell’innesto da parte delle cellule dei tessuti molli connettivali. La membrana garantisce un tempo di protezione di 4-6 settimane, trascorso il quale si riassorbe grazie all’azione delle collagenasi endogene.
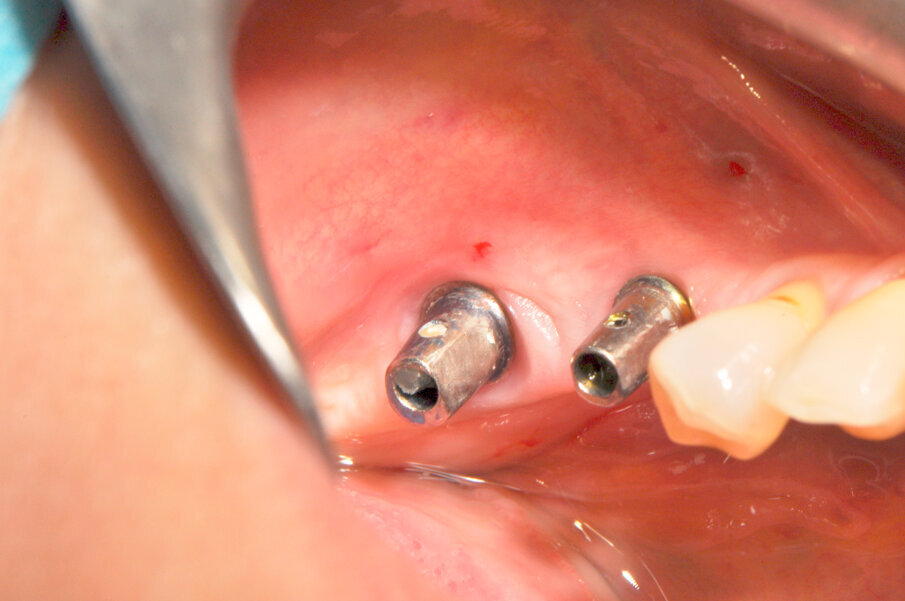
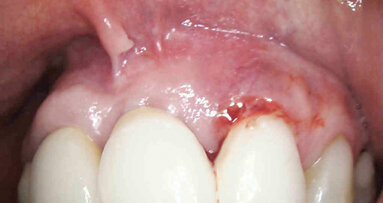
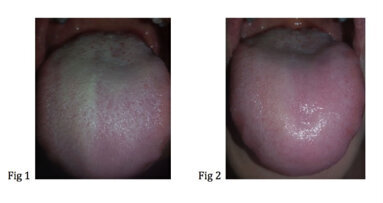
La paziente forniva il proprio consenso informato. La paziente è stata sottoposta 5 giorni prima dell’intervento a una igiene orale professionale al fine di risolvere la condizione infiammatoria relativa alla mucosa e predisporre la zona perimplantare all’intervento per la rigenerazione ossea, ottenendo uno stato ottimale dei tessuti molli, compatibilmente con la patologia in atto (Fig. 2). Si è prescritta una terapia antibiotica con amoxicillina/acido clavulanico (Augmentin, Glaxo-SmithKline, Verona, Italy) tre giorni prima della chirurgia ogni 12 ore e per i successivi 8-10 giorni. In seguito alla seduta di igiene pre-intervento, la paziente è stata anestetizzata localmente con articaina 1:100.000 per procedere alla fase chirurgica.
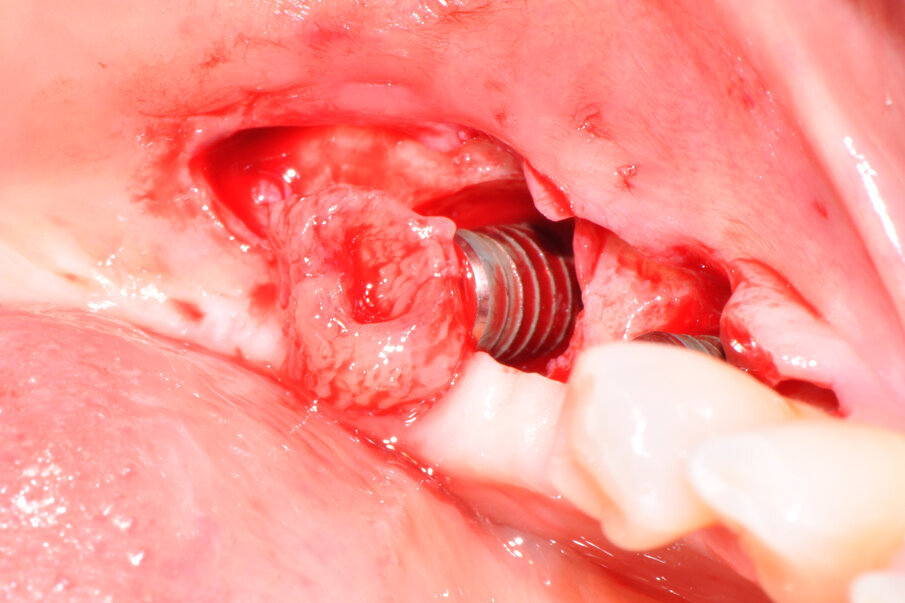
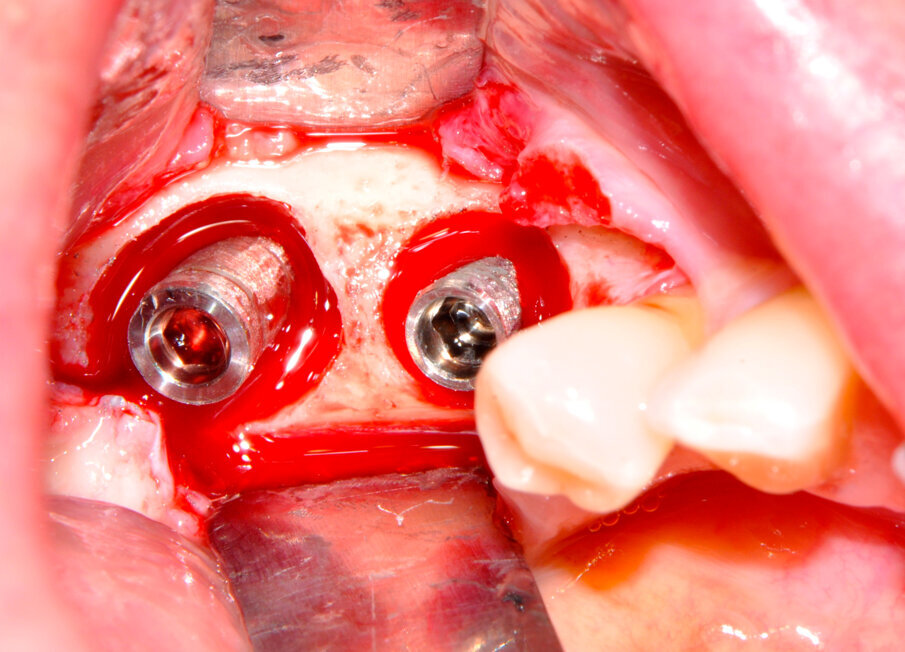
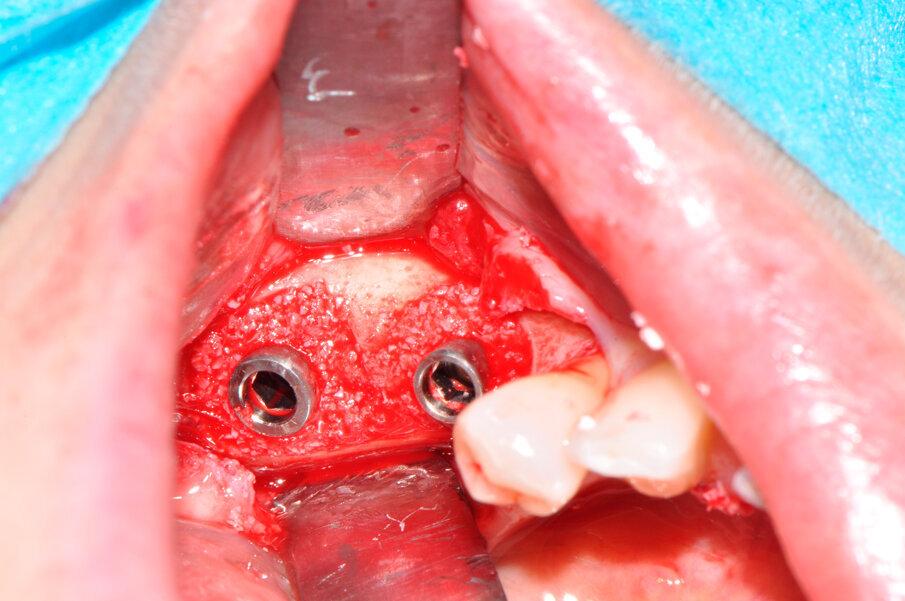
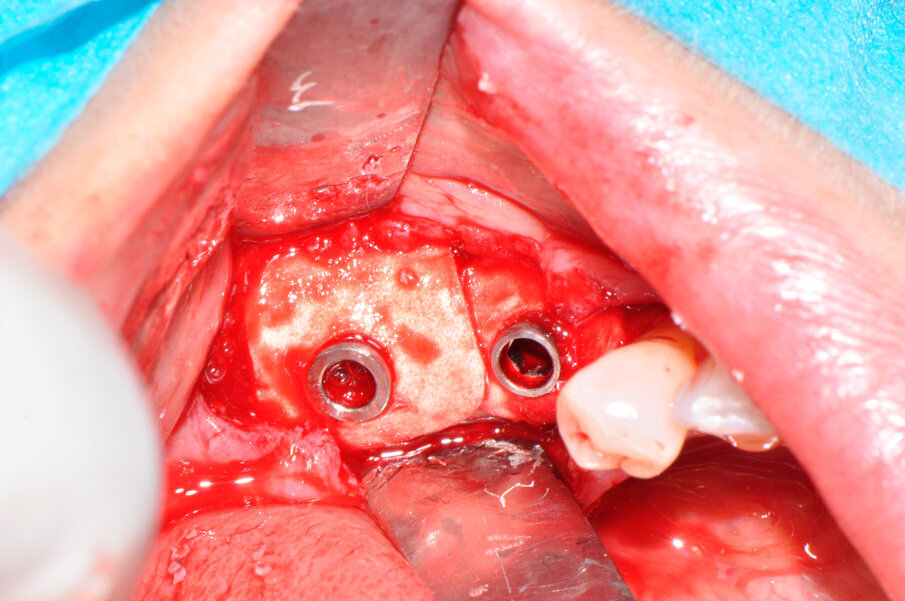
Il ponte cementato e i monconi implantari sono stati rimossi per procedere all’apertura del lembo mucoperiosteo ed esporre totalmente gli impianti e la superficie ossea; l’esame clinico confermava l’entità del riassorbimento osseo già osservata all’esame radiografico (Fig. 3). Una volta rimosso il tessuto granulomatoso sviluppatosi intorno agli impianti (Fig. 4), si è eseguito un debridement perimplantare con conseguente rimozione meccanica delle spire esposte. La superficie dell’impianto è stata ripulita con air polishing, polvere di glicina e lucidatura finale (Fig. 5). Il letto osseo perimplantare è stato cruentato per stimolare l’angiogenesi e l’integrazione con l’innesto. Il granulato, precedentemente idratato, è stato innestato nel difetto osseo a coprire le spire della superficie esposta di entrambi gli impianti fino a ripristinare il profilo osseo originale (Fig. 6).
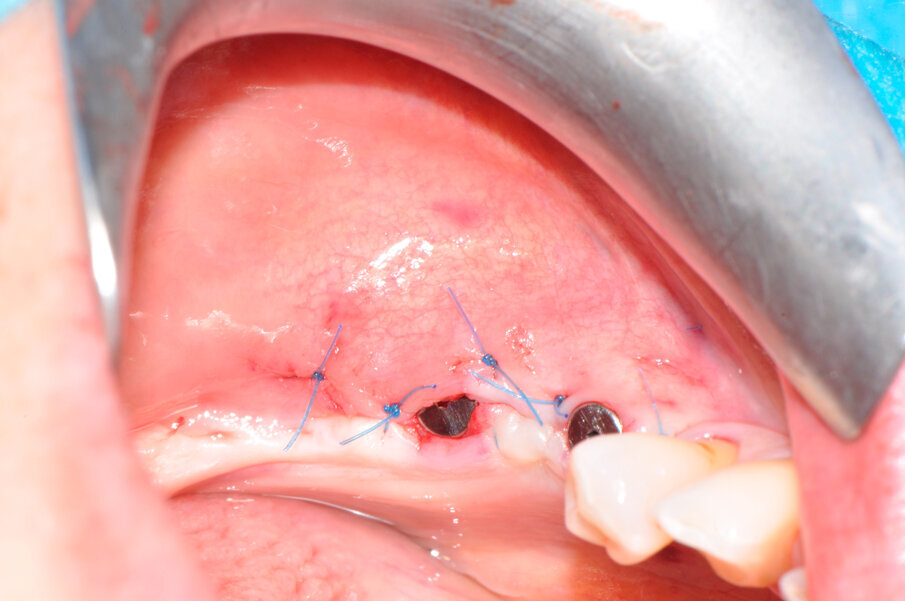
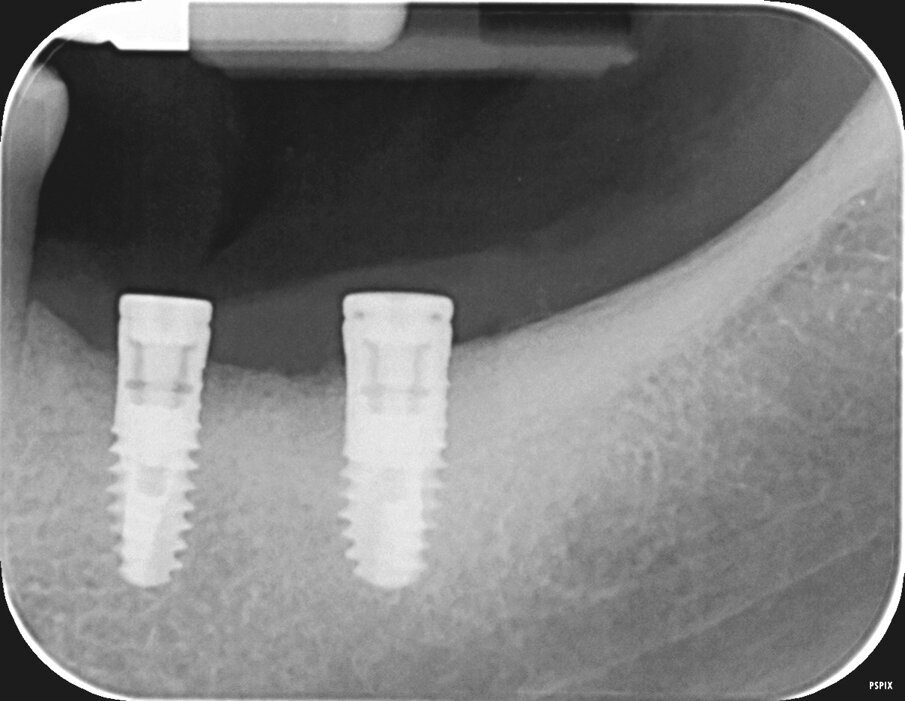
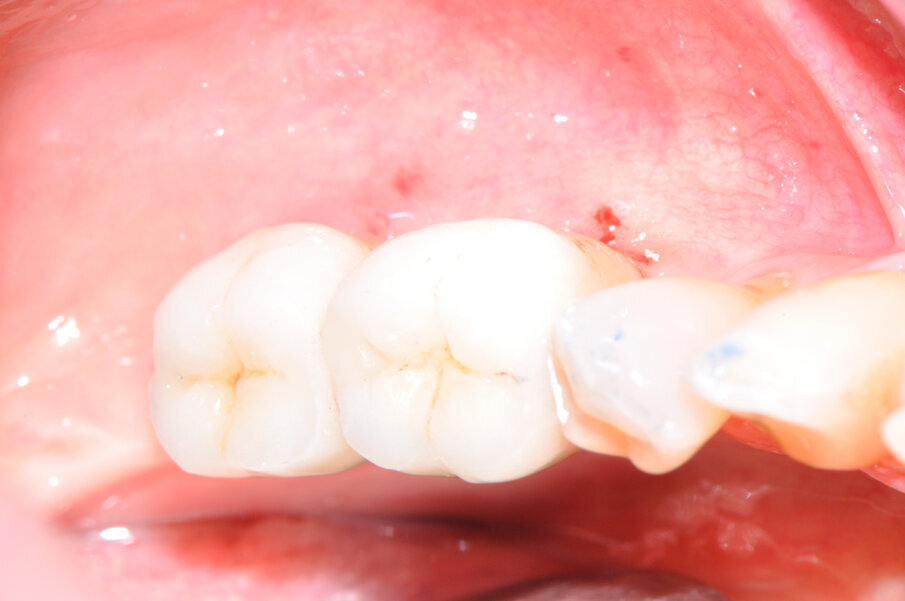
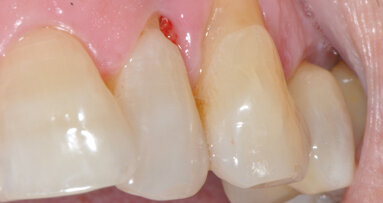
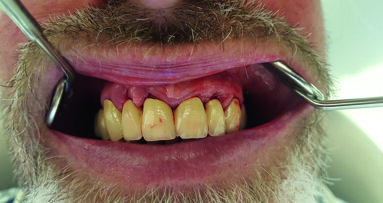
L’innesto è stato protetto con due membrane, opportunamente sagomate e forate per adattarsi attorno a ciascun impianto (Fig. 7). L’operazione è terminata con la sutura dei lembi gengivali tramite filo in poliammide non riassorbibile (Monomyd 4-0, Butterfly, Cavenago) e il posizionamento di due viti di guarigione (Fig. 8). La sutura è stata rimossa a 12 giorni dall’atto chirurgico. Una radiografia di controllo al termine dell’intervento ha confermato l’effettivo ripristino dei volumi ossei perimplantari (Fig. 9). Durante il periodo di guarigione e ai successivi controlli, non si sono osservati segni di sofferenza gengivale (Fig. 10). La paziente non ha lamentato alcuna sintomatologia spontanea o evocata. Al controllo a 3 mesi, l’esame radiografico mostrava il mantenimento dei profili ossei perimplantari (Fig. 11). Sono state quindi rimosse le viti di guarigione e riposizionate le corone.
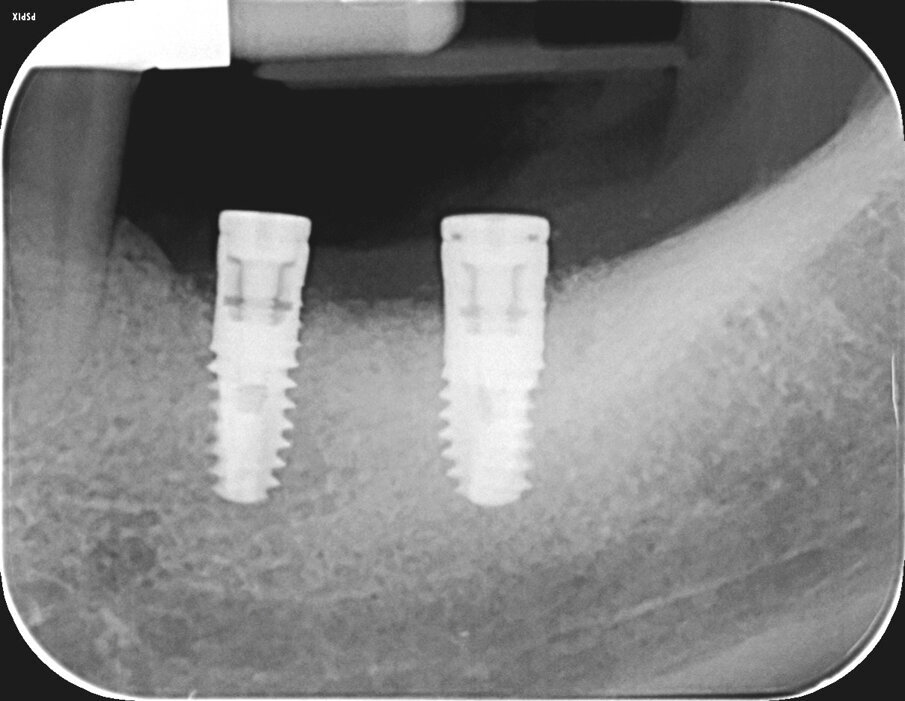
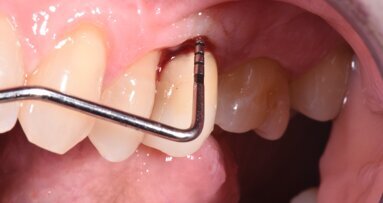
Al controllo a 15 mesi dall’intervento la paziente non lamenta alcuna sintomatologia e il sanguinamento durante le manovre di igiene orale è scomparso. Eseguita una rx endorale di controllo, si nota un mantenimento ottimale dei livelli ossei e una completa stabilità del contesto perimplantare (Fig. 12).
Fig. 1 - CBCT in sezione laterale. I coni di riassorbimento coinvolgono un’ampia porzione della superficie implantare.
Fig. 2 – Aspetto clinico delle mucose perimplantari al momento dell’atto chirurgico.
Fig. 3 - I due difetti perimplantari all’apertura del lembo.
Fig. 4 – Il tessuto granulomatoso rimosso che circondava gli impianti
Fig. 5 – L’aspetto della superficie implantare successivo alla rimozione delle spire e a lucidatura.
Fig. 6 - I due difetti perimplantari sono innestati col biomateriale a lento riassorbimento.
Fig. 7 - Le membrane in collagene sono posizionate attorno agli impianti dopo averle opportunamente forate.
Fig. 8 - La sutura al termine dell’intervento.
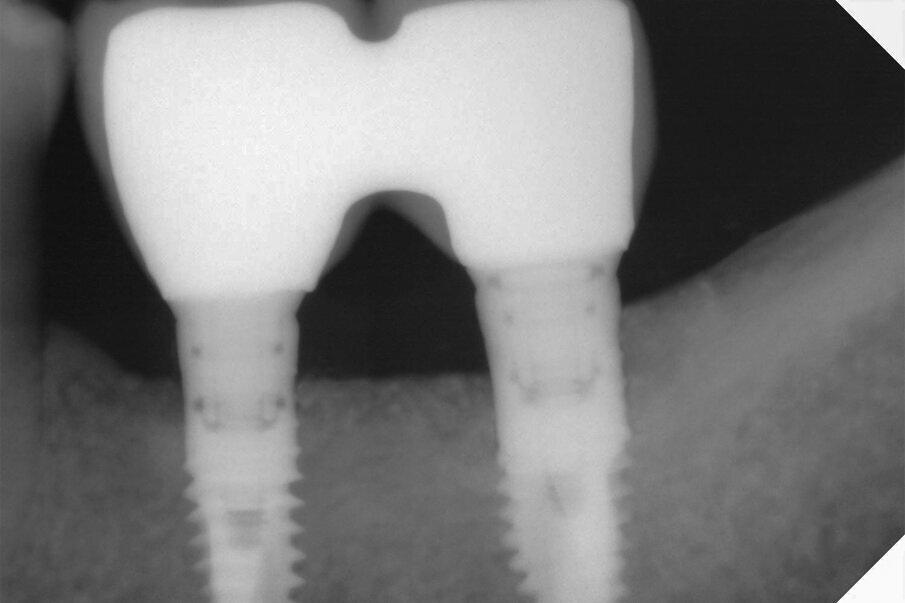
Fig. 9- Radiografia endorale di controllo al termine dell’intervento.
Fig. 10 - Controllo a 3 mesi, aspetto clinico della riabilitazione.
Fig. 11 - Controllo radiografico a 3 mesi, i livelli perimplantari sono mantenuti.
Fig. 12 - Controllo radiografico a 15 mesi, i livelli perimplantari sono mantenuti.
Conclusioni e discussione
La massima riduzione dello stato infettivo ed infiammatorio dei tessuti perimplantari è condizione necessaria per procedere all’intervento GBR. La strategia di pulizia perimplantare e disinfezione si è rivelata soddisfacente non avendo riscontrato recidive nel trascorso post-operatorio. La rigenerazione del tessuto osseo riassorbito è stata perseguita grazie all’utilizzo di un granulato osseo non antigenico a lento riassorbimento e al suo isolamento tramite una membrana di collagene riassorbibile in tempi brevi.
Entrambi i biomateriali sono di origine equina. Gli esami radiografici eseguiti al controllo a 3 e a 15 mesi dall’intervento e i sondaggi parodontali hanno permesso di osservare uno stato pressoché stabile del profilo osseo rigenerato, l’assenza di difetti e il mantenimento del sigillo perimplantare. In assenza di biopsie e analisi istologiche non è possibile determinare la frazione di osso endogeno di nuova formazione rispetto al sostituto osseo di origine equina, e determinare il grado di neo-osteointegrazione. Quando tali analisi sono state condotte in casi che hanno previsto l’uso di sostituti ossei trattati enzimaticamente, esse hanno evidenziato una sostituzione discretamente rapida (alcuni mesi) dell’innesto con tessuto osseo endogeno di nuova formazione, mimando così la cinetica del processo fisiologico di rimodellamento osseo.
Nonostante sia noto come il totale riassorbimento di innesti ossei bovini trattati termicamente possa richiedere anni8, la cinetica di sostituzione per la formulazione equina adottata in questo caso studio deve tuttora essere determinata. In particolare, sarà interessante seguire il follow-up a lungo termine per determinare l’eventuale mantenimento del profilo osseo e il perdurare del sostegno al tessuto gengivale. Nonostante la membrana in collagene offra una barriera limitata nel tempo rispetto a membrane a più lunga permanenza, anche se riassorbibili (quali, ad esempio, quelle di pericardio equino) non sono emerse problematiche relative all’infiltrazione di cellule connettivali. Si ipotizza che la membrana non solo svolga un ruolo passivo di sigillo dell’innesto e mantenimento del profilo osseo alveolare, ma offra uno scaffold per la colonizzazione da parte di precursori cellulari e il rilascio di fattori che promuovano l’osteogenesi e il rimodellamento dell’innesto14.
Al contrario delle membrane non riassorbibili (ad es., politetrafluoroetilene espanso), l’uso di una membrana in collagene idrolizzabile ha evitato di eseguire un nuovo intervento per la rimozione della stessa e di disturbare il processo rigenerativo osseo. Ancora oggi, la letteratura clinica non offre precise indicazioni sui materiali da preferire nelle procedure di GBR nel trattamento dei difetti perimplantari, e rimane aperto il quesito se sostituti ossei a lento riassorbimento debbano essere preferiti a innesti a rimodellamento fisiologico, secondo il razionale di un più efficace mantenimento nel tempo dei profili ossei, o se i secondi debbano essere preferiti ai primi per la loro potenzialità di realizzare una reale restitutio ad integrum dell’osso alveolare.
Bibliografia
- Tamura N., Ochi M., Miyakawa H. & Nakazawa F. Analysis of bacterial flora associated with peri-implantitis using obligate anaerobic culture technique and 16S rDNA gene sequence. Int. J. Oral Maxillofac. Implants 28, 1521–1529 (2013).
- Smeets R. et al. Definition, etiology, prevention and treatment of peri-implantitis – a review. Head Face Med. 10, (2014).
- Petkovic´ A. B. et al. Proinflammatory cytokines (IL-1β and TNF-α) and chemokines (IL-8 and MIP-1α) as markers of peri-implant tissue condition. Int. J. Oral Maxillofac. Surg. 39, 478–485 (2010).
- Schminke B. et al. The Pathology of Bone Tissue during Peri-Implantitis. J. Dent. Res. 94, 354–361 (2015).
- Shuto T., Wachi T., Shinohara Y., Nikawa H. & Makihira S. Increase in receptor activator of nuclear factor κB ligand/osteoprotegerin ratio in peri-implant gingiva exposed to Porphyromonas gingivalis lipopolysaccharide. J. Dent. Sci. 11, 8–16 (2016).
- Larsson L. et al. Regenerative Medicine for Periodontal and Peri-implant Diseases. J. Dent. Res. 95, 255–266 (2016).
- Benic G. I. et al. Guided bone regeneration of peri-implant defects with particulated and block xenogenic bone substitutes. Clin. Oral Implants Res. 27, 567–576 (2016).
- Di Stefano D. A. et al. Treatment of a bone defect consequent to the removal of a periapical cyst with equine bone and equine membranes: clinical and histological outcome. MINERVA Stomatol. 61, 15 (2012).
- Materni A. Managing an extreme periimplantitis: a case report. MINERVA Stomatol. 62, 295–305 (2013).
- Schwarz F., Sculean A., Bieling K., Ferrari D., Rothamel D., Becker J. Two-year clinical results following treatment of peri-implantitis lesions using a nanocrystalline hydroxyapatite or a natural bone mineral in combination with a collagen membrane. J Clin Periodontol. 2008 Jan;35(1):80-7.
- Esposito M., Grusovin MG., Worthington HV. Interventions for replacing missing teeth: treatment of peri-implantitis. Cochrane Database Syst Rev. 2012 Jan 18;1:CD004970.
- Sahrmann P., Attin T., Schmidlin PR. Regenerative treatment of peri-implantitis using bone substitutes and membrane: a systematic review. Clin Implant Dent Relat Res. 2011 Mar;13(1):46-57.
- Steven-Howe M., Richards D. Surgical regenerative treatment of periimplantitis. Evid Based Dent. 2017 Oct 27;18(3):79-81.
- Elgali I., Omar O., Dahlin C. & Thomsen P. Guided bone regeneration: materials and biological mechanisms revisited. Eur. J. Oral Sci. 125, 315–337 (2017).
Tag:
Il caso illustrato presenta i risultati clinici, radiografici e istomorfometrici ottenuti impiegando un sostituto osseo equino, trattato ad alta ...
Il presente lavoro descrive la procedura con laser neodimio Nd:YAG 1064 nm per intervento di perimplantite.
La parodontite aggressiva è stata definita come un tipo specifico di parodontite nel 1999, durante l’International Workshop, ed è stata ...
La rigenerazione ossea con tecnica GBR è uno strumento indispensabile per quanti si occupano di implantologia, al fine di garantire una ...
La perimplantite è una condizione patologica dei tessuti che circondano l’impianto dentale, caratterizzata dall’infiammazione del tessuto connettivo ...
La lingua villosa (LV) è una condizione benigna caratterizzata da un’alterazione di colore e da un aspetto villoso del dorso linguale. La prevalenza di ...
Gli impianti dentali rappresentano una delle opzioni più efficaci per il trattamento dell’edentulia, parziale o totale, consentendo la riabilitazione ...
L’obiettivo fondamentale per un trattamento di successo nella cura di parodontiti e perimplantiti non dovrebbe essere solo la rimozione del processo ...
Il trattamento delle seconde classi in età adolescenziale è un’eventualità tra le più frequenti nella clinica ortodontica. La terapia della ...
SILVER SPRING (USA) - La Food and Drug Administration (FDA) ha emesso una norma, entrata in vigore il 18 gennaio, per vietare l'uso della maggior parte dei ...
Live webinar
gio. 23 aprile 2026
17:00 (CET) Rome
Live webinar
gio. 23 aprile 2026
18:30 (CET) Rome
Live webinar
gio. 23 aprile 2026
19:00 (CET) Rome
Live webinar
gio. 30 aprile 2026
1:00 (CET) Rome
Dr. Renato Leonardo D.M.D.
Live webinar
gio. 30 aprile 2026
19:00 (CET) Rome
Live webinar
dom. 3 maggio 2026
18:00 (CET) Rome
Dr. Rickard Brånemark MSc, MD, PhD, Dr. Robert Gottlander DDS
Live webinar
lun. 4 maggio 2026
2:00 (CET) Rome



 Austria / Österreich
Austria / Österreich
 Bosnia ed Erzegovina / Босна и Херцеговина
Bosnia ed Erzegovina / Босна и Херцеговина
 Bulgaria / България
Bulgaria / България
 Croazia / Hrvatska
Croazia / Hrvatska
 Repubblica Ceca e Slovacchia / Česká republika & Slovensko
Repubblica Ceca e Slovacchia / Česká republika & Slovensko
 Francia / France
Francia / France
 Germania / Deutschland
Germania / Deutschland
 Grecia / ΕΛΛΑΔΑ
Grecia / ΕΛΛΑΔΑ
 Ungheria / Hungary
Ungheria / Hungary
 Italia / Italia
Italia / Italia
 Paesi Bassi / Nederland
Paesi Bassi / Nederland
 nordisch / Nordic
nordisch / Nordic
 Polonia / Polska
Polonia / Polska
 Portogallo / Portugal
Portogallo / Portugal
 Romania e Moldavia / România & Moldova
Romania e Moldavia / România & Moldova
 Slovenia / Slovenija
Slovenia / Slovenija
 Serbia e Montenegro / Србија и Црна Гора
Serbia e Montenegro / Србија и Црна Гора
 Spagna / España
Spagna / España
 Svizzera / Schweiz
Svizzera / Schweiz
 Turchia / Türkiye
Turchia / Türkiye
 Gran Bretagna e Irlanda / UK & Ireland
Gran Bretagna e Irlanda / UK & Ireland
 Internazionale / International
Internazionale / International
 Brasile / Brasil
Brasile / Brasil
 Canada / Canada
Canada / Canada
 America Latina / Latinoamérica
America Latina / Latinoamérica
 USA / USA
USA / USA
 Cina / 中国
Cina / 中国
 India / भारत गणराज्य
India / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
 Medio Oriente / Middle East
Medio Oriente / Middle East



















































To post a reply please login or register