Le classificazioni dell’atrofia ossea, basate sull’analisi solo anatomica del difetto in termini di profilo della cresta residua, presentano alcune limitazioni qualora esse vogliano essere impiegate come strumento predittivo del successo degli interventi di incremento dei volumi ossei.
Esse, infatti, considerano solo un sottoinsieme dei possibili difetti, non tengono conto della situazione orale complessiva e, soprattutto, non aiutano il clinico a focalizzare la propria attenzione sulle caratteristiche biologiche del difetto: quelle che, di fatto, condizioneranno effettivamente la riuscita – biologica e clinica – dell’atto rigenerativo. La classificazione anatomica dovrà essere integrata, invece, da un’analisi più fine di caratteristiche del difetto che maggiormente hanno impatto sulla probabilità di riuscita dell’evento rigenerativo e sulla sua cinetica quali, ad esempio, il numero di pareti ossee circostanti il difetto, se questo è esterno o interno al profilo crestale, l’estensione e la direzione dell’incremento desiderato, il grado di corticalizzazione del sito ricevente nonché la quantità e qualità della componente trabecolare eventualmente presente. Per potere definire la prevedibilità biologica dell’atto rigenerativo è necessario comprendere inoltre quali sono le modalità di interazione dell’innesto osseo prescelto con il tessuto ricevente già a livello cellulare.
Le componenti cellulari ossee coinvolte sono le cellule osteoblastiche e osteoclastiche nei loro diversi stadi di differenziamento. La loro interazione con l’innesto può essere diversa al variare della tipologia di materiale impiegato già in termini di adesione cellulare, evento necessario all’accadere di tutti i processi a valle che sottendono la rigenerazione ossea. L’adesione cellulare è infatti mediata da specifiche proteine di membrana (le integrine), che riconoscono altrettanto specifici segnali molecolari presenti sulla superficie del materiale innestato. Tra questi, particolare rilievo giocano specifiche sequenze amminoacidiche presenti nel collagene osseo. Il riconoscimento integrina-sequenza amminoacidica è lo specifico segnale che promuove l’adesione cellulare. Risulta chiaro, quindi, che innesti ossei privi di collagene – quali ad esempio gli innesti eterologhi resi non antigenici per via termica – non presentano condizioni altrettanto favorevoli all’adesione cellulare di innesti che, invece, conservano inalterato il collagene nativo grazie a processi differenti di fabbricazione. La conseguenza a livello istologico e, quindi, clinico è una differenza significativa nei tempi di rimodellamento ovvero, di degradazione e contemporanea sostituzione dell’innesto con tessuto osseo di nuova formazione: gli innesti a collagene osseo preservato integrato si rimodellano in tempi sostanzialmente fisiologici, laddove quelli nei quali il collagene osseo non è presente, o è presente in forma denaturata, tendono a permanere in situ più a lungo. Da un punto di vista terminologico, quindi, appare più corretto definire i primi “sostituti ossei”, vista la loro interazione quasi fisiologica con l’ambiente osseo, e i secondi invece “biomateriali”. Le ricerche immunoistochimiche danno specifica evidenza di quanto detto: gli studi eseguiti in collaborazione con l’Università di Chieti mostrano che l’espressione dei fattori di crescita tipici dell’angiogenesi (uno dei primi eventi della rigenerazione ossea) non è dissimile quando le due tipologie di materiale sono innestate in ambito clinico; tuttavia, l’adesione osteoclastica (ovvero, delle cellule deputate alla degradazione degli innesti), risulta significativamente diversa nei due casi.
Come scegliere il miglior innesto osseo?
La scelta dell’innesto ottimale per un dato intervento rigenerativo è frutto di un’attenta comprensione sia delle caratteristiche anatomo-biologiche del sito ricevente, sia delle caratteristiche dei diversi innesti disponibili, sia delle finalità ultime dell’intervento: in sintesi, qualora si voglia ottenere tessuto osseo di nuova formazione al fine di un contestuale o differito inserimento implantare si preferirà il sostituto osseo eterologo a collagene preservato (nei casi, si intende, ove l’innesto autologo non sia comunque la scelta elettiva);
dove invece si vorrà preservare un volume osseo, a fini estetici o di successivo inserimento implantare non prevedibile nel tempo, si preferirà un innesto a lunga permanenza, quali quelli ottenibili processando il tessuto osseo eterologo attraverso trattamento termico ad alta temperatura. La scelta dell’innesto osseo adeguato potrà coinvolgere anche il formato dello stesso. In questo senso, i sostituti ossei eterologhi a collagene preservato permettono l’impiego di formati differenti dall’usuale granulo quali, ad esempio, blocchi rigidi o lamine flessibili. Questi possono trovare impiego – con precisi limiti dettati, nuovamente, dal potenziale rigenerativo del sito oggetto di innesto – negli incrementi verticali e orizzontali, purché eseguiti come vere e proprie GBR, utilizzando membrane appropriate e non semplicemente mimando i classici onlay con innesti autologhi. Ulteriormente, l’impiego di lamine ossee eterologhe può trovare un preciso significato clinico nella gestione di alcune complicanze del rialzo di seno mascellare (lacerazioni della membrana sinusale) o, nel caso di impiego di lamine corticali di ridotto spessore, come membrane riassorbibili a lunga permanenza.
embedImagecenter("Imagecenter_1_2244",2244, "large");
Gli ultimi aggiornamenti dalla ricerca clinica
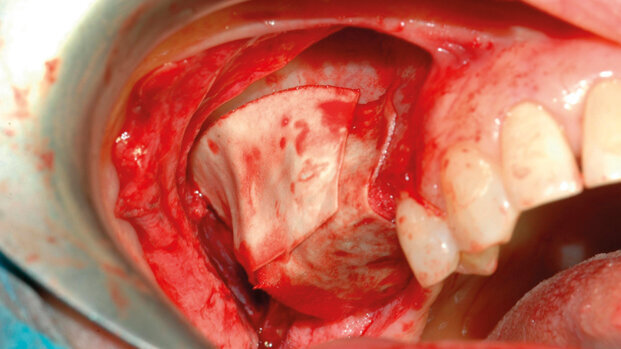
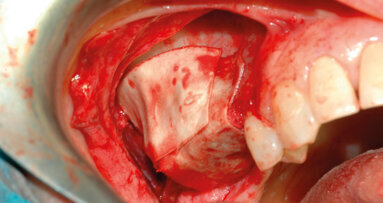
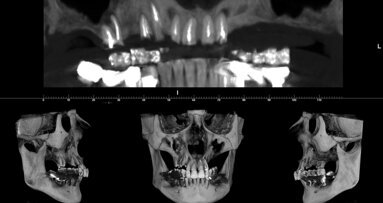
Le ricerche attuali, eseguite in collaborazione con la clinica odontoiatrica dell’Ospedale San Raffaele, Università Vita e Salute, si concentrano sul comportamento istologico dei diversi innesti in una condizione clinica modello quale è il rialzo di seno mascellare (Figg. 1a, 1b). La diversa interazione cellulare mostrata dagli innesti eterologhi a collagene preservato rispetto a quelli trattati per via termica suggerisce che sia possibile osservare differenze significative nel loro rimodellamento qualora essi siano utilizzati in ambito clinico. Di fatto, uno studio clinico randomizzato in cui pazienti con atrofia ossea del mascellare superiore sono stati riabilitati previa esecuzione di rialzo di seno con i due diversi innesti ha mostrato che, a distanza di sei mesi dall’innesto (Figg. 2a, 2b), il sostituto osseo a collagene preservato permette la formazione di una quantità significativamente maggiore di tessuto osseo (46.86% ± 12.81% rispetto 25.12% ± 7.25%) e, simmetricamente, che la quantità di innesto residuo è significativamente minore (11.05% ± 9.27%. rispetto 28.65% ± 9.70%). Il follow-up clinico a tre anni non mostrava differenze significative tra i due innesti.
Si è quindi verificata con uno studio istomorfometrico retrospettivo (Figg. 3a, 3b) l’ipotesi che il sostituto osseo a collagene preservato possa indurre la formazione di una quantità di tessuto osseo in grado di permettere il posizionamento implantare già a un tempo più precoce rispetto a quello che, tradizionalmente, si attende nel rialzo di seno eseguito in due tempi. L’ipotesi si è dimostrata vera, in quanto si è osservato che la quantità di tessuto osseo di nuova formazione osservabile a 3-5 mesi dalla chirurgia rigenerativa quando è utilizzato questo sostituto osseo non è significativamente diverso rispetto a quelle osservabili a 6-8 mesi o a 9-12 mesi dall’innesto stesso. Inoltre, a distanza di 3 anni la percentuale di successo e sopravvivenza implantare non è significativamente differente nelle tre classi temporali; è possibile quindi, utilizzando questa tipologia di innesti, procedere all’inserimento implantare a tempi più brevi (3-5 mesi) rispetto a quelli che si attendono tradizionalmente.
In conclusione, la prevedibilità dell’aumento dei volumi ossei è definita da diversi fattori che devono essere oggetto di una attenta analisi razionale; questa deve muovere da considerazioni anatomico-biologiche, e dalla precisa conoscenza delle tipologie di innesto a disposizione ma non potrà poi esimersi dal considerare la tipologia di tessuto osseo che si desidera ottenere, il tempo in cui lo si vuole ottenere, il grado di predicibilità dell’intervento e – non ultimo e più importante – il fine ultimo dell’atto clinico che ci si appresta a compiere.
Bibliografia:
1. Di Stefano DA, Gastaldi G, Vinci R, Polizzi ME, Cinci L, Pieri L, Gherlone E. Bone formation following sinus augmentation with an equine-derived bone graft: a retrospective histological and histomorphometric study with 36- month follow-up. Accepted, Int J Oral Maxillofac Implants.
2. Di Stefano DA, Gastaldi G, Vinci R, Cinci L, Pieri L, Gherlone E. Histomorphometric Comparison of Enzyme- Deantigenic Equine Bone and Anorganic Bovine Bone in Sinus Augmentation: A Randomized Clinical Trial with 3- Year Follow-up. Int J Oral Maxillofac Implants. 2015 Sep-Oct;30(5):1161-7.
3. Di Stefano DA, Greco GB, Cinci L, Pieri L. Horizontal-guided Bone Regeneration using a Titanium Mesh and an Equine Bone Graft. J Contemp Dent Pract. 2015 Feb 1;16(2):154-62.
4. Di Stefano DA, Cazzaniga A, Andreasi Bassi M, Ludovichetti M, Ammirabile G, Celletti R. The use of cortical heterologous sheets for sinus lift bone grafting: a modification of Tulasne’s technique with 7-year follow-up. Int J Immunopathol Pharmacol. 2013 Apr-Jun;26(2):549-56.
5. Di Stefano DA, Andreasi Bassi M, Cinci L, Pieri L, Ammirabile G. Treatment of a bone defect consequent to the removal of a periapical cyst with equine bone and equine membranes: clinical and histological outcome. Minerva Stomatol. 2012 Nov-Dec;61(11-12):477-90.
6. Testori T, Drago L, Wallace SS, Capelli M, Galli F, Zuffetti F, Parenti A, Deflorian M, Fumagalli L, Weinstein RL, Maiorana C, Di Stefano D, Valentini P, Giannì AB, Chiapasco M, Vinci R, Pignataro L, Mantovani M, Torretta S, Pipolo C, Felisati G, Padoan G, Castelnuovo P, Mattina R, Del Fabbro M. Prevention and treatment of postoperative infections after sinus elevation surgery: clinical consensus and recommendations. Int J Dent. 2012;2012:365809.
7. Artese L, Piattelli A, Di Stefano DA, Piccirilli M, Pagnutti S, D’Alimonte E, Perrotti V. Sinus lift with autologous bone alone or in addition to equine bone: an immunohistochemical study in man. Implant Dent. 2011 Oct;20(5):383-8.
8. Ludovichetti M, Di Stefano DA, Pagnutti S, Vaccari E, Ludovichetti FS, Celletti R. Vertical ridge augmentation using a flexible heterologous cortical bone sheet: three-year follow-up. Int J Periodontics Restorative Dent. 2011 Jul- Aug;31(4):401-7.
9. Di Stefano DA, Artese L, Iezzi G, Piattelli A, Pagnutti S, Piccirilli M, Perrotti V. Alveolar ridge regeneration with equine spongy bone: a clinical, histological, and immunohistochemical case series. Clin Implant Dent Relat Res. 2009 Jun;11(2):90-100.
10. Chiapasco M, Casentini P, Zaniboni M. Bone augmentation procedures in implant dentistry. Int J Oral Maxillofac Implants. 2009;24 Suppl:237-59.
11. Chiapasco M, Zaniboni M, Boisco M. Augmentation procedures for the rehabilitation of deficient edentulous ridges with oral implants. Clin Oral Implants Res. 2006 Oct;17 Suppl 2:136-59.
12. Piattelli A, Degidi M, Di Stefano DA, Rubini C, Fioroni M, Strocchi R. Microvessel density in alveolar ridge regeneration with autologous and alloplastic bone. Implant Dent. 2002;11(4):370-5.
13. Tinti C, Parma-Benfenati S, Polizzi G. Vertical ridge augmentation: what is the limit? Int J Periodontics Restorative Dent. 1996 Jun; 16(3):220-9.
14. Jovanovic SA, Schenk RK, Orsini M, Kenney EB. Supracrestal bone formation around dental implants: an experimental dog study. Int J Oral Maxillofac Implants. 1995 Jan-Feb; 10(1):23-31.
15. Simion M, Trisi P, Piattelli A. Vertical ridge augmentation using a membrane technique associated with osseointegrated implants. Int J Periodontics Restorative Dent. 1994 Dec; 14(6):496-511.
16. Schenk RK, Buser D, Hardwick WR, Dahlin C. Healing pattern of bone regeneration in membrane-protected defects: a histologic study in the canine mandible. Int J Oral Maxillofac Implants.1994 Jan-Feb; 9(1):13-29.
L'articolo è stato pubblicato su Implant Tribune Italian Edition, marzo 2016.
Le classificazioni dell’atrofia ossea, basate sull’analisi solo anatomica del difetto in termini di profilo della cresta residua, presentano ...
Al XXVII Congresso di Monte Carlo dello scorso novembre 2015, Dental Tribune ha incontrato il professor Danilo Alessio Di Stefano (in foto), docente di ...
Al XXVII Congresso di Monte Carlo dello scorso novembre 2015, Dental Tribune ha incontrato il professor Danilo Alessio Di Stefano (in foto), docente di ...
Gli innesti ossei sono una procedura chirurgica che permette di ristabilire un volume osseo adeguato prima di una terapia implantare, utilizzando materiali ...
Il caso illustrato presenta i risultati clinici, radiografici e istomorfometrici ottenuti impiegando un sostituto osseo equino, trattato ad alta ...
Il successo di un trattamento implantare si basa sulla disponibilità di una sufficiente quantità e qualità ossea. Ecco perché ...
Il successo di un trattamento implantare si basa sulla disponibilità di una sufficiente quantità e qualità ossea. Ecco perché ...
SILVER SPRING - La Food and Drug Administration aggiorna le raccomandazioni circa l'uso di sostituti per innesto osseo contenenti proteine ricombinanti o ...
Gli innesti ossei sono una procedura chirurgica che permette di ristabilire un volume osseo adeguato prima di una terapia implantare, utilizzando materiali ...
La rigenerazione ossea guidata (GBR) è una tecnica di incremento osseo efficace e ben documentata. L’espressione “incremento osseo ...
Live webinar
mer. 3 giugno 2026
19:00 (CET) Rome
Live webinar
gio. 4 giugno 2026
20:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
18:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
19:00 (CET) Rome
Dr. Anthony Mak B.D.S, Prof. Marleen Peumans
Live webinar
lun. 8 giugno 2026
20:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
17:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
20:00 (CET) Rome
Nacho Fernández-Baca DDS, MSc



 Austria / Österreich
Austria / Österreich
 Bosnia ed Erzegovina / Босна и Херцеговина
Bosnia ed Erzegovina / Босна и Херцеговина
 Bulgaria / България
Bulgaria / България
 Croazia / Hrvatska
Croazia / Hrvatska
 Repubblica Ceca e Slovacchia / Česká republika & Slovensko
Repubblica Ceca e Slovacchia / Česká republika & Slovensko
 Francia / France
Francia / France
 Germania / Deutschland
Germania / Deutschland
 Grecia / ΕΛΛΑΔΑ
Grecia / ΕΛΛΑΔΑ
 Ungheria / Hungary
Ungheria / Hungary
 Italia / Italia
Italia / Italia
 Paesi Bassi / Nederland
Paesi Bassi / Nederland
 nordisch / Nordic
nordisch / Nordic
 Polonia / Polska
Polonia / Polska
 Portogallo / Portugal
Portogallo / Portugal
 Romania e Moldavia / România & Moldova
Romania e Moldavia / România & Moldova
 Slovenia / Slovenija
Slovenia / Slovenija
 Serbia e Montenegro / Србија и Црна Гора
Serbia e Montenegro / Србија и Црна Гора
 Spagna / España
Spagna / España
 Svizzera / Schweiz
Svizzera / Schweiz
 Turchia / Türkiye
Turchia / Türkiye
 Gran Bretagna e Irlanda / UK & Ireland
Gran Bretagna e Irlanda / UK & Ireland
 Internazionale / International
Internazionale / International
 Brasile / Brasil
Brasile / Brasil
 Canada / Canada
Canada / Canada
 America Latina / Latinoamérica
America Latina / Latinoamérica
 USA / USA
USA / USA
 Cina / 中国
Cina / 中国
 India / भारत गणराज्य
India / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
 Medio Oriente / Middle East
Medio Oriente / Middle East

















































To post a reply please login or register