Le classificazioni dell’atrofia ossea, basate sull’analisi solo anatomica del difetto in termini di profilo della cresta residua, presentano alcune limitazioni qualora esse vogliano essere impiegate come strumento predittivo del successo degli interventi di incremento dei volumi ossei.
Esse, infatti, considerano solo un sottoinsieme dei possibili difetti, non tengono conto della situazione orale complessiva e, soprattutto, non aiutano il clinico a focalizzare la propria attenzione sulle caratteristiche biologiche del difetto: quelle che, di fatto, condizioneranno effettivamente la riuscita – biologica e clinica – dell’atto rigenerativo. La classificazione anatomica dovrà essere integrata, invece, da un’analisi più fine di caratteristiche del difetto che maggiormente hanno impatto sulla probabilità di riuscita dell’evento rigenerativo e sulla sua cinetica quali, ad esempio, il numero di pareti ossee circostanti il difetto, se questo è esterno o interno al profilo crestale, l’estensione e la direzione dell’incremento desiderato, il grado di corticalizzazione del sito ricevente nonché la quantità e qualità della componente trabecolare eventualmente presente. Per potere definire la prevedibilità biologica dell’atto rigenerativo è necessario comprendere inoltre quali sono le modalità di interazione dell’innesto osseo prescelto con il tessuto ricevente già a livello cellulare.
Le componenti cellulari ossee coinvolte sono le cellule osteoblastiche e osteoclastiche nei loro diversi stadi di differenziamento. La loro interazione con l’innesto può essere diversa al variare della tipologia di materiale impiegato già in termini di adesione cellulare, evento necessario all’accadere di tutti i processi a valle che sottendono la rigenerazione ossea. L’adesione cellulare è infatti mediata da specifiche proteine di membrana (le integrine), che riconoscono altrettanto specifici segnali molecolari presenti sulla superficie del materiale innestato. Tra questi, particolare rilievo giocano specifiche sequenze amminoacidiche presenti nel collagene osseo. Il riconoscimento integrina-sequenza amminoacidica è lo specifico segnale che promuove l’adesione cellulare. Risulta chiaro, quindi, che innesti ossei privi di collagene – quali ad esempio gli innesti eterologhi resi non antigenici per via termica – non presentano condizioni altrettanto favorevoli all’adesione cellulare di innesti che, invece, conservano inalterato il collagene nativo grazie a processi differenti di fabbricazione. La conseguenza a livello istologico e, quindi, clinico è una differenza significativa nei tempi di rimodellamento ovvero, di degradazione e contemporanea sostituzione dell’innesto con tessuto osseo di nuova formazione: gli innesti a collagene osseo preservato integrato si rimodellano in tempi sostanzialmente fisiologici, laddove quelli nei quali il collagene osseo non è presente, o è presente in forma denaturata, tendono a permanere in situ più a lungo. Da un punto di vista terminologico, quindi, appare più corretto definire i primi “sostituti ossei”, vista la loro interazione quasi fisiologica con l’ambiente osseo, e i secondi invece “biomateriali”. Le ricerche immunoistochimiche danno specifica evidenza di quanto detto: gli studi eseguiti in collaborazione con l’Università di Chieti mostrano che l’espressione dei fattori di crescita tipici dell’angiogenesi (uno dei primi eventi della rigenerazione ossea) non è dissimile quando le due tipologie di materiale sono innestate in ambito clinico; tuttavia, l’adesione osteoclastica (ovvero, delle cellule deputate alla degradazione degli innesti), risulta significativamente diversa nei due casi.
Leggi l'articolo completo nella sezione CLINICA > IMPLANTOLOGY
Le classificazioni dell’atrofia ossea, basate sull’analisi solo anatomica del difetto in termini di profilo della cresta residua, presentano ...
Al XXVII Congresso di Monte Carlo dello scorso novembre 2015, Dental Tribune ha incontrato il professor Danilo Alessio Di Stefano (in foto), docente di ...
Al XXVII Congresso di Monte Carlo dello scorso novembre 2015, Dental Tribune ha incontrato il professor Danilo Alessio Di Stefano (in foto), docente di ...
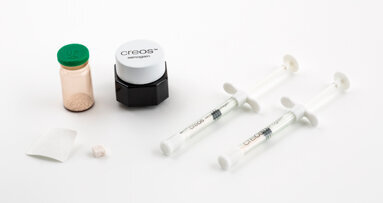
Gli innesti ossei sono una procedura chirurgica che permette di ristabilire un volume osseo adeguato prima di una terapia implantare, utilizzando materiali ...
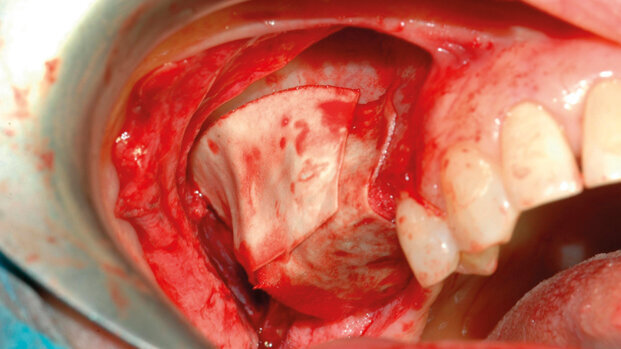
Il caso illustrato presenta i risultati clinici, radiografici e istomorfometrici ottenuti impiegando un sostituto osseo equino, trattato ad alta ...
Il successo di un trattamento implantare si basa sulla disponibilità di una sufficiente quantità e qualità ossea. Ecco perché ...
Il successo di un trattamento implantare si basa sulla disponibilità di una sufficiente quantità e qualità ossea. Ecco perché ...
SILVER SPRING - La Food and Drug Administration aggiorna le raccomandazioni circa l'uso di sostituti per innesto osseo contenenti proteine ricombinanti o ...
Gli innesti ossei sono una procedura chirurgica che permette di ristabilire un volume osseo adeguato prima di una terapia implantare, utilizzando materiali ...
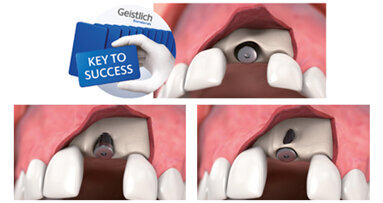
La rigenerazione ossea guidata (GBR) è una tecnica di incremento osseo efficace e ben documentata. L’espressione “incremento osseo ...
Live webinar
mer. 22 aprile 2026
17:00 (CET) Rome
MDT Andreas Chatzimpatzakis
Live webinar
mer. 22 aprile 2026
17:00 (CET) Rome
Live webinar
mer. 22 aprile 2026
18:00 (CET) Rome
Live webinar
gio. 23 aprile 2026
17:00 (CET) Rome
Live webinar
gio. 23 aprile 2026
18:30 (CET) Rome
Live webinar
gio. 23 aprile 2026
19:00 (CET) Rome
Live webinar
gio. 30 aprile 2026
1:00 (CET) Rome
Dr. Renato Leonardo D.M.D.



 Austria / Österreich
Austria / Österreich
 Bosnia ed Erzegovina / Босна и Херцеговина
Bosnia ed Erzegovina / Босна и Херцеговина
 Bulgaria / България
Bulgaria / България
 Croazia / Hrvatska
Croazia / Hrvatska
 Repubblica Ceca e Slovacchia / Česká republika & Slovensko
Repubblica Ceca e Slovacchia / Česká republika & Slovensko
 Francia / France
Francia / France
 Germania / Deutschland
Germania / Deutschland
 Grecia / ΕΛΛΑΔΑ
Grecia / ΕΛΛΑΔΑ
 Ungheria / Hungary
Ungheria / Hungary
 Italia / Italia
Italia / Italia
 Paesi Bassi / Nederland
Paesi Bassi / Nederland
 nordisch / Nordic
nordisch / Nordic
 Polonia / Polska
Polonia / Polska
 Portogallo / Portugal
Portogallo / Portugal
 Romania e Moldavia / România & Moldova
Romania e Moldavia / România & Moldova
 Slovenia / Slovenija
Slovenia / Slovenija
 Serbia e Montenegro / Србија и Црна Гора
Serbia e Montenegro / Србија и Црна Гора
 Spagna / España
Spagna / España
 Svizzera / Schweiz
Svizzera / Schweiz
 Turchia / Türkiye
Turchia / Türkiye
 Gran Bretagna e Irlanda / UK & Ireland
Gran Bretagna e Irlanda / UK & Ireland
 Internazionale / International
Internazionale / International
 Brasile / Brasil
Brasile / Brasil
 Canada / Canada
Canada / Canada
 America Latina / Latinoamérica
America Latina / Latinoamérica
 USA / USA
USA / USA
 Cina / 中国
Cina / 中国
 India / भारत गणराज्य
India / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
 Medio Oriente / Middle East
Medio Oriente / Middle East



















































To post a reply please login or register