L’articolo presenta una case series (10 casi clinici) di trattamento non chirurgico di tasche parodontali. In tutti i casi è stato applicato un nuovo hydrogel collagenico (H42, Bioteck Spa, Arcugnano – Vicenza) in seguito al debridement e alla levigatura radicolare degli elementi coinvolti mediante l’impiego di inserti a ultrasuoni dedicati e curette manuali.
I 10 pazienti trattati non avevano patologie sistemiche e avevano i seguenti parametri parodontali: una profondità di tasca (PPD) media di 7.4±1.2 mm, un indice di placca (PI) medio di 1.7±1 e un CAL di 7.8±1.4 mm. A seguito del debridement meccanico, il sito veniva mantenuto asciutto durante l’applicazione dell’hydrogel, il quale veniva estruso direttamente dalla siringa attraverso opportuno ago, partendo dal fondo della tasca e riempiendola fino a colmare il difetto. A questo punto il sito veniva mantenuto asciutto per 5 minuti mediante l’utilizzo di un aspiratore chirurgico e il paziente veniva dimesso senza limitazioni nell’igiene orale e nell’alimentazione. I pazienti così trattati hanno mostrato un’accelerazione nella guarigione dei tessuti gengivali e una riduzione dell’infiammazione tessutale, già a 7 giorni. Il follow-up a 90 giorni ha evidenziato un miglioramento di tutti i parametri parodontali, con una diminuzione della PPD di circa 4 mm, il PI ridotto a 1.2 e una diminuzione di circa 2.5 mm del CAL.
Introduzione
La parodontite è una malattia cronica multifattoriale infiammatoria che colpisce circa 150 milioni di persone in Europa1. La sua causa scatenante va ricercata nell’accumulo di biofilm batterico, che, insieme al perdurare della risposta immunitaria dell’organismo porta al progressivo distacco dell’epitelio gengivale dall’elemento dentale2, 3. Ciò determina la formazione di tasche parodontali e il successivo danneggiamento dell’osso alveolare, condizione che, se non opportunamente trattata, può portare alla perdita degli elementi dentari interessati4.
Per prevenire e arrestare la progressione della malattia parodontale, il primo passo è quello di un trattamento non chirurgico mediante levigatura radicolare per eliminare i batteri e la placca formata. Tale procedura è considerata il gold standard della terapia non-chirurgica della parodontite5 e favorisce la guarigione della tasca.
Tuttavia, è comune osservare una recrudescenza dell’infezione e quindi la necessità di un ulteriore trattamento. Ciò ha portato all’utilizzo di prodotti adiuvanti da applicare successivamente al debridement meccanico, come antibiotici e sostanze battericide. Sebbene tali procedure si siano dimostrate superiori al solo trattamento meccanico, nel caso degli antibiotici vi è un problema legato allo sviluppo di batteri antibiotico-resistenti e ai possibili effetti collaterali; riguardo invece le sostanze battericide, come la clorexidina, è necessario sottolineare che possono avere effetti negativi anche sulla flora batterica orale e creare dunque una disbiosi che può favorire l’insorgenza di malattie dentali6. Oggetto del presente articolo è una valutazione dei risultati clinici ottenuti su 10 pazienti a seguito dell’impiego di un nuovo hydrogel collagenico come coadiuvante del trattamento meccanico delle tasche parodontali al fine di impedire la ricolonizzazione batterica e favorire la guarigione dei tessuti.
Casi clinici
I 10 pazienti non avevano patologie sistemiche ed erano affetti da parodontite, con una severità compresa tra grado II e grado IV. 9 tasche parodontali erano di tipo intraosseo, mentre una tasca era associata a lesione endoparodontale. I parametri parodontali iniziali erano: profondità di tasca (PPD) = 7.4±1.2 mm, livello di attacco clinico (CAL) = 7.8±1.4 mm e indice di placca (PI) = 1.7±1. I tessuti dei siti trattati sono stati valutati per l’infiammazione con una scala da 1 a 4, così suddivisa: 1 (molto infiammato), 2 (mediamente infiammato), 3 (infiammazione lieve), 4 (tessuto non infiammato). Alla prima visita il livello di infiammazione era così distribuito: 4 pazienti presentavano un grado di infiammazione elevato, 3 pazienti un grado medio, 2 pazienti un grado lieve e 1 paziente non presentava infiammazione.
Il dolore percepito dal paziente è stato misurato tramite scala NRS (scala da 1-10) e alla prima visita era in media di 3.9 ± 2.4. Ai controlli si è effettuata una valutazione dello stato di guarigione dei tessuti molli attraverso l’impiego di una scala da 1 a 4 così suddivisa: 1 (nessuna guarigione), 2 (strato di fibrina visibile), 3 (guarigione avanzata), 4 (tessuto guarito).
Tutti i pazienti sono stati inizialmente sottoposti a scaling sottogengivale e levigatura radicolare mediante l’impiego di inserti ad ultrasuoni dedicati e curette manuali. In seguito, le tasche sono state riempite con un nuovo hydrogel collagenico in siringa (H42, Bioteck Spa, Arcugnano - Vicenza) (Fig. 1) costituito da collagene di tipo I, polimeri ad alto peso molecolare e quantità ancillari di vitamina C per l’ottimizzazione della reologia. Il prodotto è stato estruso mediante l’impiego di aghi smussi per irrigazione di tasche parodontali con Gauge compreso tra 20 e 25, a partire dal fondo della tasca parodontale, fino a colmarla completamente (Fig. 2). Durante l’estrusione del prodotto e per i successivi 5 minuti (tempo di “setting”), il sito è stato mantenuto asciutto mediante l’impiego di aspiratore chirurgico. In questo periodo di tempo il prodotto diventa più colloso, pur mantenendo un aspetto liquido, tale per cui viene ottimizzata l’adesione ai tessuti connettivali. Nei giorni successivi al trattamento, i pazienti non hanno dovuto osservare particolari accorgimenti nell’igiene dentale e nell’alimentazione.
I controlli qualitativi (livello di infiammazione, livello di guarigione tessuti e dolore) sono stati fatti settimanalmente per il primo mese e poi a 3 mesi. Le misurazioni parodontali sono state effettuate ai controlli a 30 e 90 giorni. A 7 giorni di follow-up, il grado di infiammazione era sceso: 4 pazienti erano privi di infiammazione, 5 pazienti avevano un grado lieve di infiammazione e solo uno aveva un grado di infiammazione medio. 7 pazienti presentavano un livello di guarigione avanzata dei tessuti mentre per 3 pazienti i tessuti si presentavano completamente guariti. Il dolore era quasi assente per tutti i pazienti (NRS medio 1.7 ± 1.3).
Il successivo follow-up a 14 giorni mostrava un’ulteriore riduzione dell’infiammazione, con 8 pazienti privi di infiammazione e 2 pazienti con infiammazione lieve. Anche la guarigione dei tessuti mostrava un ulteriore miglioramento: 5 pazienti erano in fase di guarigione avanzata e 5 erano del tutto guariti. Allo stesso modo il dolore scompariva completamente in tutti i pazienti (NRS 1).
Il follow-up a 30 giorni mostrava che i tessuti di tutti i pazienti erano guariti e privi di infiammazione. Anche i parametri parodontali erano migliorati: PPD a 4.8 ± 1.5 mm, CAL a 6.5 ± 2.6 mm e PI a 1.4± 2. In nessun caso si è osservata una recrudescenza dell’infezione.
Il follow-up a 90 giorni mostrava un ulteriore miglioramento dei parametri parodontali: PPD diminuito a 3.7 ± 1.2 mm, CAL diminuito a 5.5 ± 2.5 mm e PI pari a 1.2 ± 0.8. In nessun caso si è osservata una recrudescenza dell’infezione.
Un caso clinico illustrativo è presentato nelle figure 3-8.
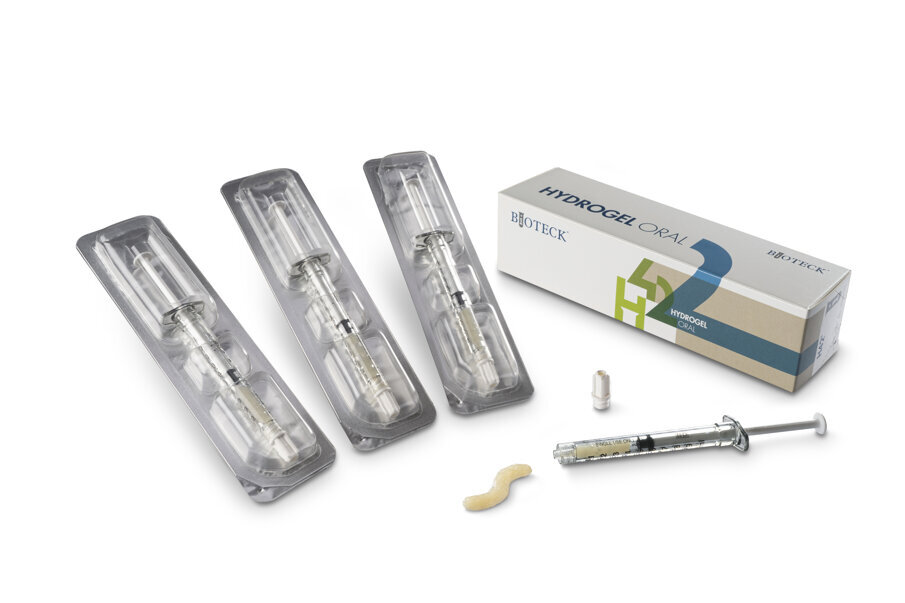
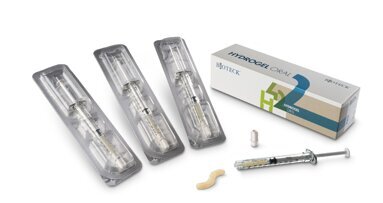
Fig. 1 - L’hydrogel collagenico H42 si presenta all’interno di siringhe fornite di attacco luer lock maschio, per poter essere abbinate all'ago più opportuno.
Fig. 2 - H42 viene applicato partendo dal fondo della tasca fino a colmarla completamente.
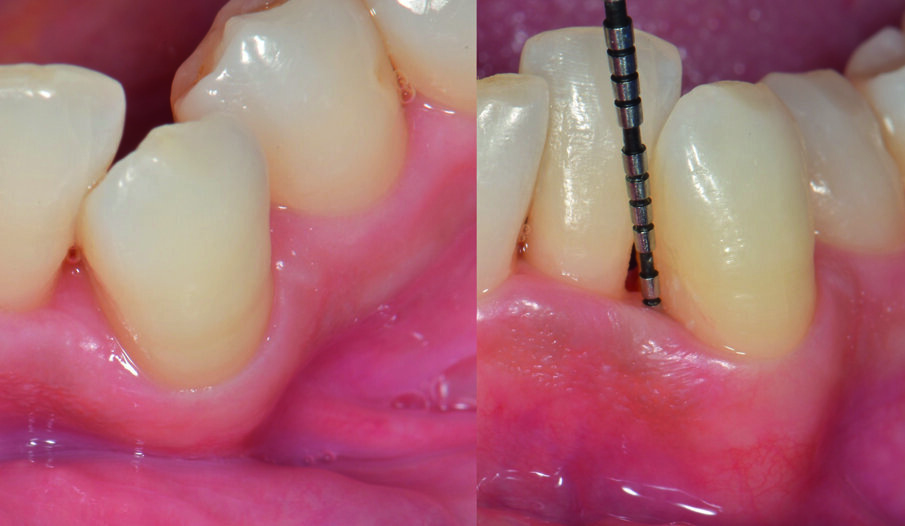
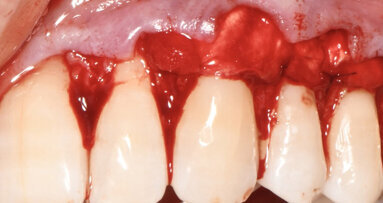
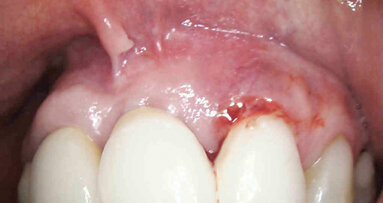
Fig. 3 - Caso clinico illustrativo. Visione frontale del difetto iniziale. I tessuti appaiono edematosi, la papilla interdentale è rigonfia e distaccata dalle superfici dei denti contigui.
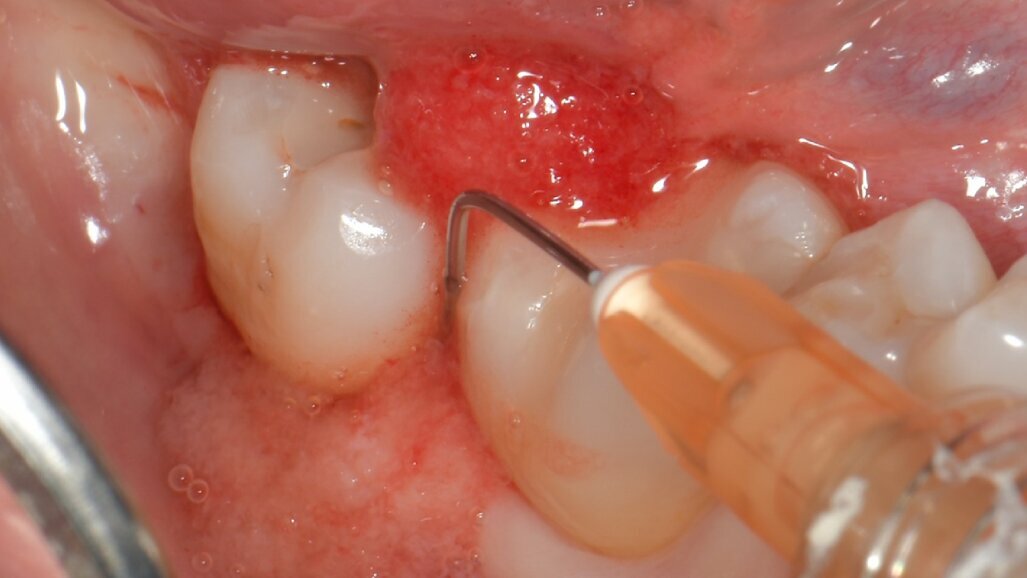
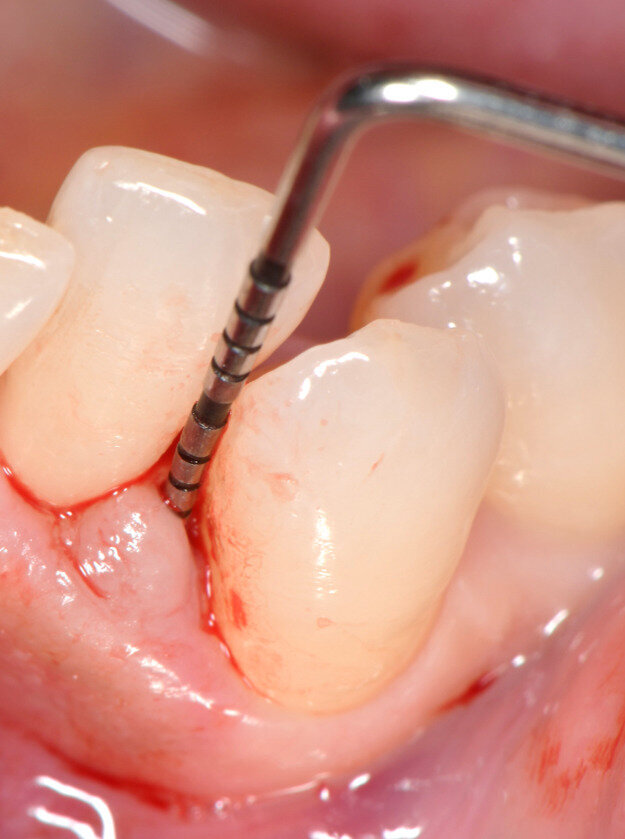
Fig. 4 - Sondaggio parodontale. PPD di 6 mm e CAL di 7 mm per l’elemento 33.
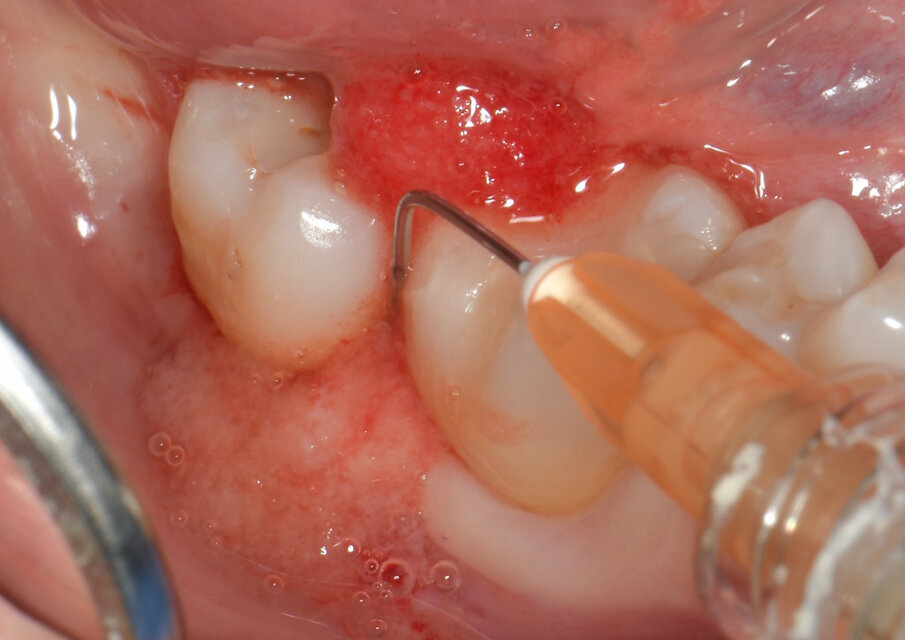
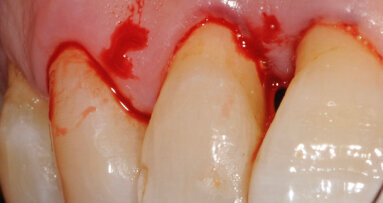
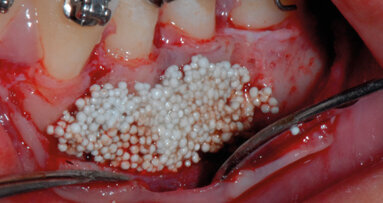
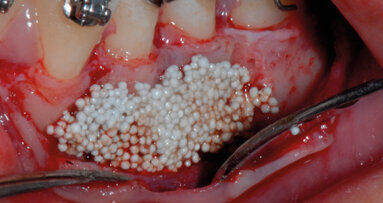
Fig. 5 - Fase di setting del prodotto H42. Il sito deve essere tenuto asciutto per 5 minuti dopo l’applicazione di H42 per favorirne l’adesione ai tessuti. Il prodotto è messo a colmare completamente la tasca, fino a uscirne.
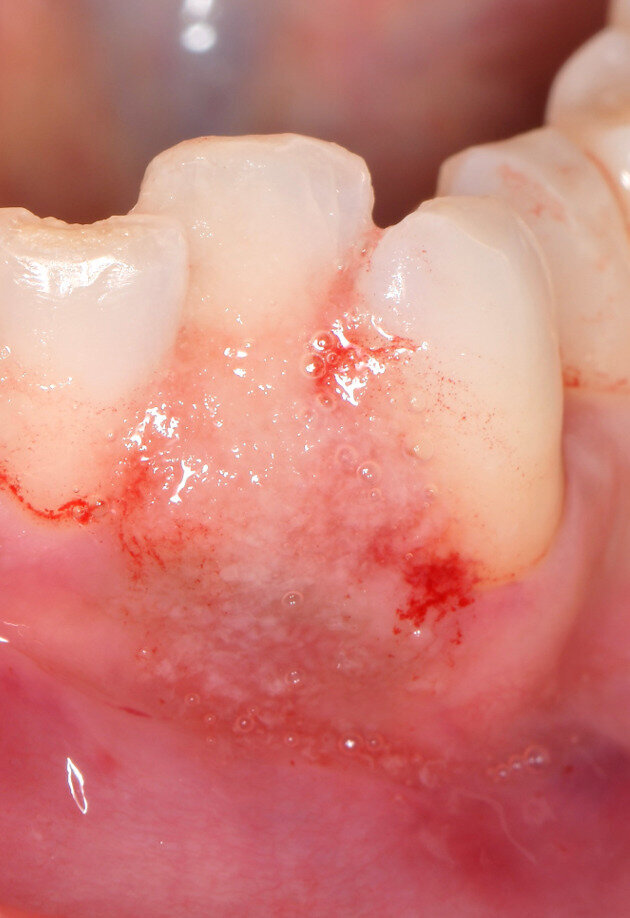
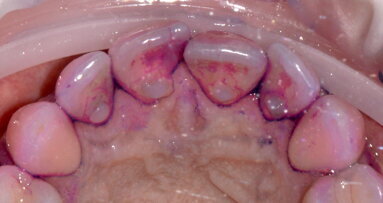
Fig. 6 - Visione occlusale del difetto trattato a 7 giorni di follow-up. Notare l’assenza di infiammazione e il tessuto guarito.
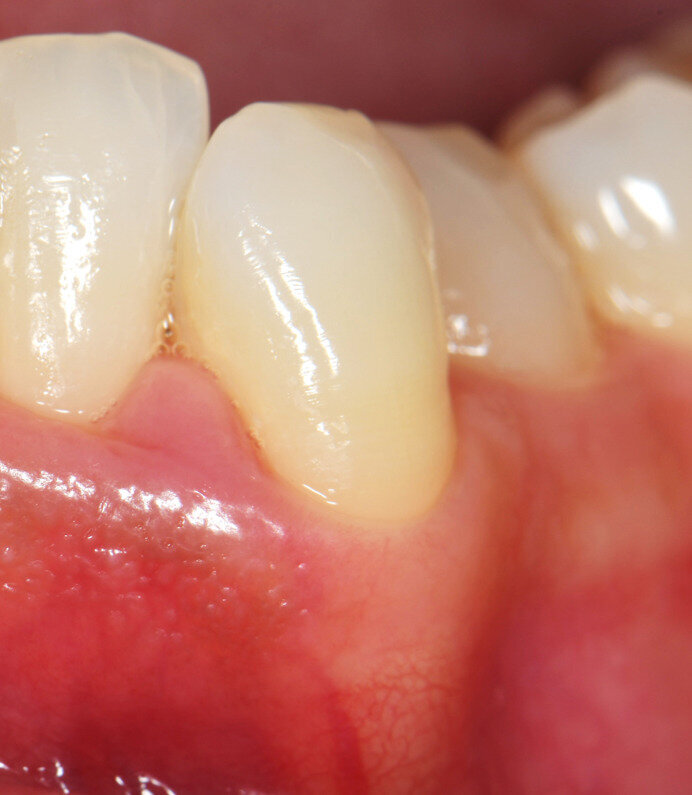
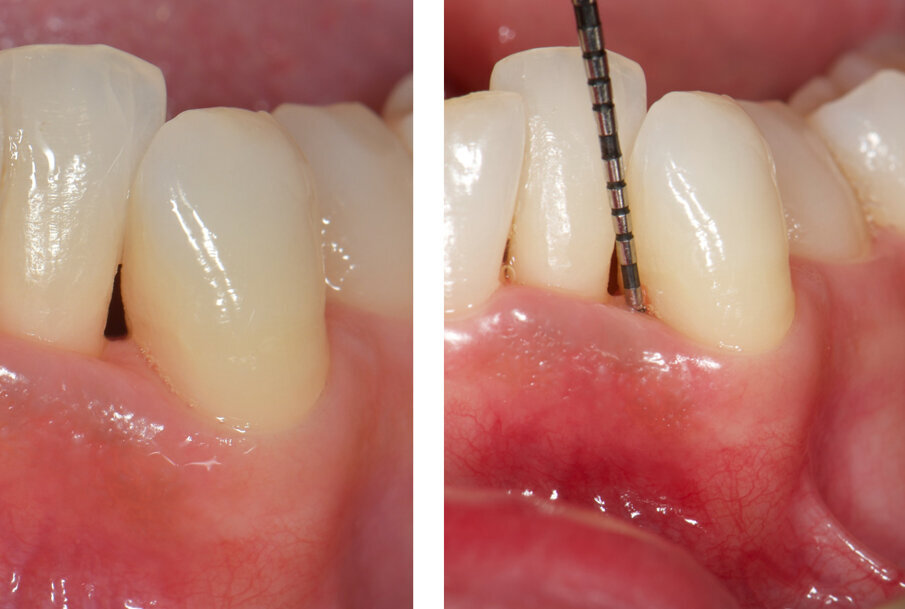
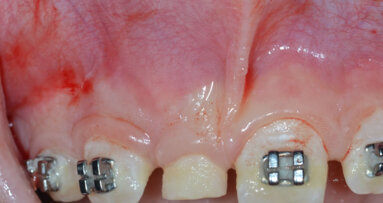
Fig. 7 - Visione frontale del difetto trattato a 30 giorni di follow-up. I parametri parodontali sono migliorati: PPD di 3 mm e CAL 4 mm. L’aspetto clinico dei tessuti è significativamente migliorato. L’edema della fase iniziale è rientrato e si nota una depressione al centro della papilla che evidenzia una fase avanzata della guarigione.
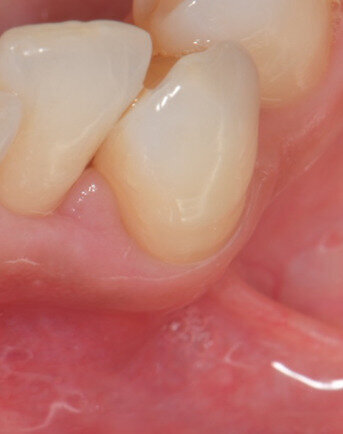
Fig. 8 - Visione occlusale del difetto trattato a 90 giorni di follow-up. La papilla è guarita con una retrazione del tessuto conseguente alla riduzione della profondità di tasca. La profondità di tasca si è ulteriormente ridotta: PPD di 2 mm e CAL 4 mm.
Discussione e conclusioni
La parodontite è una malattia infiammatoria multifattoriale causata dal biofilm sintetizzato da batteri patogeni che determina una risposta immunitaria che progressivamente danneggia l’epitelio connettivale. Ciò porta alla formazione di tasche parodontali e al possibile coinvolgimento dell’osso alveolare. È dunque importante intervenire precocemente per arrestare la progressione della malattia parodontale, favorendo la naturale rigenerazione dei tessuti.
La procedura standard prevede il debridement meccanico per eliminare il biofilm batterico5, causa dell’infiammazione che danneggia i tessuti gengivali. Tuttavia, una delle sfide più difficili è costituita dal mantenere pulito il sito trattato senza disturbare il naturale processo rigenerativo, che necessita di circa 4 settimane per arrivare a compimento7, 8. Diversi prodotti ad azione locale esercitano la loro funzione mediante antibiotici e/o sostanze battericide, che se da un lato sono efficaci a contrastare una reinfezione batterica, dall’altro possono interferire con il naturale processo di rigenerazione tessutale. Il collagene è invece la proteina che costituisce la maggior parte dei tessuti connettivi (compreso quello gengivale) e il suo apporto fornisce uno scaffold per la proliferazione dei fibroblasti e delle cellule implicate nella rigenerazione del tessuto parodontale.
Questa case series mostra che l’impiego del nuovo hydrogel collagenico (H42, Bioteck Spa, Arcugnano - Vicenza) costituito da collagene di tipo I, polimeri ad alto peso molecolare e quantità ancillari di vitamina C, è efficace nel promuovere la guarigione delle tasche parodontali, riducendo di circa 4 mm la profondità di tasca, diminuendo il CAL di circa 2.5 mm e riducendo l’indice di placca a circa 1 fino a 3 mesi di follow-up. Inoltre, già a 7 giorni dall’applicazione di H42 si è potuto constatare un’accelerazione della guarigione tissutale così come una riduzione dell’infiammazione. L’hydrogel H42 ha esercitato la propria funzione occludente, impedendo la ricolonizzazione batterica e, allo stesso tempo, il collagene ha fornito l’impalcatura necessaria ai fibroblasti per colonizzare il difetto e favorire la rigenerazione dell’epitelio gengivale attorno al dente, chiudendo dunque le tasche parodontali. Nessun effetto collaterale è stato osservato.
Bibliografia
- Kassebaum NJ, et al. Global burden of severe periodontitis in 1990-2010: a systematic review and meta-regression. J Dent Res, 93, (11), 1045-1053 (2014).
- Slots J. Periodontitis: facts, fallacies and the future. Periodontol 2000, 75, (1), 7-23 (2017).
- Papapanou PN, et al. Periodontitis: Consensus report of workgroup 2 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol, 89 Suppl 1, S173-S182 (2018).
- Kwon T, et al. Current Concepts in the Management of Periodontitis. Int Dent J, 71, (6), 462-476 (2021).
- Loesche WJ & Grossman NS. Periodontal disease as a specific, albeit chronic, infection: diagnosis and treatment. Clin Microbiol Rev, 14, (4), 727-752, table of contents (2001).
- Chatzigiannidou I, et al. Oral biofilms exposure to chlorhexidine results in altered microbial composition and metabolic profile. NPJ Biofilms Microbiomes, 6, (1), 13 (2020).
- Fraser D, et al. Periodontal Wound Healing and Regeneration: Insights for Engineering New Therapeutic Approaches. Front Dent Med, (2022).
- Christgau M, et al. Extracellular matrix expression and periodontal wound-healing dynamics following guided tissue regeneration therapy in canine furcation defects. J Clin Periodontol, 34, (8), 691-708 (2007).
Tag:
H42 è un hydrogel collagenico in siringa creato da Bioteck che possiede funzione coadiuvante nel trattamento di tasche parodontali e peri-implantari. La ...
La parodontite è una patologia infiammatoria cronica il cui sviluppo dipende dalla presenza di biofilm batterici disbiotici ed è caratterizzata dalla ...
Paziente di sesso femminile di anni 27 con anamnesi generale negativa e senza storia di malattia parodontale, si presenta in prima visita lamentando ...
Nel 2021, un paziente di 38 anni, non fumatore, si presentava all’attenzione del medico odontoiatra per la risoluzione di una recessione gengivale a ...
Le ampie riflessioni del Presidente SIDOC, Mangani, su una Conservativa “non più cenerentola”.
Già nel 1892, Bryan aveva introdotto la possibilità di accelerare il trattamento ortodontico tramite una stimolazione chirurgica. La tecnica ...
Già nel 1892, Bryan1 aveva introdotto la possibilità di accelerare il trattamento ortodontico tramite una stimolazione chirurgica. La tecnica ...
Gli odontomi composti sono neoformazioni benigne di origine odontogena localizzate prevalentemente nella parte anteriore del mascellare; compaiono ...
Il presente lavoro descrive la procedura con laser neodimio Nd:YAG 1064 nm per intervento di perimplantite.
Per ricercare mezzi terapeutici adiuvanti al trattamento delle lesioni parziali del nervo alveolare inferiore in seguito ad inserzione di impianti ...
Live webinar
mer. 3 giugno 2026
19:00 (CET) Rome
Live webinar
gio. 4 giugno 2026
20:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
18:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
19:00 (CET) Rome
Dr. Anthony Mak B.D.S, Prof. Marleen Peumans
Live webinar
lun. 8 giugno 2026
20:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
17:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
20:00 (CET) Rome
Nacho Fernández-Baca DDS, MSc



 Austria / Österreich
Austria / Österreich
 Bosnia ed Erzegovina / Босна и Херцеговина
Bosnia ed Erzegovina / Босна и Херцеговина
 Bulgaria / България
Bulgaria / България
 Croazia / Hrvatska
Croazia / Hrvatska
 Repubblica Ceca e Slovacchia / Česká republika & Slovensko
Repubblica Ceca e Slovacchia / Česká republika & Slovensko
 Francia / France
Francia / France
 Germania / Deutschland
Germania / Deutschland
 Grecia / ΕΛΛΑΔΑ
Grecia / ΕΛΛΑΔΑ
 Ungheria / Hungary
Ungheria / Hungary
 Italia / Italia
Italia / Italia
 Paesi Bassi / Nederland
Paesi Bassi / Nederland
 nordisch / Nordic
nordisch / Nordic
 Polonia / Polska
Polonia / Polska
 Portogallo / Portugal
Portogallo / Portugal
 Romania e Moldavia / România & Moldova
Romania e Moldavia / România & Moldova
 Slovenia / Slovenija
Slovenia / Slovenija
 Serbia e Montenegro / Србија и Црна Гора
Serbia e Montenegro / Србија и Црна Гора
 Spagna / España
Spagna / España
 Svizzera / Schweiz
Svizzera / Schweiz
 Turchia / Türkiye
Turchia / Türkiye
 Gran Bretagna e Irlanda / UK & Ireland
Gran Bretagna e Irlanda / UK & Ireland
 Internazionale / International
Internazionale / International
 Brasile / Brasil
Brasile / Brasil
 Canada / Canada
Canada / Canada
 America Latina / Latinoamérica
America Latina / Latinoamérica
 USA / USA
USA / USA
 Cina / 中国
Cina / 中国
 India / भारत गणराज्य
India / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
 Medio Oriente / Middle East
Medio Oriente / Middle East
















































To post a reply please login or register