Oberurzwil, Svizzera/Lipsia, Germania: circa 1,5 milioni di diversi dispositivi medici sono disponibili in tutto il mondo. Ogni anno, migliaia di nuovi prodotti vengono lanciati sul mercato. L’International Organization for Standardization (ISO) ha introdotto un nuovo standard internazionale, che mira a valutare la sicurezza e le prestazioni di tali dispositivi e migliorare la sicurezza per i pazienti.
ISO è una rete globale che identifica gli standard internazionali che sono richiesti da aziende, governi e società. L’organizzazione non governativa che sviluppa queste norme, in collaborazione con i settori che le metteranno in uso, adotta procedure trasparenti basate su input nazionali e permette che vengano attuate a livello mondiale.
Secondo le norme ISO, il nuovo standard ISO 14155:2011 fornirà una base tecnica per la regolamentazione e la riduzione al minimo degli ostacoli tecnici al commercio. È stata sviluppata per incoraggiare i produttori medicali al fine di garantire che i loro prodotti non compromettano la sicurezza del paziente.
Nel 2007, l’Organizzazione Mondiale della Sanità ha riferito che più di un milione di infortuni attribuibili a dispositivi medici ogni anno si verificano negli Stati Uniti. Inoltre, in alcuni Paesi in via di sviluppo, la metà delle apparecchiature mediche è risultata essere inutilizzabile o solo parzialmente utilizzabile.
Il nuovo standard indirizza la buona pratica clinica alla progettazione, all’esecuzione, registrazione e segnalazione degli esami clinici effettuati sugli esseri umani per valutare la sicurezza o le prestazioni dei dispositivi medici per motivi di regolamentazione e di altra specie. Questa norma internazionale specifica i requisiti generali diretti a tutelare i diritti, la sicurezza e il benessere degli esseri umani e per assicurare lo svolgimento scientifico dell’indagine clinica e la credibilità dei risultati delle indagini cliniche. I requisiti dovrebbero anche definire le responsabilità degli sponsor e dei ricercatori principali, nonché aiutare sponsor, sperimentatori, comitati etici, autorità di regolamentazione e altri organismi coinvolti nella valutazione della conformità dei dispositivi medici.
“I requisiti fissati dalla norma ISO 14.155 sono un importante passo avanti verso l’accettazione dei dati clinici a livello mondiale”, dice Danielle Giroud, Convenor del gruppo di lavoro che ha sviluppato lo standard.
LONDRA, Inghilterra: Il College of General Dentistry del Regno Unito ha pubblicato la terza edizione di Standards in Dentistry, un manuale completo e ...
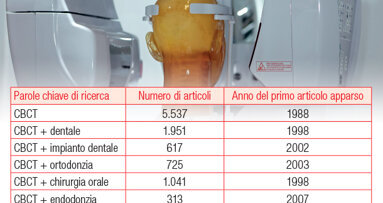
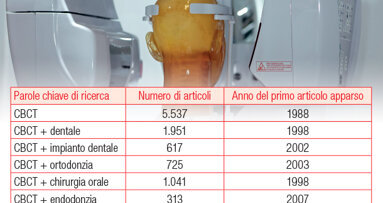
Fin dalla sua introduzione commerciale in odontoiatria nel 2001, la tomografia computerizzata cone beam (CBCT) è in rapida evoluzione come un nuovo ...
Fin dalla sua introduzione commerciale in odontoiatria nel 2001, la tomografia computerizzata cone beam (CBCT) è in rapida evoluzione come un nuovo ...
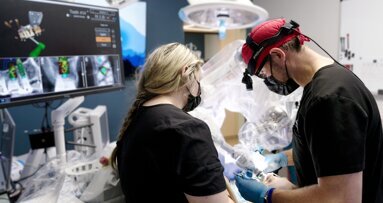
La robotica ha continuato a fare passi da gigante in diversi campi medici e l’implantologia dentale non fa eccezione. Il sistema Yomi di Neocis, l’unico...
SYDNEY, Australia: le ricerche dimostrano che l’attrattiva del viso può influenzare in modo significativo le decisioni sociali, comprese quelle legate ...
Norimberga, Germania – Gli ospedali universitari di Erlangen e di Ratisbona hanno annunciato che ospiteranno la 23a European Dental Materials ...
Rochester (USA) e Vancouver (Canada). L’interruzione della secrezione delle ghiandole salivari gioca un ruolo importante in alcune malattie della ...
In occasione del prossimo Congresso SIO, Sirona propone momenti di formazione continua nell’ambito delle tecnologie digitali.
WEST LAFAYETTE, Indiana, USA: La xerostomia è una condizione frequentemente riscontrata nei pazienti sottoposti a emodialisi, chemioterapia o radioterapia ...
A Chia (Sardegna) dal 13 al 15 giugno 2019 il top dell’Odontoiatria si trasforma in docente, aperte le iscrizioni su congressaio.it
Live webinar
mer. 3 giugno 2026
19:00 (CET) Rome
Live webinar
gio. 4 giugno 2026
20:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
18:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
19:00 (CET) Rome
Dr. Anthony Mak B.D.S, Prof. Marleen Peumans
Live webinar
lun. 8 giugno 2026
20:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
17:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
20:00 (CET) Rome
Nacho Fernández-Baca DDS, MSc



 Austria / Österreich
Austria / Österreich
 Bosnia ed Erzegovina / Босна и Херцеговина
Bosnia ed Erzegovina / Босна и Херцеговина
 Bulgaria / България
Bulgaria / България
 Croazia / Hrvatska
Croazia / Hrvatska
 Repubblica Ceca e Slovacchia / Česká republika & Slovensko
Repubblica Ceca e Slovacchia / Česká republika & Slovensko
 Francia / France
Francia / France
 Germania / Deutschland
Germania / Deutschland
 Grecia / ΕΛΛΑΔΑ
Grecia / ΕΛΛΑΔΑ
 Ungheria / Hungary
Ungheria / Hungary
 Italia / Italia
Italia / Italia
 Paesi Bassi / Nederland
Paesi Bassi / Nederland
 nordisch / Nordic
nordisch / Nordic
 Polonia / Polska
Polonia / Polska
 Portogallo / Portugal
Portogallo / Portugal
 Romania e Moldavia / România & Moldova
Romania e Moldavia / România & Moldova
 Slovenia / Slovenija
Slovenia / Slovenija
 Serbia e Montenegro / Србија и Црна Гора
Serbia e Montenegro / Србија и Црна Гора
 Spagna / España
Spagna / España
 Svizzera / Schweiz
Svizzera / Schweiz
 Turchia / Türkiye
Turchia / Türkiye
 Gran Bretagna e Irlanda / UK & Ireland
Gran Bretagna e Irlanda / UK & Ireland
 Internazionale / International
Internazionale / International
 Brasile / Brasil
Brasile / Brasil
 Canada / Canada
Canada / Canada
 America Latina / Latinoamérica
America Latina / Latinoamérica
 USA / USA
USA / USA
 Cina / 中国
Cina / 中国
 India / भारत गणराज्य
India / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
 Medio Oriente / Middle East
Medio Oriente / Middle East























































To post a reply please login or register