I pazienti edentuli da molti anni presentano un’atrofia dei mascellari variabile da paziente a paziente. Questa atrofia è dovuta a un riassorbimento dell’osso alveolare che si modifica con una predicibilità che segue un andamento bidimenzionale, verticale e orizzontale, nella mandibola e su tre dimensioni nel mascellare, verticale, orizzontale e centripeto1.
Il risultato generale porta, nell’edentulo bimascellare, a una modifica del profilo, individuabile con una normale cefalometria, verso una terza classe scheletrica di Angle. Il dato che riguarda il mascellare è particolare perché il fenomeno atrofico inizia con riassorbimento orizzontale che porta la cresta alveolare ad assumere in un primo momento una forma a lama (III-IV classe di Cawood e Howell per mascellare anteriore). Si assiste nello stesso tempo a un modico spostamento posteriore del punto cefalometrico A, in maniera diversa da paziente a paziente. Successivamente il riassorbimento diventa verticale (V classe di Cawood ed Howell). L’ulteriore spostamento palatale del punto A si traduce in una nuova morfologia da modifica in senso centripeto. Il rispetto di questa situazione anatomica acquisita è il must cui fare riferimento qualora si volesse procedere a una riabilitazione protesica fissa su impianti. Non sempre è possibile procedere a una GBR mirata a ricostruire la parte ossea persa, sia per motivazioni riferibili allo stato clinico del paziente sia per una sempre minore predicibilità dell’intervento correlata alla complessità del riassorbimento. A ciò si aggiunge la compliance del paziente, oggi sempre più esigente.
Gli interventi rigenerativi, relativi a questa complessità, sono associabili a una elevata morbilità, a un allungamento dei tempi e a un non sempre soddisfacente risultato. La necessità di riabilitare in tempi sempre più brevi il paziente ha determinato un by pass delle procedure rigenerative a favore di metodiche chirurgiche dirette che permettono una protesizzazione veloce. Nel mascellare superiore, in relazione ai diversi livelli di atrofia, si sono messe in campo tecniche tipo impianti pterigoidei (per le atrofie posteriori), impianti zigomatici e nasali (per le atrofie anteriori e laterali), e infine gli impianti sottoperiostei o iuxtagengivali per le atrofie totali. Se l’atrofia mascellare è moderata, nel senso che mantiene ancora una parte di osso alveolare nella zona della premaxilla, si possono attuare procedure con impianti angolati per evitare di poter danneggiare alcune strutture nobili come naso e seni mascellari. Gli impianti nasali e pterigoidei per essere attuati richiedono una chirurgia complessa con diversi gradi di possibili complicanze. Gli impianti zigomatici, oltre alla complessità dell’intervento, presentano un notevole impatto chirurgico e nello stesso tempo richiedono una particolare vigilanza del paziente spesso attuabile solo con sedute operatorie in narcosi e quindi in sala operatoria. Meno aggressivi sull’osso ma di grande impatto chirurgico sono gli impianti sottoperiostei customizzati con tecniche digitali che per essere posizionati richiedono ampie incisioni a tutto spessore della mucosa, importante scheletrizzazione del mascellare ovvero fissazione con viti di osteosintesi2-11.
I principi generali cui rispondono questi impianti sono relativi a una protesizzazione rapida senza osteointegrazione. I requisiti di stabilità e ritenzione del manufatto protesico vengono garantiti dalla collocazione sottoperiostea la quale, oltre alle viti di osteosintesi, garantisce l’inamovibilità della struttura che viene trattenuta dalla mucosa e con una estensione massima del suo disegno. Alla luce di queste considerazioni si osserva che i limiti delle soluzioni chirurgico-protesiche descritte sono i seguenti: o abbiamo osso a sufficienza da potere mettere impianti osteointegrati oppure, se non c’è osso, bisogna ricorrere a chirurgie aggressive, perfino nei sottoperiostei. Oggi si tende a ridurre l’estensione dell’impianto iuxtagengivale e a fissarlo con viti di osteosintesi; comunque, la customizzazione tende sempre a richiedere estensioni importanti, e quindi a chirurgie ad alto impatto per il paziente. Il Premaxillary Device (in seguito denominato PD) è un dispositivo che nasce per compensare molti degli aspetti negativi descritti in precedenza, in merito alle soluzioni chirurgico protesiche da attuare in caso di grave atrofia del mascellare.
Una prima osservazione da fare, proprio sull’anatomia del mascellare gravemente compromesso, è che non sempre si possono usare impianti zigomatici o pterigoidei; pertanto, l’alternativa potrebbe essere quella di creare un dispositivo sottoperiosteo. Il PD rientra nei dispositivi a collocazione sottoperiostea. Sappiamo, ai fini protesici, che oggi la riabilitazione dell’assetto dentario si ritiene sufficiente almeno fino ai premolari. Motivo per cui nelle riabilitazioni con impianti angolati e in numero ridotto tipo all-on-four si tende a protesizzare l’arcata dentaria in maniera non completa, ossia fino ai premolari oppure ai primi molari. Questa base di partenza della pianificazione chirurgica, che deve sempre essere su base protesica, è in ordine con la filosofia del PD perché nel mascellare gravemente compromesso ci garantisce l’estensione della dentatura fino a quanto detto. Il dispositivo però non è customizzato e questa è la novità; si dispone cioè di un dispositivo standardizzato, che si può produrre in misure variabili, sempre standard, tipo piccolo-medio-grande che ha una forma ad arco e che si estende in un settore del mascellare che va da 1.3/1.2 e 2.2/2.3, che in anatomia si chiama Premaxilla.
Il mascellare atrofico, con arretramento del punto cefalometrico A, vede spostato il riferimento dell’osso basale residuo, in cui si può eseguire fissazione di viti, al limite nucale della spina nasale anteriore; in pratica il limite anatomico nella cavità nasale non sarà più il setto cartilagineo ma la parte anteriore del vomere.
Materiali e metodi
Il dispositivo presenta quattro alloggiamenti per impianti di piccole dimensioni (3,3 mm) e di lunghezza variabile tra 8 e 12 mm. Se consideriamo lo spessore del dispositivo diciamo che gli impianti dovrebbero essere collocati a una profondità non superiore ai 4 mm. I punti precisi di fissazione sarebbero, con l’ultimo disegno del PD, uno anteriore nella parte più nucale della spina nasale anteriore e uno più nucale nella parte iniziale della zona in cui il vomere si incastona con il versante nasale della sutura palatina mediana. Gli altri due sono rispettivamente nel primo e secondo quadrante in corrispondenza delle suture della premaxilla con le ossa mascellari. La testa degli impianti è progettata per restare una frazione di millimetro sotto la superfice del dispositivo.
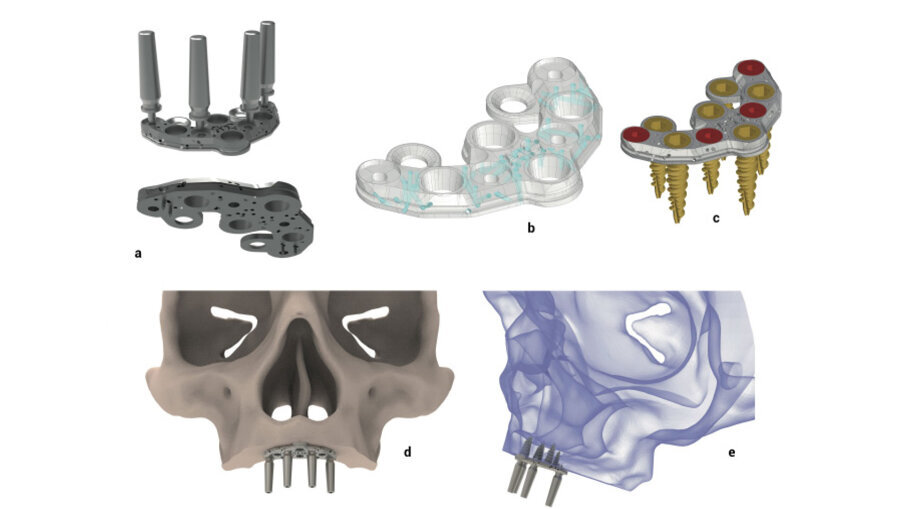
Lo spessore della struttura del PD presenta 44 microfori passanti che permettono allo stesso di non fare effetto barriera tra l’osso basale e il periostio sovrastante. I dispositivi si distinguono in “a carico immediato” con i monconi monolitici senza connessioni da protesizzare subito; ed “a carico differito” cioè senza monconi ma con alloggiamenti filettati per permette di avvitare in un secondo momento quattro monconi per la protesizzazione (Fig. 1). Il procedimento chirurgico prevede una minima incisione da canino a canino, scheletrizzazione con distacco della parte terminale del nervo nasopalatino, come tutti i sottoperiostei, la modellazione dell’osso residuo con piezosurgery o fresoni per accogliere la forma del dispositivo ad appoggio completo e fissazione con impianti ridotti come detto sopra. La sutura sarà a completa copertura del PD a seconda se a carico immediato o differito prevede una seconda apertura solo sulle connessioni dei monconi che hanno delle viti tappo inserite (Figg. 2-15).
Fig. 1 - Struttura dei diversi dispositivi.
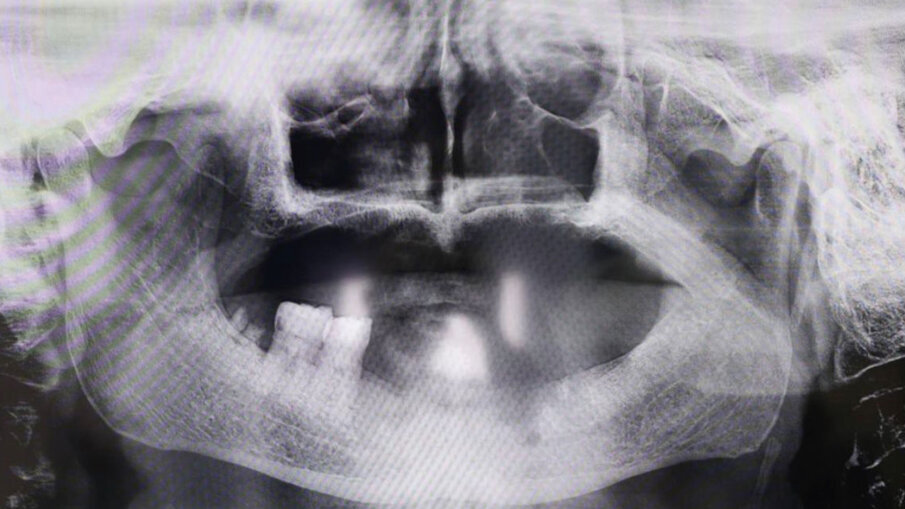
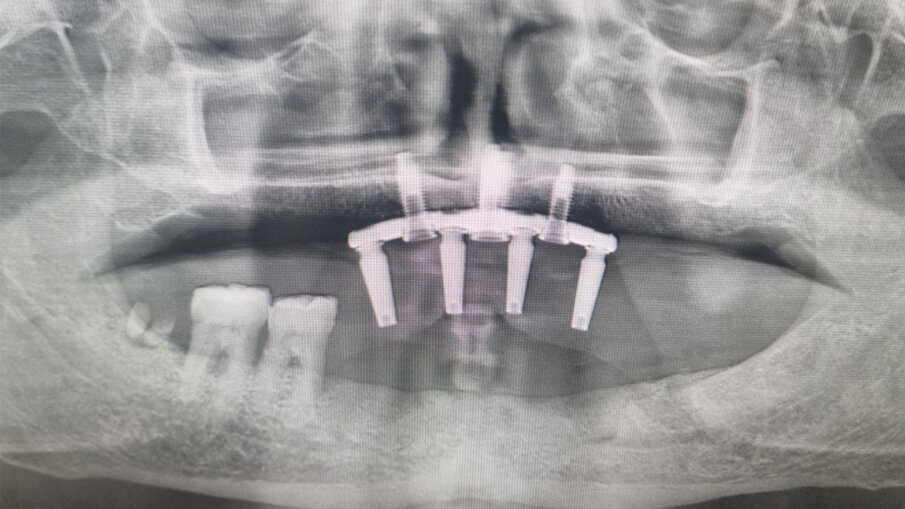
Fig. 3 - RX iniziale. Il Paziente ottantenne si presenta con una protesi mobile realizzata e inserita da oltre 20 anni. Il desiderio di avere i denti fissi non l’ha mai abbandonato. Dalla RX si evince la chiara assenza totale di osso, situazione che non permette l’inserimento degli impianti in titanio tramite intervento tradizionale. Questo caso è stato affrontato tramite l’inserimento del Premaxillary Device.
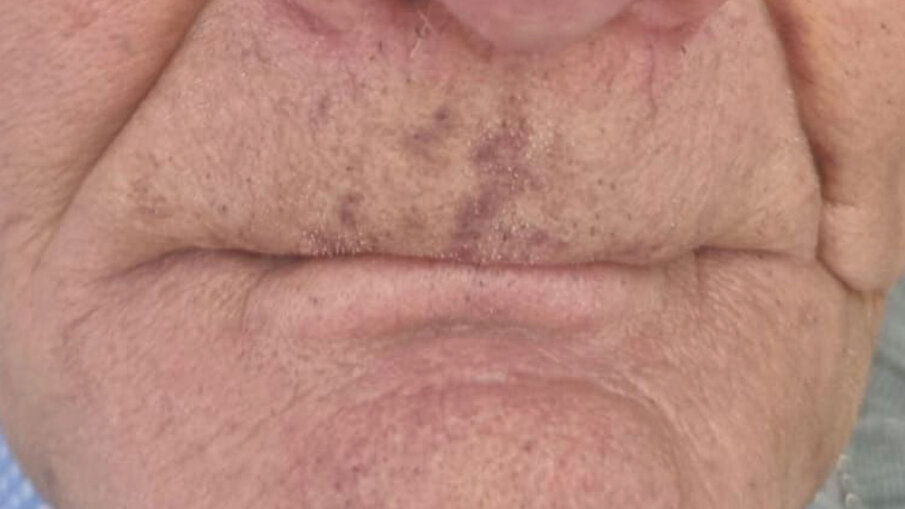
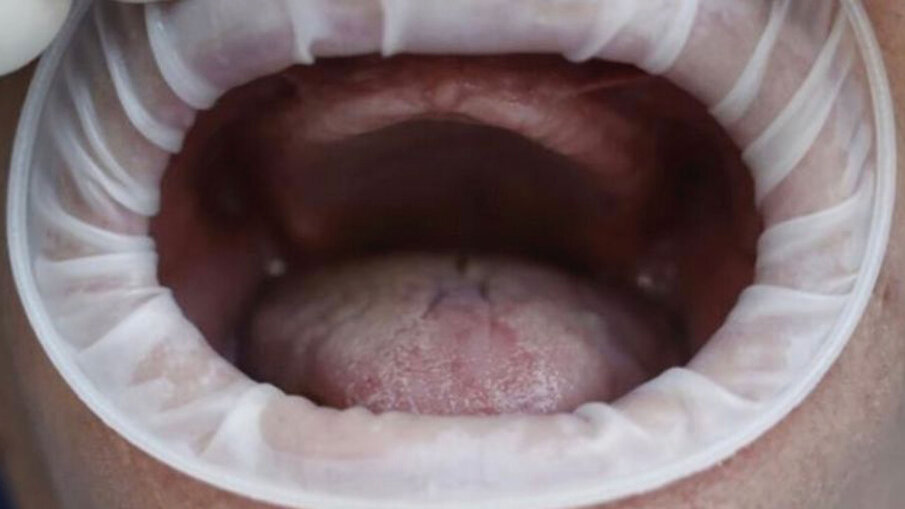
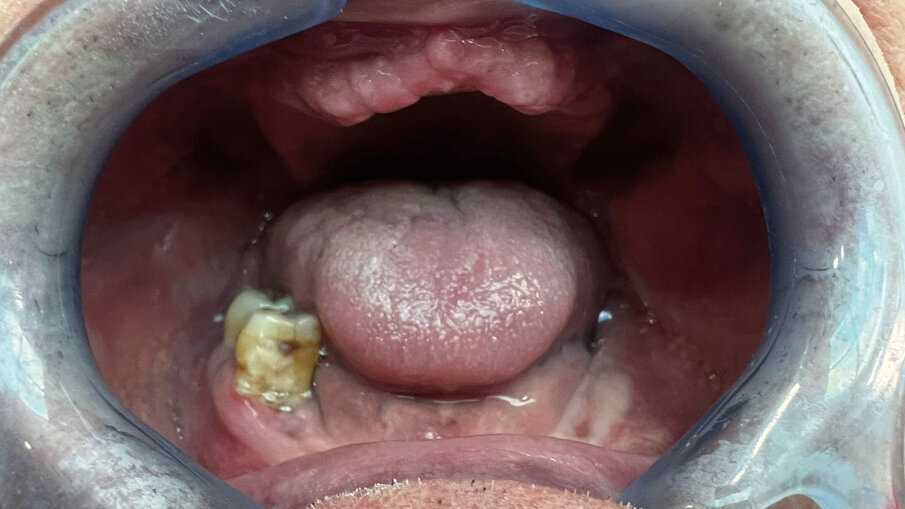
Fig. 4 - Foto della mucosa prima dell’inserimento del device.
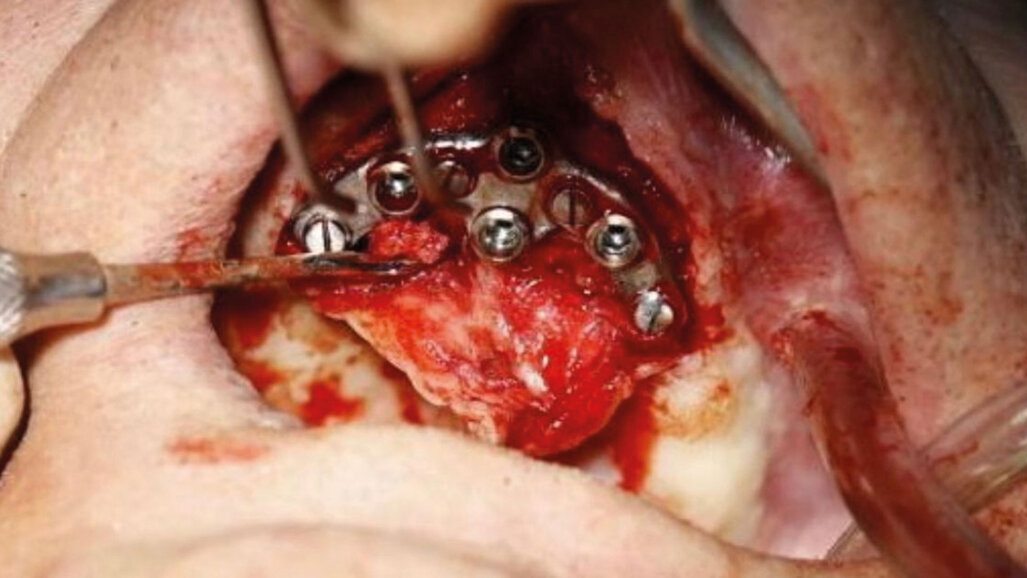
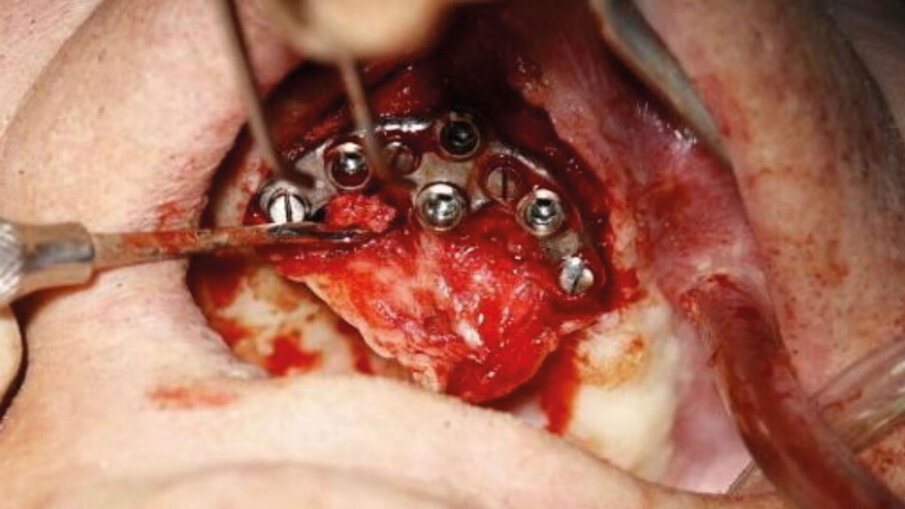
Fig. 5 - Foto durante l’inserimento del device.
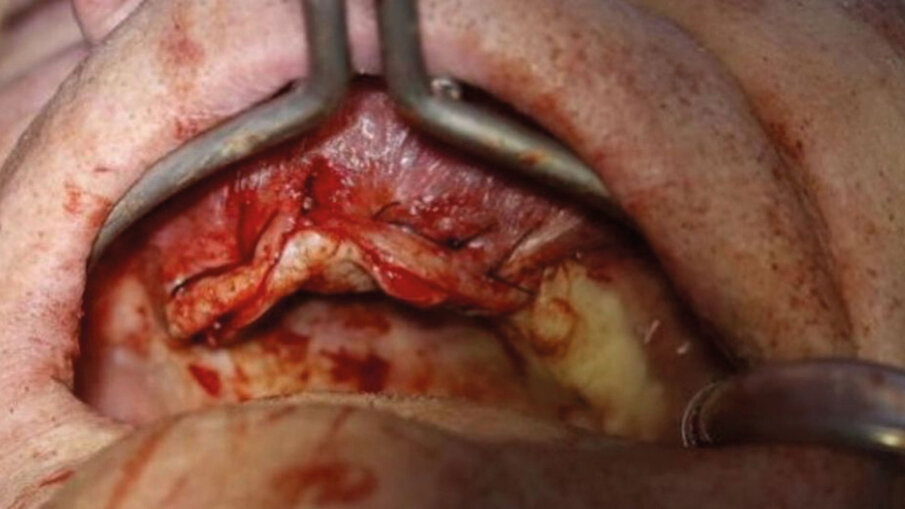
Fig. 6 - Foto chiusura tramite punti riassorbibili. Fine Intervento con durata massimo 18/20 minuti suture comprese.
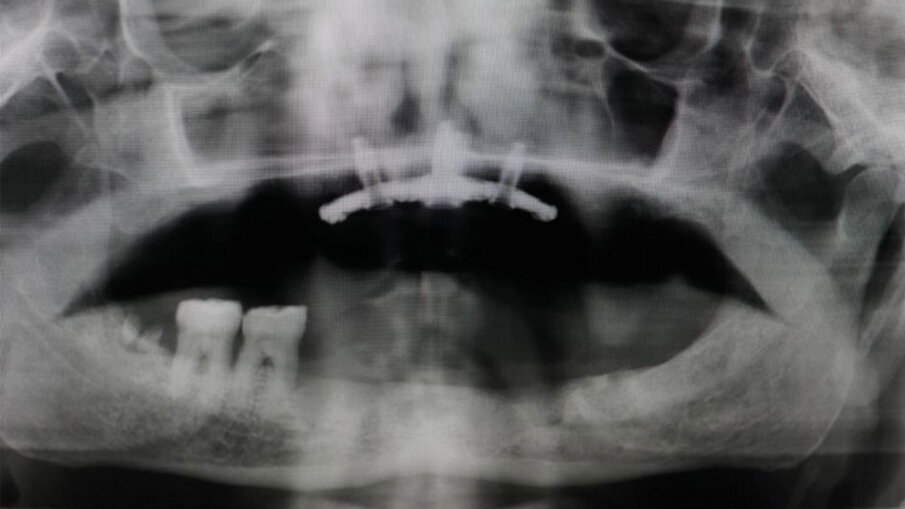
Fig. 7 - RX dopo l’inserimento del Premaxillary Device.
Fig. 8 - Mucosa gengivale prima della scopertura delle viti tappo e successivo inserimento dei monconi.
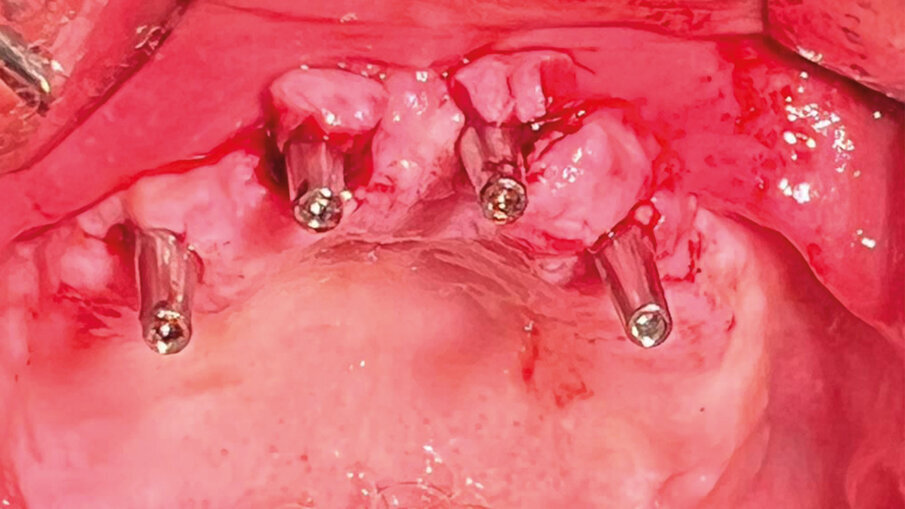
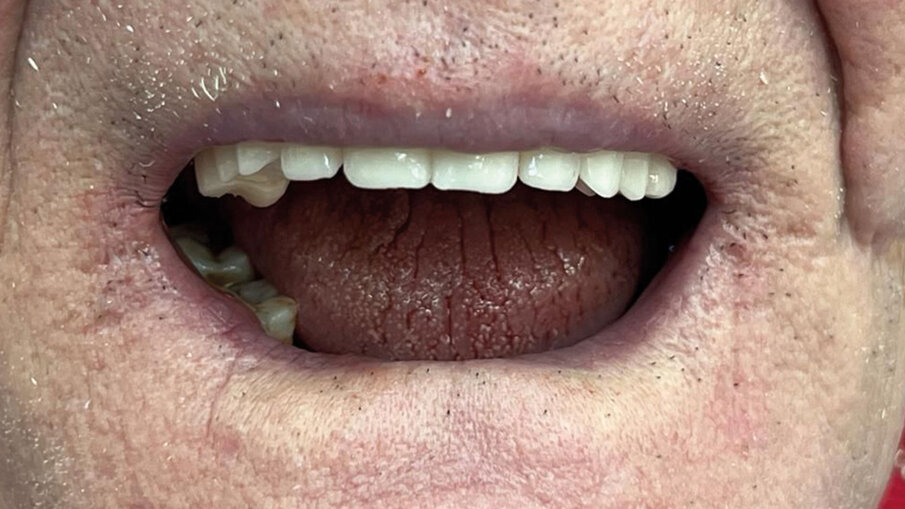
Fig. 9 - Foto vista completa dopo aver inserito i monconi.
Fig. 10 - RX dopo 3 Mesi. Si è proceduto con l’inserimento dei monconi più provvisorio fisso.
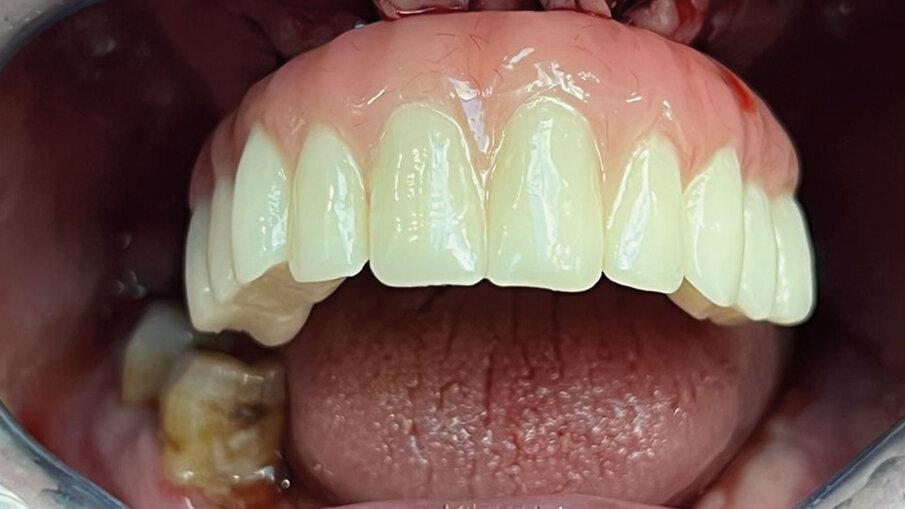
Fig. 11 - Fotografia con vista frontale prima dell’inserimento dei monconi.
Fig. 12 - Inserimento provvisori - vista frontale.
Fig. 13 - Senza provvisori - vista laterale.
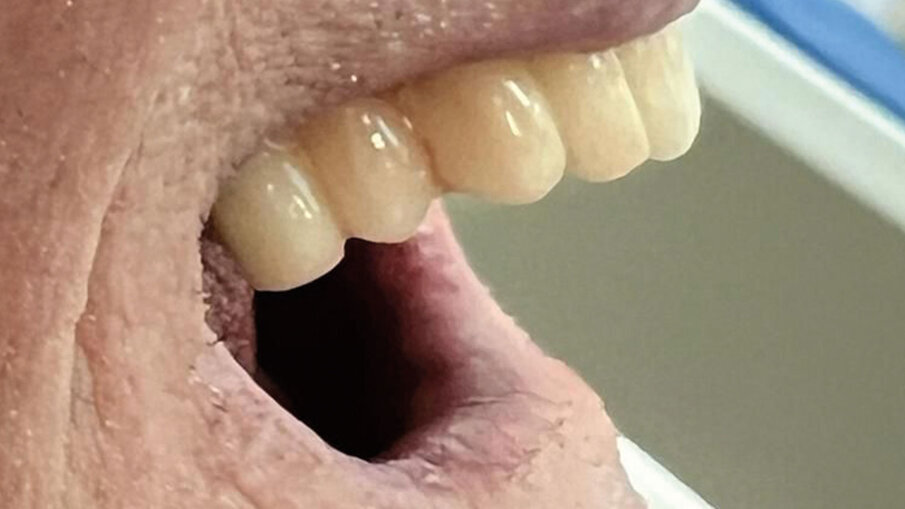
Fig. 14 - Inserimento provvisori - vista laterale.
Fig. 15 - Inserimento dei denti provvisori subito dopo aver avvitato i monconi sul Device.
Discussione
Gli impianti sottoperiostei, inseriti sotto il periostio, direttamente sul tessuto osseo, sono stati proposti da Dahl in Svezia nei primi anni 40, sono stati in uso in uso negli anni 50 e 60 del secolo scorso2, 4, 8, 11-22. Successivamente sono andati in disuso, per le problematiche legate, soprattutto, a una notevole e non accettabile percentuale di fallimenti. In quegli anni, la tecnica per fabbricare gli impianti sottoperiostei era molto complessa, era molto difficile ottenere un adattamento preciso dell’impianto al letto osseo, e la tecnica di posizionamento era molto indaginosa e richiedeva una notevole quantità di tempo2, 4. La struttura implantare era di grandi dimensioni e necessitava dell’esecuzione e realizzazione di lembi molto ampi per essere posizionata5. La necessità di un doppio intervento chirurgico, il primo per prendere l’impronta della struttura ossea e il secondo per posizionare l’impianto, certamente avevano un effetto negativo sui processi di guarigione5, 11. I materiali, poi, soprattutto cromo-cobalto e vitallium non erano dei più performanti4, 5, 11. Inoltre, le tecniche radiologiche disponibili in quei tempi non permettevano un’immagine precisa dell’anatomia della struttura ossea del paziente. Stvrecky e coll.19, nel 1993, in un lavoro retrospettivo sui vecchi impianti sottoperiostei per un periodo di 15 anni riportavano una sopravvivenza a 5-10 anni del 58.3%. Dalla fine degli anni 60, gli impianti endossei proposti inizialmente da PI Branemark hanno completamente soppiantato e sostituito gli impianti sottoperiostei4. Negli ultimi anni, grazie al notevole sviluppo sia delle nuove tecnologie digitali, CBCT, scanners intraorali, che di materiali, soprattutto metalli molto più performanti, e di tecniche di manifattura e chirurgiche sempre più sofisticate, gli impianti sottoperiostei sono tornati un po’ in auge e di moda4, 5, 11. La stampa in 3D dei metalli ha permesso un’accuratezza sempre più precisa, rispecchiando il disegno originale, durante il processo di realizzazione del manufatto implantare5, 11.
La osteointegrazione del titanio è un altro fattore estremamente positivo, perché permette la realizzazione di un manufatto protesico di minori dimensioni5. Infatti, ci sono delle condizioni cliniche di grave atrofia della ossa mascellari, soprattutto a livello del mascellare superiore, che possono essere trattati con grande difficoltà. Tecniche proposte sono state:
- innesti ossei, tipo inlay/onlay ed impianti endossei;
- rigenerazione ossea guidata (GBR);
- impianti angolati;
- impianti zigomatici;
- impianti pterigo-mascellari;
- distrazione osteogenetica;
- splitting della cresta alveolare;
- rialzo di seno mascellare3, 4, 6, 11.
Tutte queste tecniche sono, però, molto complesse, devono essere affidate a chirurghi orali e implantologi esperti, richiedono molto tempo per la loro realizzazione. Possono essere gravate da complicanze anche importanti, comportano un costo biologico e aggiuntivo per il paziente4.
Oggi, l’utilizzo di questi impianti può offrire tutta una serie di grandi vantaggi, dalla riduzione dei tempi di trattamento, al poter evitare procedimenti chirurgici particolarmente complessi, alla riduzione dell’onere finanziario per il paziente2. Il notevole sviluppo delle conoscenze con l’ausilio di nuovi hardware e software sempre più sofisticati hanno permesso la realizzazione estremamente precisa di modelli digitali 3D e della realizzazione di manufatti implantari estremamente precisi ed efficaci2. Recentemente, in letteratura è possibile trovare dei lavori su questa nuova generazione di impianti sottoperiostei in cui si mette in evidenza che questi impianti non sarebbero associati con segni di riassorbimento osseo, mobilità, infezione oppure frattura della protesi2. Soddisfacenti percentuali di sopravvivenza sono state riportate (circa 95%). Nemtoi e coll.4 riportano uno studio su 16 pazienti, seguiti per 6 mesi, con solo un impianto perso, con intervento chirurgico-protesico in un tempo medio di circa 90 minuti, senza complicazioni rilevanti. Sono stati riferiti, nell’immediato periodo postoperatorio, dolore, tumefazione ed edema, in alcuni casi sanguinamento, in altri casi un’esposizione di parte dell’impianto senza, però, perdita della funzionalità dello stesso. Ottima è, poi, risultata l’apposizione del dispositivo a livello del tessuto osseo, con un fit estremamente preciso. Dimitroulis e coll.5 riportano uno studio su 21 pazienti, seguiti per un periodo di tempo di 22 mesi. Complicazioni osservate sono state:
- 5 esposizioni;
- 1 mobilità dell’impianto;
- 1 impianto rimosso, ma per cause diverse (salute mentale).
I pazienti hanno riferito dei risultati positivi per quanto riguarda il loro confort, la capacità della masticazione, e la stabilità della restaurazione protesica fissa. Mangano e coll.11 riferiscono su 10 pazienti con una percentuale di sopravvivenza dell’impianto sottoperiosteo del 100% a un anno, e una percentuale di complicanze precoci del 10% e di complicanze tardive del 20%. Van der Borre e coll.10 hanno condotto uno studio su 15 pazienti, con un follow-up di un anno, senza nessuna complicanza e perdita di impianti.
In un caso si è avuta frattura della protesi provvisoria. D’altra parte, bisogna tener conto che si tratta di lavori con un numero esiguo di pazienti (circa 10-15), con un brevissimo o breve follow-up, da 6 mesi a pochissimi anni. Sono presenti anche singoli case reports. L’uso, poi, di impianti sottoperiostei customizzati rende possibile una terapia rapida ed estremamente poco invasiva2. Uno degli aspetti più importanti in questa tipologia di impianti è che devono avere una stabilità meccanica sufficiente, in grado di permettere una buona resistenza ai carichi masticatori2.
Per favorire la neoformazione di tessuto osseo, il device oggetto di questo articolo è stato fornito di fori, che servono a favorire la stabilità secondaria dell’impianto, mentre quella primaria viene a essere garantita dalle viti di fissaggio5. Un altro possibile vantaggio degli impianti sottoperiostei potrebbe essere il fatto che permetterebbero una funzione estetica, masticatoria e fonetica immediata3.
Ringraziamenti
Una menzione particolare va al Sig.re Aldo Corbo, imprenditore sanitario agrigentino meritevole di un riconoscimento per la sua intuizione, il Premaxillary Device, oggetto della presente ricerca.
Bibliografia
- Cawood JI, Howell RA. A classification of the edentulous jaws. Int J Oral Maxillofac Surg. 1988;17:232-6.
- Bai L, Zheng L, Ji P, Wan H, Zhou N, Liu R, Wang C Additively Manufactured Lattice-like Subperiosteal Implants for Rehabilitation of the Severely Atrophic Ridge. ACS Biomater Sci Eng. 2022;8:912-920.
- Rinaldi M, De Neef B, Loomans NAJ, Mommaerts MY Guidelines for the Use of Resection Guides for Subperiosteal Maxillary Implants in Cases of Terminal Dentition - A Novel Approach. Ann Maxillofac Surg. 2020;10:467-471.
- Nemtoi A, Covrig V, Nemtoi A, Stoica G, Vatavu R, Haba D, Zetu I Custom-Made Direct Metal Laser Sintering Titanium Subperiosteal Implants in Oral and Maxillofacial Surgery for Severe Bone-Deficient Patients-A Pilot Study. Diagnostics 2022;12:2531
- Dimitroulis, Gupta B, Wilson I, Hart C The atrophic edentulous alveolus. A preliminary study on a new generation of subperiosteal implants Oral Maxillofac Surg 2022 Feb 4. doi: 10.1007/s10006-022-01044-3
- De Moor E, Huys SEF , van Lenthe GH , Mommaerts MY , Vander Sloten J Mechanical evaluation of a patient-specific additively manufactured subperiosteal jaw implant (AMSJI) using finite-element analysis Int J Oral Maxillofac Surg 2022;51:405-411
- Mommaerts MY. Additively manufactured sub-periosteal jaw implants. Int J Oral Maxillofac Surg. 2017;46:938-940.
- Van den Borre C, Rinaldi M, De Neef B, Loomans NAJ, Nout E, Van Doorne L, Naert I, Politis C, Schouten H, Klomp G, Beckers L, Freilich MM, Mommaerts MY. Radiographic Evaluation of Bone Remodeling after Additively Manufactured Subperiosteal Jaw Implantation (AMSJI) in the Maxilla: A One-Year Follow-Up Study. J Clin Med. 2021;10:3542
- Mommaerts MY. Evolutionary steps in the design and biofunctionalization of the additively manufactured sub-periosteal jaw implant 'AMSJI' for the maxilla. Int J Oral Maxillofac Surg. 2019;48:108-114.
- Van den Borre C, Rinaldi M, De Neef B, Loomans NAJ, Nout E, Van Doorne L, Naert I, Politis C, Schouten H, Klomp G, Beckers L, Freilich MM, Mommaerts MY. Patient- and clinician-reported outcomes for the additively manufactured sub-periosteal jaw implant (AMSJI) in the maxilla: a prospective multicentre one-year follow-up study. Int J Oral Maxillofac Surg. 2022;51:243-250.
- Mangano C, Bianchi A, Mangano FG , Dana J , Colombo M , Solop I, Admakin O Custom-made 3D printed subperiosteal titanium implants for the prosthetic restoration of the atrophic posterior mandible of elderly patients: a case series 3D Print Med 2020;6:1.
- Bodine RL Jr, Kotch RL. Experimental subperiosteal dental implants. US Armed Forces Med J. 1953;4:440-51.
- Webster RC, White MF, Smith RC, Johnson CM, Smith RR, White BJ, Clairmont AA, Smith CW Chin augmentation: Subperiosteal and supraperiosteal implants. Aesthetic Plast Surg. 1976;1:149-60.
- Yamane T. Theory of endosteal-subperiosteal implants. 1977;1:150-5.
- Benson D Tissue considerations for mandibular subperiosteal implants. J Prosthet Dent. 1977;37:67-73.
- Young L Jr, Michel JD, Moore DJ A twenty-year evaluation of subperiosteal implants. J Prosthet Dent. 1983;49:690-4
- James RA, Lozada JL, Truitt PH, Foust BE, Jovanovic SA Subperiosteal implants. CDA J. 1988;16:10-4.
- Linkow LI Titanium subperiosteal implants. J Oral Implantol. 1989;15:29-33, 36-40.
- Stvrtecky RO, Borgetti ZA, Manzano M Subperiosteal implants. J Oral Implantol. 1993;19:48-53.
- Golec TS, Krauser JT Long-term retrospective studies on hydroxyapatite coated endosteal and subperiosteal implants. Dent Clin North Am. 1992;36:39-65.
- Linkow LI, Ghalili R Ramus hinges for excessive movements of the condyles: a new dimension in mandibular tripodal subperiosteal implants. J Oral Implantol. 1999;25:11-7.
- Schou S, Pallesen L, Hjørting-Hansen E, Pedersen CS, Fibaek B. A 41-year history of a mandibular subperiosteal implant. Clin Oral Implants Res. 2000;11:171-8.
L'Articolo è stato pubblicato su Implant Tribune Italian Edition 2/2023.
Tag:
Evento esclusivo a Firenze per il lancio sul mercato della “nuova sensazione”.
Evento esclusivo a Firenze per il lancio sul mercato della “nuova sensazione”.
MILANO, Italia: Straumann ha sviluppato un nuovo e più resistente materiale metallico con proprietà superiori di osteointegrazione: ...
SALLANCHES, Francia: Lo specialista francese in implantologia Anthogyr, parte di Straumann Group, è noto per il suo impegno nell’innovazione e nei ...
Sweden & Martina presenta i nuovi impianti Premium Kohno transmucosi, a completamento del programma di impianti Premium Kohno sommersi già ...
Impianto monocomponente con filettatura a compressione.
Progettato partendo da un’esigenza di semplicità, CSR-DAT rappresenta l’ultima sfida di Sweden & Martina: creare un impianto che ...
Progettato partendo da un’esigenza di semplicità, CSR-DAT rappresenta l’ultima sfida di Sweden & Martina: creare un impianto che ...
Due straordinarie giornate di corso gratuito tenute dal dott. Ignazio Loi il 24 e 25 ottobre scorsi ad Abano Terme, presso il centro congressi Pietro ...
Tutte le case produttrici di impianti hanno dei cataloghi molto accurati che illustrano con foto e disegni tutta la gamma dei prodotti dagli impianti agli ...
A un anno esatto dall’arrivo del sistema implantare NeO sul mercato italiano, Alpha-Bio Tec presenta NeO CS, connessione conometrica standard per gli ...
Live webinar
lun. 8 giugno 2026
18:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
19:00 (CET) Rome
Dr. Anthony Mak B.D.S, Prof. Marleen Peumans
Live webinar
lun. 8 giugno 2026
20:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
17:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
20:00 (CET) Rome
Nacho Fernández-Baca DDS, MSc
Live webinar
gio. 11 giugno 2026
1:00 (CET) Rome
Live webinar
gio. 11 giugno 2026
19:00 (CET) Rome



 Austria / Österreich
Austria / Österreich
 Bosnia ed Erzegovina / Босна и Херцеговина
Bosnia ed Erzegovina / Босна и Херцеговина
 Bulgaria / България
Bulgaria / България
 Croazia / Hrvatska
Croazia / Hrvatska
 Repubblica Ceca e Slovacchia / Česká republika & Slovensko
Repubblica Ceca e Slovacchia / Česká republika & Slovensko
 Francia / France
Francia / France
 Germania / Deutschland
Germania / Deutschland
 Grecia / ΕΛΛΑΔΑ
Grecia / ΕΛΛΑΔΑ
 Ungheria / Hungary
Ungheria / Hungary
 Italia / Italia
Italia / Italia
 Paesi Bassi / Nederland
Paesi Bassi / Nederland
 nordisch / Nordic
nordisch / Nordic
 Polonia / Polska
Polonia / Polska
 Portogallo / Portugal
Portogallo / Portugal
 Romania e Moldavia / România & Moldova
Romania e Moldavia / România & Moldova
 Slovenia / Slovenija
Slovenia / Slovenija
 Serbia e Montenegro / Србија и Црна Гора
Serbia e Montenegro / Србија и Црна Гора
 Spagna / España
Spagna / España
 Svizzera / Schweiz
Svizzera / Schweiz
 Turchia / Türkiye
Turchia / Türkiye
 Gran Bretagna e Irlanda / UK & Ireland
Gran Bretagna e Irlanda / UK & Ireland
 Internazionale / International
Internazionale / International
 Brasile / Brasil
Brasile / Brasil
 Canada / Canada
Canada / Canada
 America Latina / Latinoamérica
America Latina / Latinoamérica
 USA / USA
USA / USA
 Cina / 中国
Cina / 中国
 India / भारत गणराज्य
India / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
 Medio Oriente / Middle East
Medio Oriente / Middle East


























































To post a reply please login or register