Le patologie infettive che colpiscono i tessuti parodontali e perimplantari hanno un comune primum movens eziopatogenetico: l’accumulo di placca batterica a livello marginale.
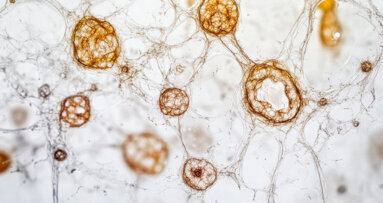
La placca batterica presenta tutte le caratteristiche proprie di un biofilm; si tratta, infatti, di un aggregato di cellule microbiche adese a una superficie e incluse in una matrice polimerica extracellulare da esse prodotta. Come tutti i biofilm, la placca batterica è caratterizzata da eterogeneità strutturale e interazioni biologiche complesse fra le specie batteriche in essa incluse.
Subito dopo la detersione meccanica delle superfici dentarie o implantoprotesiche, si verifica la precipitazione di una pellicola composta prevalentemente da glicoproteine salivari che mediano la successiva adesione dei batteri orali a tali superfici. I colonizzatori precoci della pellicola sono rappresentati da specie aerobie Gram-positive, appartenenti al genere Streptococcus e Actinomyces, con metabolismo saccarolitico; tali specie, infatti, utilizzano come substrato energetico i carboidrati semplici introdotti con la dieta. La mancata rimozione della placca determina un aumento del suo spessore, con diminuzione della concentrazione di ossigeno e dei nutrienti provenienti dal cavo orale negli strati più profondi.
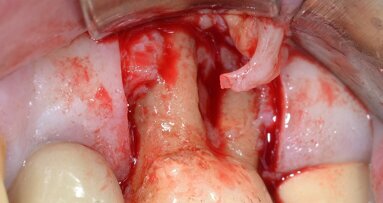
Le mutate condizioni ambientali inducono una progressiva variazione della composizione del biofilm, soprattutto nella porzione che si estende sotto il margine gengivale (placca sottogengivale). In questa sede, che rappresenta una nicchia ecologica dove i fattori antimicrobici salivari non hanno accesso, compaiono, e si espandono progressivamente, specie anaerobie facoltative e anaerobie obbligate, in prevalenza Gram-negative, caratterizzate da un metabolismo asaccarolitico; tali specie, infatti, utilizzano come substrato energetico proteine presenti nel fluido del solco gengivale o della tasca parodontale. La presenza di batteri Gram-negativi nella placca sottogengivale induce, nell’arco di pochi giorni, un processo infiammatorio che si estrinseca, dal punto di vista clinico, in una gengivite marginale; tale processo, se non adeguatamente trattato, può evolvere in parodontite cronica, patologia che si estende anche ai tessuti parodontali profondi (connettivo gengivale, legamento parodontale, osso alveolare, cemento) determinandone la distruzione irreversibile. Anche a livello dei tessuti perimplantari, l’accumulo di placca in sede sopra- e sottogengivale induce la comparsa di patologie placca-indotte: la mucosite perimplantare, reazione infiammatoria reversibile dei tessuti molli perimplantari che non determina perdita di osso, e la perimplantite, processo infiammatorio a carico dei tessuti perimplantari che si estende anche alla struttura ossea di sostegno di un impianto, determinandone il riassorbimento.
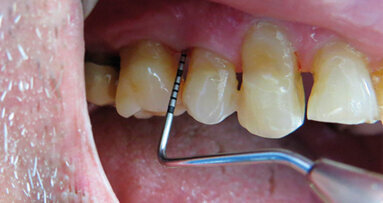
Un corretto e costante controllo domiciliare della placca rappresenta un requisito indispensabile per la prevenzione della malattia parodontale; la letteratura scientifica ha altresì dimostrato che il successo della terapia parodontale può essere ottenuto e mantenuto soltanto in presenza di un ottimo controllo di placca batterica da parte del paziente. In presenza di impianti osteointegrati, la mancata rimozione domiciliare della placca aumenta in modo significativo il rischio di insorgenza delle patologie infiammatorie perimplantari, e, analogamente a quanto dimostrato per le malattie parodontali, il controllo della placca rappresenta un momento fondamentale nella terapia delle patologie perimplantari placca-indotte. La difficoltà di ottenere e mantenere elevati livelli di igiene orale ha indirizzato la ricerca in campo odontoiatrico degli ultimi decenni ad individuare agenti chimici antiplacca da utilizzare, sotto forma di collutori o dentifrici, in aggiunta alle manovre di igiene orale domiciliare. Gli agenti antiplacca attualmente più utilizzati nella pratica clinica appartengono alla categoria degli antisettici, composti chimici caratterizzati da attività batteriostatica o battericida, generalmente dose-dipendente, che danneggiano, per contatto, la membrana batterica o determinano precipitazione dei componenti citoplasmatici, con effetti di gravità variabile (dal rallentamento della duplicazione cellulare fino alla morte del microrganismo).
embedImagecenter("Imagecenter_2_1229",1229,"small");
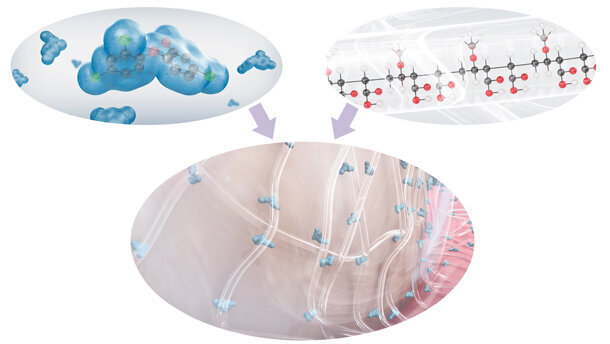
La clorexidina rappresenta, tra gli antisettici orali, la molecola più diffusamente prescritta dagli odontoiatri. Per il suo spettro di azione molto ampio, comprendente anche lieviti e virus, e soprattutto per la sua elevata sostantività (è attiva nel cavo orale fino a 12 ore), è considerata il gold-standard fra gli agenti chimici antiplacca. È un composto biguanidico, cationico, che presenta nella sua formula chimica un residuo guanidinico, responsabile della rapida e persistente adesione a superfici anioniche (idrossiapatite dello smalto, polisaccaridi della parete batterica, mucine salivari), un ponte carbonioso che conferisce alla molecola spiccate proprietà lipofile (elevata diffusibilità nei microrganismi) e un anello cloro-fenilico, che esplica attività biocida ad ampio spettro (Fig. 1). La molecola della clorexidina, per esplicare l’attività antiplacca, si lega alle membrane cellulari, alterandone la permeabilità; ha attività batteriostatica o battericida, a seconda della concentrazione, non ha effetti collaterali sistemici, poiché non è assorbita a livello gastro-intestinale, e anche dopo uso prolungato non induce resistenze batteriche o superinfezioni. La sua spiccata attività cationica e l’elevata sostantività sono alla base degli effetti collaterali conseguenti all’uso prolungato: pigmentazioni su denti, mucose, restauri (precipitazione di cromogeni anionici della dieta), alterazioni del gusto e sapore sgradevole, aumento dell’accumulo di tartaro, erosioni mucose (poco frequenti), parotidomegalia (rara).
La clorexidina è presente nelle seguenti formulazioni farmaceutiche: collutorio, spray (per usi localizzati), dentifricio, gel e vernici (per la prevenzione della carie radicolare). La formulazione più utilizzata è il collutorio, con concentrazione della clorexidina pari a 0,2% o 0,12%, con tempo di sciacquo pari a 30-60 secondi, con 10 o 15 ml di prodotto, rispettivamente; da pochi anni è disponibile in commercio anche il collutorio contenere clorexidina 0,3%. Lo sciacquo va effettuato almeno 30 minuti dopo l’uso di dentifrici contenenti sodiolaurilsolfato, per l’interazione antagonista con questo o altri surfattanti/detergenti anionici; analoga interazione è nota nei confronti della nistatina. Un’interazione inibente l’attività antiplacca potrebbe verificarsi anche nei prodotti commerciali contenenti sistemi anti-pigmentazione, sulla cui piena efficacia permangono ancora dubbi. L’agente anti-discolorante, infatti, inibisce l’attività pigmentante della clorexidina legandosi a uno dei due residui guanidinici, responsabili del legame con i cromogeni alimentari, ma anche con le superfici orali e batteriche. È noto, inoltre, che i migliori risultati antiplacca si ottengono nel breve termine, quando le manovre di igiene orale sono difficili, inadeguate o impossibili da effettuarsi. Al contrario, l’utilizzo a lungo termine, per periodi superiori a 10-15 giorni, è gravato dagli effetti collaterali sopra descritti. Inoltre, poiché sangue ed essudati infiammatori ne diminuiscono l’attività antiplacca, la clorexidina è più efficace quando utilizzata come presidio preventivo, cioè per inibire la formazione del biofilm su una superficie non ancora colonizzata dai batteri e per conservare lo stato di salute gengivale.
L’associazione fluoruro amminico-fluoruro stannoso, brevettata negli anni ‘80 dall’azienda svizzera GABA e formulata in collutorio o dentifricio (meridol®), è stata ampiamente studiata per i suoi effetti antiplacca. L’attività antibatterica dell’associazione è assicurata dallo ione stannoso, stabilizzato mediante inserimento nel polo idrofilo della molecola di fluoruro amminico, che ha a sua volta un’attività antibatterica intrinseca, grazie alla presenza del fluoro e della componente amminica. I dati provenienti da studi in vitro/in situ hanno evidenziato importanti effetti inibenti sulla crescita del biofilm e sulla vitalità delle specie batteriche in esso contenute; gli studi clinici hanno indicato un’attività antiplacca clinicamente significativa, inferiore a quella della clorexidina, ma priva degli effetti collaterali associati all’uso dell’antisettico biguanidico (pigmentazioni, alterazioni del gusto). Per tali caratteristiche, l’associazione fluoruro amminico-fluoruro stannoso ben si presta all’utilizzo prolungato, specie nei pazienti in terapia di mantenimento, nei quali permette di ottenere un migliore controllo della placca e della gengivite rispetto a quello ottenuto con la tradizionale igiene orale meccanica. Trial clinici documentano inoltre l’efficacia clinica del fluoruro amminico-fluoruro stannoso dopo chirurgia parodontale o implantare, supportandone l’uso alternativo alla clorexidina in queste situazioni cliniche, così come l’effetto sinergico dell’associazione collutorio-dentifricio-spazzolino meridol® sulla riduzione dell’indice di sanguinamento (62% rispetto alle misure standard di igiene orale domiciliare). La posologia d’uso del collutorio contenente l’associazione fluoruro amminico-fluoruro stannoso prevede 2 sciacqui giornalieri, ognuno della durata di 30 secondi, con 10 ml di prodotto non diluito.
Il triclosan è un antisettico fenolico presente da quasi 50 anni in prodotti commerciali per l’igiene personale o l’igiene delle mani in ambiente ospedaliero; dagli anni ’80 è presente nei dentifrici come agente antiplacca. È dotato di attività antibatterica ad ampio spettro d’azione e di proprietà anti-infiammatorie intrinseche. Il triclosan danneggia la membrana cellulare, inducendo rapidamente la morte dei microrganismi con cui viene a contatto, oppure ne inibisce la crescita interferendo con l’uptake degli amminoacidi; l’attività anti-infiammatoria è mediata dall’inibizione esercitata sulla biosintesi delle citochine pro-infiammatorie e dei mediatori flogistici, nonché sull’attività collagenolitica dei fibroblasti gengivali.
Colgate ha brevettato una specifica formulazione del triclosan con un copolimero PVM/MA (Polivinilmetil etere/acido maleico), che aumenta la sostantività dell’antisettico fino a 12 ore (Fig. 2). Gli studi disponibili in letteratura documentano altresì effetti benefici sulla flora sottogengivale, rallentamento della progressione della parodontite lieve/moderata, riduzione di tartaro, alitosi e carie. È stata altresì dimostrata l’efficacia del triclosan-copolimero nella riduzione della perdita di attacco nei giovani, specie a livello di tasche profonde, e la riduzione degli indici di placca e di flogosi, compreso il sanguinamento, a livello dei tessuti perimplantari. L’utilizzo, anche a lungo termine, del dentifricio contenente triclosan 0,3%-copolimero 2% non è gravato da nessun effetto collaterale specifico, come pigmentazione o disgeusia, né da insorgenza di resistenze o superinfezioni; la sua sicurezza, peraltro, è documentata da più di 80 studi e certificata da autorità regolatorie negli USA, in Canada e nell’Unione Europea.
L'articolo è stato pubblicato sul numero 2 di Implant Tribune Italy 2014
Le patologie infettive che colpiscono i tessuti parodontali e perimplantari hanno un comune primum movens eziopatogenetico: l’accumulo di placca ...
Alexandria (Usa) - Proteggere i bambini contro il precoce insorgere della carie è qualcosa che tutti i dentisti dovrebbero considerare come priorità. ...
Fitoterapici a base di componenti naturali, preparati a base di erbe che contengono principi attivi di piante o di altri componenti vegetali vengono ...
Un parodontologo è uno specialista di cui molti pazienti sanno molto poco ‒ fino al giorno in cui non ne devono cercare uno. I parodontologi sono ...
Curare l’igiene orale è ormai di fondamentale importanza al fine di mantenere una bocca e un corpo in perfetta salute. La ricerca ha ormai ...
TORONTO, Canada: I ricercatori canadesi hanno suggerito che la placca dentale, biofilm batterico che si forma sulle superfici dentali, può essere ...
I rapporti tra le patologie che interessano la polpa dentaria e quelle riguardanti il parodonto marginale si verificano attraverso le connessioni anatomiche...
FILADELFIA, USA: la malattia parodontale colpisce quasi il 60% degli adulti di età superiore ai 65 anni e comporta un onere considerevole dal punto di ...
Un valido aiuto nel combattere il biofilm batterico, causa dei principali insuccessi nel trattamento sia della parodontite sia della perimplantite, viene ...
Amsterdam. All’EuroPerio9 è stato annunciato un nuovo sistema per la classificazione dello stato di salute del parodonto (malattie e sue condizioni) ...
Live webinar
mer. 3 giugno 2026
19:00 (CET) Rome
Live webinar
gio. 4 giugno 2026
20:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
18:00 (CET) Rome
Live webinar
lun. 8 giugno 2026
19:00 (CET) Rome
Dr. Anthony Mak B.D.S, Prof. Marleen Peumans
Live webinar
lun. 8 giugno 2026
20:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
17:00 (CET) Rome
Live webinar
mer. 10 giugno 2026
20:00 (CET) Rome
Nacho Fernández-Baca DDS, MSc



 Austria / Österreich
Austria / Österreich
 Bosnia ed Erzegovina / Босна и Херцеговина
Bosnia ed Erzegovina / Босна и Херцеговина
 Bulgaria / България
Bulgaria / България
 Croazia / Hrvatska
Croazia / Hrvatska
 Repubblica Ceca e Slovacchia / Česká republika & Slovensko
Repubblica Ceca e Slovacchia / Česká republika & Slovensko
 Francia / France
Francia / France
 Germania / Deutschland
Germania / Deutschland
 Grecia / ΕΛΛΑΔΑ
Grecia / ΕΛΛΑΔΑ
 Ungheria / Hungary
Ungheria / Hungary
 Italia / Italia
Italia / Italia
 Paesi Bassi / Nederland
Paesi Bassi / Nederland
 nordisch / Nordic
nordisch / Nordic
 Polonia / Polska
Polonia / Polska
 Portogallo / Portugal
Portogallo / Portugal
 Romania e Moldavia / România & Moldova
Romania e Moldavia / România & Moldova
 Slovenia / Slovenija
Slovenia / Slovenija
 Serbia e Montenegro / Србија и Црна Гора
Serbia e Montenegro / Србија и Црна Гора
 Spagna / España
Spagna / España
 Svizzera / Schweiz
Svizzera / Schweiz
 Turchia / Türkiye
Turchia / Türkiye
 Gran Bretagna e Irlanda / UK & Ireland
Gran Bretagna e Irlanda / UK & Ireland
 Internazionale / International
Internazionale / International
 Brasile / Brasil
Brasile / Brasil
 Canada / Canada
Canada / Canada
 America Latina / Latinoamérica
America Latina / Latinoamérica
 USA / USA
USA / USA
 Cina / 中国
Cina / 中国
 India / भारत गणराज्य
India / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
Algeria, Marocco e Tunisia / الجزائر والمغرب وتونس
 Medio Oriente / Middle East
Medio Oriente / Middle East



















































To post a reply please login or register